-
(15分)硝酸铵在现代农业生产和国防中都占有重要地位,下图是云南天然气化工厂合成硝酸铵的简要生产工艺流程:
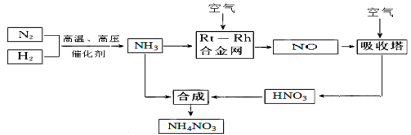
回答下列问题:
(1)N2的电子式 ,合成氨的反应中,若生成1g氨放出热量a KJ,写出该反应的热化学方程式 。
(2)氨催化氧化的化学方程式是 ,
试从化学反应速率和化学平衡原理分析温度、压强对合成氨反应的影响 。
(3)若输送NH3的管道某处发生泄漏,检测的简单方法 。
(4)农业生产上长期、过量使用化肥硝酸铵,会加重土壤酸化,原因是(用离子方程式回答) 。
(5)25℃时,将x mol NH4NO3溶于一定量水中,向该溶液中滴加y L氨水后溶液呈中性,则滴加氨水过程中水的电离平衡将 (填“正向” “不”或“逆向”)移动,所滴加氨水的物质的量浓度为 (25℃时,Kb(NH3·H2O)=2.0 × 10-5 mol·L-1)。
-
硝酸铵在工农业生产和国防中占有极为重要的位置,下面的流程图是硝酸铵的工业生产工艺过程.

根据图回答下列问题:(1)已知N2(g)+3H2(g)⇌2NH3(g)△H=-92.4 kJ/mol.请回答:①在500℃、1.01×105 kPa和铁催化条件下向一密闭容器中充入1 mol N2和3 mol H2,充分反应后,放出的热量小于92.4 kJ,理由:②为有效提高氢气的转化率,实际生产中宜采取的措施有.A.降低压强B.最适合催化剂活性的适当高温C.增大压强D.及时移出氨E.循环利用和不断补充氮气(2)氨催化氧化的化学方程式为4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)△H<0.
该反应的化学平衡常数表达式K=______,当温度升高时,K值______(填“增大”“减小”或“无影响”).
-
【化学――选修化学与技术】(15分)
氨在国民经济中占有重要地位,下图是合成氨的简要流程:
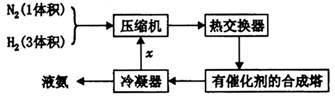
I.原料气的制备:
(1) 合成氨所需氮气来自空气,方法之一是将空气液化后再加热分馆;请另设计一种从空气中分离出氮气的方法:_________________________________________________________;
(2) 请写出工业上获得氢气的一种方法(用化学方程式表示)____________
II.原料气的净化:、
为防止催化剂“中毒”,原料气在进人压缩机之前必须经过净化、精制处理,“精制”过程通常是将含有少量CO、CO2、O2和H2S等杂质的原料气体通入含有氨水的醋酸亚铜二氨( )溶液,以获得纯净原料气。其中,吸收CO的反应为:
)溶液,以获得纯净原料气。其中,吸收CO的反应为:

(3) 为提髙CO吸收率,可采取的有效措施是__________________
(4) 除去氧气时,氧气将 氧化为
氧化为 ,则反应中还原剂与氧化剂的物质的量之比是____________;
,则反应中还原剂与氧化剂的物质的量之比是____________;
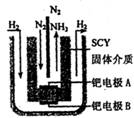
III.氨的合成:
(5)据报道,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了髙温常压下高转化率的电化学合成氨。其实验装置如图。请写出钯电极A上的电极反应式________________________
-
氨在国民经济中占有重要的地位,2008年,我国氨产量接近500万吨.下图是合成氨的简要流程.
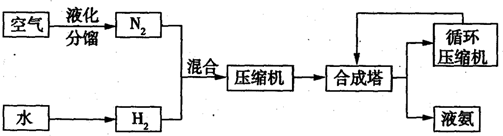
(1)下表是空气中部分气体的沸点.将空气液化加热分馏,依据下表数据判断,最先气化得到的气体是________.
| 气体名称 | 氨气 | 氧气 | 氦气 | 氖气 | 氩气 | 氪气 | 氚气 |
| 沸点/℃ | -196 | -183 | -269 | -264 | -186 | -153 | -108 |
(2)天然气、重油、煤都可以与水反应制得氢气.下表是某合成氨厂采用不同原料的相对投资和能量消耗.
| 原料 | 天然气 | 重油 | 煤 |
| 相对投资费用 | 1.0 | 1.5 | 2.0 |
| 能量消耗/J•t-1 | 28×109 | 38×109 | 48×109 |
①依据上表信息,你认为采用________为原料最好.
②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式:________.
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ•mol-1;
2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1;
试写出由C于水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式________.
(3)下表是在某种催化剂作用下用体积比为1:3的氮、氢混合气反应应达到平衡时的一些实验数据.
NH3含量%
压强/MPa
温度/℃ | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
①依据表中数据判断,合成氨反应N2+3H2 2NH3的△H________(填“>”、“<”或“无法判断”)0,请简要说明理由________;
2NH3的△H________(填“>”、“<”或“无法判断”)0,请简要说明理由________;
②该反应的化学平衡常数表达式为________.
③在300℃、10MPa下,合成氨反应达到平衡时,混合气体的体积是反应开始时的________倍.
-
(16分)氨、硝酸、硝酸铵、硝酸铜是重要的化工产品。工业合成氨与制备硝酸一般可连续生产,流程如下:

请回答下列问题:
(1)吸收塔中通入空气的作用是 。
下列可以代替硝酸镁加入到蒸馏塔中的是 。
A.浓硫酸 B.氯化钙 C.生石灰 D.硝酸亚铁
(2)制硝酸尾气中的氮氧化物常用尿素[CO(NH2)2]作为吸收剂,其主要的反应为:NO、NO2混合气与水反应生成亚硝酸,亚硝酸再与尿素[CO(NH2)2]反应生成CO2 和N2,请写出反应的化学方程式 、 。
(3)在氧化炉里,催化剂存在时氨气和氧气反应:
4NH3 + 5O2 4NO + 6H2O 4NH3 + 3O2
4NO + 6H2O 4NH3 + 3O2 2N2+ 6H2O
2N2+ 6H2O
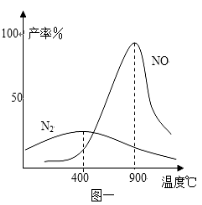
在不同温度时生成产物如图一所示。在氧化炉里,反应温度通常控制在800℃~900℃的理由是 。
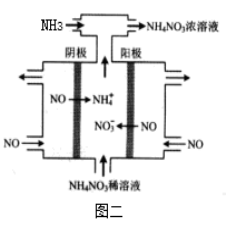
(4)如图二所示装置可用于电解NO制备 NH4NO3,电解总反应方程式为 ,需补充氨气的理由是 。
(5)工业上通常用铜与浓硝酸反应制得光谱纯硝酸铜晶体(化学式为Cu(NO3)2·3H2O,摩尔质量为242g/mol)。已知:25℃、1.01×105 Pa时,在密闭容器发生反应:2NO2 N2O4,达到平衡时,c(NO2)=0.0400 mol/L,c(N2O4)=0.0100 mol/L。
N2O4,达到平衡时,c(NO2)=0.0400 mol/L,c(N2O4)=0.0100 mol/L。
现用一定量的Cu与足量的浓高纯度硝酸反应,制得5.00 L已达到平衡的N2O4和NO2的混合气体(25℃、1.01×105 Pa),理论上生成光谱纯硝酸铜晶体的质量为________ g。
-
氨、硝酸、硝酸铵、硝酸铜是重要的化工产品.工业合成氨与制备硝酸一般可连续生产,流程如图1:请回答下列问题
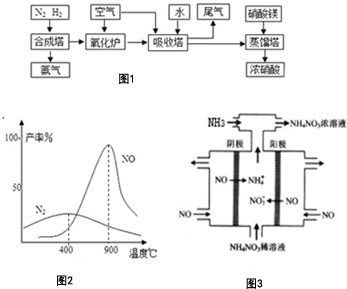
(1)吸收塔中通入空气的作用是 .
下列可以代替硝酸镁加入到蒸馏塔中的是 .
A.浓硫酸 B.氯化钙 C.生石灰 D.硝酸亚铁
(2)制硝酸尾气中的氮氧化物常用尿素[CO(NH2)2]作为吸收剂,其主要的反应为:NO、NO2混合气与水反应生成亚硝酸,亚硝酸再与尿素[CO(NH2)2]反应生成CO2和N2,请写出反应的化学方程式 、 .
(3)在氧化炉里,催化剂存在时氨气和氧气反应:4NH3+5O2⇌4NO+6H2O 4NH3+302⇌2N2+6H2O 在不同温度时生成产物如图一所示.在氧化炉里,反应温度通常控制在800℃~900℃的理由是 .
(4)如图二所示装置可用于电解NO制备 NH4NO3,电解总反应方程式为 ,需补充氨气的理由是 .
(5)工业上通常用铜与浓硝酸反应制得光谱纯硝酸铜晶体(化学式为Cu(NO3)2•3H2O,摩尔质量为242g/mol).已知:25℃、1.01×105Pa时,在密闭容器发生反应:2NO2⇌N2O4,达到平衡时,c(NO2)=0.0400mol/L,c(N2O4)=0.0100mol/L.
现用一定量的Cu与足量的浓高纯度硝酸反应,制得5.00L已达到平衡的N2O4和NO2的混合气体(25℃、1.01×105Pa),理论上生成光谱纯硝酸铜晶体的质量为 g.
-
I.氮和氮的化合物在国防建设、工农业生产和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂。它可由Cl2和NO在通常条件下反应制得,反应方程式为2NO(g)+Cl2(g) 2ClNO(g)。已知几种化学的键能数据如下表所示:
2ClNO(g)。已知几种化学的键能数据如下表所示:

当Cl2与NO反应生成ClNO的过程中转移了5mol电子,理论上放出的热量为____kJ.
(2)在一个恒容密闭容器中究入2molNO(g)和1 mol Cl2(g)发生(1)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示
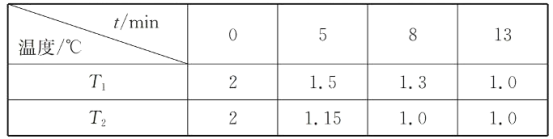
①T1________T2(填“>“”<”或”=”)。
②温度为T2℃时,起始时容器内的强为p0,则该反应的平衡常数Kp=______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
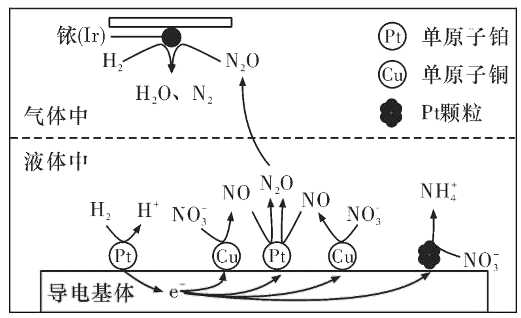
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-),其工作原理如图所示
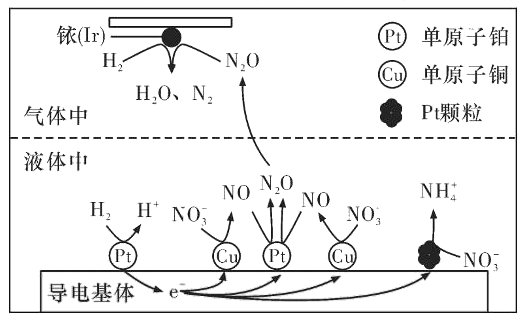
①Ir表面发生反应的方程式为_____________。
②若导电基体上的Pt颗粒增多,造成的后果是______________。
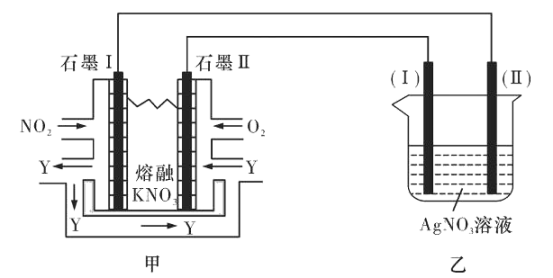
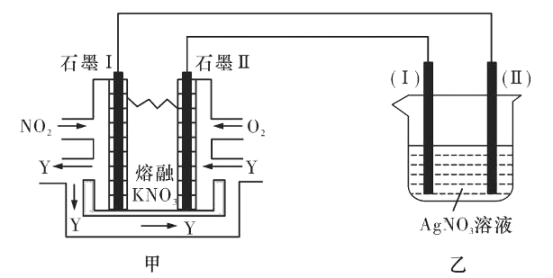
II:利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来精炼银,装置如图所示
 请回答下列问题:
请回答下列问题:
(4)①甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用,则石墨Ⅱ附近发生的电极反应式为________。
②若用10A的电流电解60min后,乙中阴极得到32.4gAg,则该电解池的电解效率为____%。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为96500C/mol)
-
I.氮和氮的化合物在国防建设、工农业生产和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂。它可由Cl2和NO在通常条件下反应制得,反应方程式为2NO(g)+Cl2(g) 2ClNO(g)。已知几种化学的键能数据如下表所示:
2ClNO(g)。已知几种化学的键能数据如下表所示:

当Cl2与NO反应生成ClNO的过程中转移了5mol电子,理论上放出的热量为____kJ.
(2)在一个恒容密闭容器中充入2molNO(g)和1 mol Cl2(g)发生(1)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示
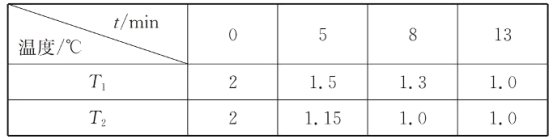
①T1________T2(填“>“”<”或”=”)。
②温度为T2℃时,起始时容器内的强为p0,则该反应的平衡常数Kp=______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-),其工作原理如图所示
①Ir表面发生反应的方程式为_____________。
②若导电基体上的Pt颗粒增多,造成的后果是______________。
II:利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来精炼银,装置如图所示
 请回答下列问题:
请回答下列问题:
(4)①甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用,则石墨Ⅱ附近发生的电极反应式为________。
②若用10A的电流电解60min后,乙中阴极得到32.4gAg,则该电解池的电解效率为____%。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为96500C/mol)
-
【化学——选修2:化学与技术】(15分)氮的化合物是重要的化工原料,在工农业生产中有很多重要应用。工业上合成氨的流程示意图如下:
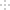
回答下列问题:
(1)25℃时合成氨反应热化学方程式为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol。在该温度时,取1 mol N2和3 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4 kJ。其原因是______________。
2NH3(g) ΔH=-92.4 kJ/mol。在该温度时,取1 mol N2和3 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4 kJ。其原因是______________。
(2)原料氢气的来源是水和碳氢化合物,写出工业生产中分别采用煤和天然气为原料制取氢气的化学反应方程式: , 。
(3)设备B的名称是________,其中m和n是两个通水口,入水口是 (填“m”或“n”),不宜从相反方向通水的原因 。
(4)设备C的作用是 。
(5)为了提高其产量,降低能耗,近年有人将电磁场直接加在氮气与氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了较好的产率。从化学反应本质角度分析,电磁场对合成氨反应的作用是 ;与传统的合成氨的方法比较,该方法的优点是 。
-
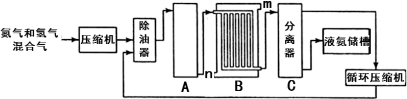
【化学—选修2:化学与技术】(15分)化学是人类进步的关键,化学为人类的生产、生活提供了物质保证。氮的化合物是重要的化工原料,在工农业生产中有很多重要应用。工业上合成氨的流程示意图如下:
回答下列问题:
(1)25℃时合成氨反应热化学方程式为:N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJ/mol。在该温度时,取1molN2和3molH2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4kJ。其原因是___________________________________________________________。
2NH3(g) ΔH=-92.4kJ/mol。在该温度时,取1molN2和3molH2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4kJ。其原因是___________________________________________________________。
(2)原料氢气的来源是水和碳氢化合物,写出工业生产中分别采用煤和天然气为原料制取氢气的化学反应方程式:___________________________, 。
(3)设备B的名称________________,其中m和n是两个通水口,入水口是 (填“m”或“n”),不宜从相反方向通水的原因_________________________________。
(4)设备C的作用是____________________________________________________。
(5)为了提高其产量,降低能耗,近年有人将电磁场直接加在氮气与氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了较好的产率。从化学反应本质角度分析,电磁场对合成氨反应的作用是_________________________________________________________________________________;
与传统的合成氨的方法比较,该方法的优点是________________________________________。













 请回答下列问题:
请回答下列问题:


 请回答下列问题:
请回答下列问题: