-
工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法。
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。
①请用离子方程式说明上述除杂的原理______________________。
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是_________(填序号)
A.Ba(NO3)2 B.BaCl2
C.Ba(OH)2 D.溶有NH3的BaCl2溶液
③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是___________。
(2)电解法处理酸性含铬废水(主要含有Cr2O72-)时,在废水中加入适量NaCl,以铁板作阴、阳极,处理过程中存在如下反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+ 以Cr(OH)3形式除去,下列说法不正确的是______(填序号)
A.阳极反应为Fe-2e-═Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有2mol Cr2O72-被还原
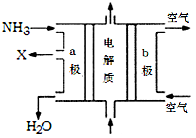
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。右图是该燃料电池示意图,产生的X气体可直接排放到大气中,a电极作_________极(填“正”“负”“阴”或“阳”),其电极反应式为___________。
-
工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法正确的是( )。
选项 污染物 处理措施 方法类别
A 废酸 加生石灰中和 物理法
B Cu2+等重金属离子 加硫酸盐沉降 化学法
C 含苯废水 用活性炭吸附 物理法
D 含纯碱的废水 加石灰水反应 化学法
-
工业废水中常含有不同类型的污染物 ,可采用不同的方法
,可采用不同的方法 处理。以下处理措施和方法正确的是
处理。以下处理措施和方法正确的是
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含苯废水 | 用活性炭吸附 | 物理法 |
| D | 含纯碱的废水 | 加石灰水反应 | 化学法 |
-
工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法正确的是
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含苯废水 | 用活性炭吸附 | 物理法 |
| D | 含纯碱的废水 | 加石灰水反应 | 化学法 |
-
(10分)(1)工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36。请用离子方程式说明上述除杂的原理____________。
(2)工业上为了处理含有Cr2O72-的酸性工业废水, 用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原 成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为_________________________________。
②常温下,Cr(OH)3的溶度积Ksp =1×10—32 ,溶液的pH至少为 ,才能使Cr3+沉淀完全。
③现用上述方法处理100m3含铬(+6价)78mg•L—1的废水,需用绿矾的质量为 kg。(写出计算过程,保留到小数点后一位)
-
水是人类生存和发展的宝贵资源,而水质的污染问题却越来越严重。目前,世界各国已高度重视这个问题,并采取积极措施进行治理。
(1)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法都正确的是________(填字母编号,可多选)。
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含纯碱的废水 | 加石灰水反应 | 化学法 |
(2)下图是某市污水处理的工艺流程示意图:
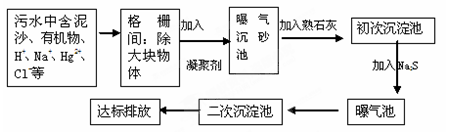
① 下列物质中不可以作为混凝剂(沉降剂)使用的是________(填字母编号,可多选)。
A.偏铝酸钠 B.氧化铝 C.碱式氯化铝 D.氯化铁
② 混凝剂除去悬浮物质的过程是________(填字母编号)。
A.只是物理过程 B. 只是化学过程 C. 是物理和化学过程
(3)在氯氧化法处理含CN一的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
某厂废水中含KCN,其浓度为650 mg·L-1。现用氯氧化法处理,发生如下反应:
KCN + 2KOH + Cl2 = KOCN + 2KCl + H2O 再投入过量液氯,可将氰酸盐进一步氯化为氮气。请配平下列化学方程式:口KOCN + 口KOH + 口Cl2→口CO2 + 口N2 + 口KCl + 口H2O若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯________g。
-
地球是我们赖以生存的美丽家园,人类在生产和生活中的下列活动能对环境造成污染的是 ( )。
①工业“三废”未经处理直接排放 ②植树造林,加大绿化面积 ③随意丢
弃废旧电池和塑料制品垃圾 ④生活污水的任意排放 ⑤减少空气中硫氧化
物和氮氧化物的排放,防止生成酸雨
A.①④⑤ B.②④⑤ C.①②⑤ D.①③④
-
下列对水体污染物的处理方法中,不正确的是
A.含H+的废水用中和法处理 B.含Cu2+、Fe3+的废水用沉淀法处理
C.含有细菌的废水用臭氧杀菌处理 D.含有重金属离子的废水用明矾处理
-
下列对水体污染物的处理方法中,不正确的是( )
A.含H+的废水用中和法处理
B.含Cu2+、Fe3+的废水用沉淀法处理
C.含有细菌的废水用臭氧杀菌处理
D.含有重金属离子的废水用明矾处理
-
下列对水体污染物的处理方法中,不正确的是
A.含有重金属离子的废水用明矾处理 B.含Cu2+、Fe3+的废水用沉淀法处理
C.含有细菌的污水用臭氧杀菌 D.含盐酸的酸性废水用中和法处理

