-
回答下列问题:
(1)已知下列反应:SO2 (g)+2OH–(aq) =SO32–(aq)+H2O(l) ΔH1;
ClO–(aq)+SO32–(aq)=SO42–(aq)+Cl–(aq) ΔH2;
CaSO4(s)=Ca2+(aq)+SO42–(aq) ΔH3。
则反应SO2(g)+Ca2+(aq)+ClO–(aq)+2OH–(aq)=CaSO4(s)+H2O(l)+Cl–(aq)的ΔH=______________。(用ΔH1、ΔH2、ΔH3表示)
(2)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,用甲烷制备合成气的反应为:①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-72 kJ·mol﹣1;
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+216 kJ·mol﹣1。现 有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
若x=0.2时,反应①放出的能量为________kJ;
若x=_________时,反应①与②放出(或吸收)的总能量为0。
(3)一定条件,在水溶液中1 mol Cl-和1 mol ClOx(x=1,2,3,4)的能量(kJ)相对大小如图所示。
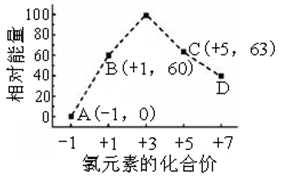
①D是________(填离子符号)。
②B→A+C反应的热化学方程式为_______________(用离子符号表示)。
-
煤燃烧排放的烟气中(主要含SO2、CO2)的SO2形成酸雨、污染大气,对烟气进行脱硫,回答下列问题:
(1)采用Ca(ClO)2烟气脱硫可得到较好的效果。已知下列反应:
①SO2(g)+2OH− (aq) =SO32− (aq)+H2O(l) ΔH1
②ClO− (aq)+SO32− (aq) =SO42− (aq)+Cl− (aq) ΔH2
③CaSO4(s) =Ca2+(aq)+SO42−(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO− (aq) +2OH− (aq) = CaSO4(s) +H2O(l) +Cl− (aq)的ΔH=_ 。
(2)采用氨水烟气脱硫,最终可得到氮肥。将相同物质的量的SO2与NH3溶于水所得溶液中c(H+)﹣c(OH-)= (填字母编号).
A.c(SO32-)﹣c(H2SO3)
B.c(SO32-)+c(NH3·H2O)﹣c(H2SO3)
C.c(HSO3-)+c(SO32-)﹣c(NH4+)
D.c(HSO3-)+2c(SO32-)﹣c(NH4+)
(3)烟气在较高温度经下图方法脱除SO2,并制得H2SO4。
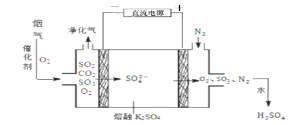
①在阴极放电的物质是 。
②在阳极生成SO3的电极反应式是 。
③已知室温下,Ksp(BaSO4)=1.1×10-10。将脱除SO2后制得的H2SO4配成pH=4 的H2SO4溶液,与pH=9的 Ba(OH)2 溶液混合,若所得混合溶液的 pH=7,则 Ba(OH)2 溶液与 H2SO4 溶液的体积比为 。欲使溶液中c(SO42-) =2.0×10-4mol·L-1,则应保持溶液中 c(Ba2+) = mol·L-1。
(4)一定条件下,用Fe2O3、NiO或Cr2O3作催化剂,利用如下反应回收燃煤烟气中的硫。反应为:2CO(g)+SO2(g) 2CO2(g)+S(l) ΔH= - 270KJ·mol-1其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,不考虑催化剂的价格因素,选择_ 为该反应的催化剂较为合理(选填序号)。
2CO2(g)+S(l) ΔH= - 270KJ·mol-1其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,不考虑催化剂的价格因素,选择_ 为该反应的催化剂较为合理(选填序号)。
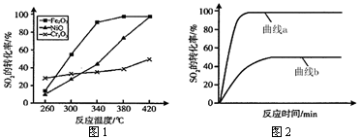
a. Cr2O3 b. NiO c. Fe2O3
选择该催化剂的理由是:_ 。
某科研小组用选择的催化剂,在380℃时,研究了n(CO) : n(SO2)分别为1:1、3:1时,SO2转化率的变化情况(图2)。则图2中表示n(CO) : n(SO2)=3:1的变化曲线为 。
-
下列化学反应中,属于氧化还原反应的是( )
A. SO2+2OH-=SO32—+H2O B. Al2O3+2OH-=2AlO2-+H2O
C. Cl2+2OH-=Cl-+ClO-+H2O D. HCO3-+OH-=CO32-+H2O
-
下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是( )
A.NaClO(aq)中通入过量SO2:ClO-+SO2+H2O=HClO+HSO3-
B.FeC12在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH-
C.AlCl3(aq)中投入少量Na:Al3++4Na+2H2O=AlO2-+4Na++2H2↑
D.FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2
-
(题文)以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH− ClO−+Cl−+H2O是放热反应。
ClO−+Cl−+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
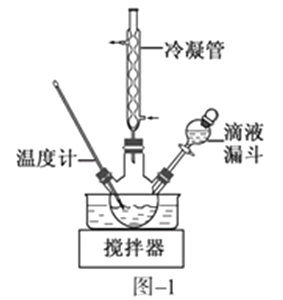
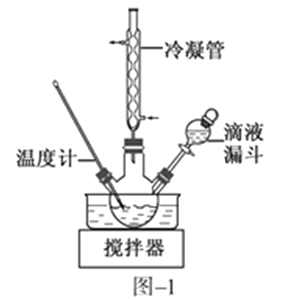
(2)步骤Ⅱ合成N2H4·H2O的装置如图−1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。
(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、 、
、 随pH的分布如图−2所示,Na2SO3的溶解度曲线如图−3所示)。
随pH的分布如图−2所示,Na2SO3的溶解度曲线如图−3所示)。

①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。
-
(题文)以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:
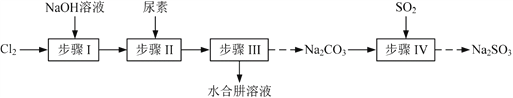
已知:①Cl2+2OH− ClO−+Cl−+H2O是放热反应。
ClO−+Cl−+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如图−1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。
(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、 、
、 随pH的分布如图−2所示,Na2SO3的溶解度曲线如图−3所示)。
随pH的分布如图−2所示,Na2SO3的溶解度曲线如图−3所示)。

①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。
-
以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH− ClO−+Cl−+H2O是放热反应。
ClO−+Cl−+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如题图1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。
(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、 、
、 随pH的分布如题图2所示,Na2SO3的溶解度曲线如题图3所示)。
随pH的分布如题图2所示,Na2SO3的溶解度曲线如题图3所示)。

①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装(结合图2、图3说明)
-
下列反应的离子方程式书写正确的是
A.98.3%的硫酸加入到稀氢氧化钡溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol
B.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3-
C.泡沫灭火器的反应原理:3HCO3-+Al3+=Al(OH)3↓+3CO2↑
D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O
-
下列离子方程式正确的是 ( )
A.Ca(HCO3)2与少量NaOH溶液的反应:Ca2++2HCO3-+2OH- == CaCO3↓+CO32-+2H2O
B.少量SO2通入NaClO溶液中:3ClO-+SO2+H2O == Cl-+SO42-+2HClO
C.用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42- ==2Mn2++10CO2↑+8H2O
D.NH4HSO4和少量Ba(OH)2溶液反应:NH4++H++SO42-+Ba2++2OH- == BaSO4↓+NH3·H2O+H2O
-
下列反应的离子方程式正确的是
A.HSO3-在溶液中发生水解:HSO3-+H2O SO32-+H3O+
SO32-+H3O+
B.向NaClO溶液中通入少量SO2:2ClOˉ+SO2+H2O=SO32ˉ+2HClO
C.苯酚钠溶液显碱性:C6H5O-+H2O C6H5OH+OH-
C6H5OH+OH-
D.惰性电极电解MgCl2溶液:Cl-+2H2O OH-+Cl2↑+H2↑
OH-+Cl2↑+H2↑
有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。










