制太阳能电池需要高纯硅,工业上用粗硅制高纯硅可通过以下反应实现:
①Si+3HCl(气) SiHCl3(气)+H2
②SiHCl3(气)+H2Si+3HCl(气)
对上述两个反应的叙述错误的是( )
A.都是置换反应 B.都是氧化还原反应
C.反应中硅元素都被还原 D.都不是离子反应
高一化学选择题简单题
制太阳能电池需要高纯硅,工业上用粗硅制高纯硅可通过以下反应实现:
①Si+3HCl(气) SiHCl3(气)+H2
②SiHCl3(气)+H2Si+3HCl(气)
对上述两个反应的叙述错误的是( )
A.都是置换反应 B.都是氧化还原反应
C.反应中硅元素都被还原 D.都不是离子反应
高一化学选择题简单题
制太阳能电池需要高纯硅,工业上用粗硅制高纯硅可通过以下反应实现:
Si(粗)+3HCl(g) SiHCl3(g) + H2、 ②SiHCl3 (g) + H2
Si(纯) + 3HCl(g)
对上述两个反应的叙述错误的是
A.两个反应互为可逆反应 B.都是置换反应
C.都是氧化还原反应 D.都不是离子反应
高一化学选择题中等难度题查看答案及解析
制太阳能电池需要高纯硅,工业上用粗硅制高纯硅可通过以下反应实现:
①Si+3HCl(气) SiHCl3(气)+H2
②SiHCl3(气)+H2Si+3HCl(气)
对上述两个反应的叙述错误的是( )
A.都是置换反应 B.都是氧化还原反应
C.反应中硅元素都被还原 D.都不是离子反应
高一化学选择题简单题查看答案及解析
高一化学选择题中等难度题查看答案及解析
制造太阳能电池需要高纯度的硅,工业上制高纯度的硅常用以下化学反应实现:
①Si(s)+3HCl(g) SiHCl3(g)+H2(g)(放热反应);②SiHCl3(g)+H2(g)
Si(s)+3HCl(g)。
以下对上述两个化学反应的叙述,其中错误的是( )
A.两个反应都是置换反应
B.反应②是放热反应
C.两个反应都有化学能与热能之间的转化
D.两个反应都是氧化还原反应
高一化学单选题中等难度题查看答案及解析
制造太阳能电池需要高纯度的硅,工业上制高纯度的硅常用以下化学反应实现:
①Si(s)+3HCl(g) SiHCl3(g)+H2(g)(放热反应)
②SiHCl3(g)+H2(g)Si(s)+3HCl(g)
以下是对上述两个化学反应的叙述,其中错误的是
A.两个反应都是置换反应 B.反应②是放热反应
C.两个反应都有化学能与热能之间的转化 D.两个反应都是氧化还原反应
高一化学选择题中等难度题查看答案及解析
制造太阳能电池需要高纯度的硅,工业上制高纯度硅常用以下反应来实现:
(1)Si(粗)+3HClSiHCl3+H2,
(2)SiHCl3+H2Si+3HCl。
对上述两个反应的下列叙述中错误的是( )
A. 两个反应都是置换反应
B. 两个反应中的H2均为还原剂
C. 两个反应的条件不同
D. 两个反应都是氧化还原反应
高一化学选择题中等难度题查看答案及解析
制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现:
①Si(s) +3HCl(g)SiHCl3(g) + H2(g) △H= -381kJ/mol
②SiHCl3(g)+H2(g)S(s) + 3HCl(g)
对上述两个反应的下列叙述中,不正确的是
A. 两个反应都是置换反应 B. 反应②是吸热反应
C. 两个反应互为可逆反应 D. 两个反应都是氧化还原反应
高一化学单选题中等难度题查看答案及解析
硅是太阳能电池的重要材料。工业冶炼纯硅的原理是:
粗硅冶炼:①SiO2 + 2CSi + 2CO
精炼硅:②Si + 3HClSiHCl3 + H2
③SiHCl3 + H2Si + 3HCl
化学反应与能量变化如图所示,回答下列问题:
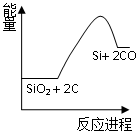
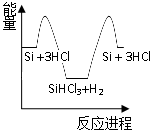
(1)反应①是_________反应(填“吸热”或“放热”),反应②是_________反应(填“吸热”或“放热”)。
(2)反应③破坏反应物中的化学键所吸收的能量_________形成生成物中化学键所放出的能量(填“大于”或“小于”)。
(3)研究物质变化时,人们可以从不同角度、不同层面来认识物质变化时所引起的化学键及能量变化。据此判断下列说法错误的是_________(双选)。
A.金属钠和氯气反应生成氯化钠后,其结构的稳定性增强,体系的能量降低
B.等量的硫蒸气和硫固体分别完全燃烧,前者放出的能量多
C.氮气分子内部存在着很强的共价键,故通常状况下氮气的化学性质很活泼
D.由石墨制取金刚石是吸热反应,可知金刚石比石墨稳定
E.由放热反应H2 + Cl2 ==== 2HCl来说,断裂1mol H—H键和1molCl—Cl键所吸收的能量小于形成2molH—Cl键所放出的能量
(4)在研究化学反应中的能量变化时,我们通常做下面的实验:
在一个小烧杯里,加入20g已经研磨成粉末的氢氧化钡晶体【Ba(OH)2.8H2O】,将小烧杯放在事先已滴有3—4滴水的玻璃片上,然后向烧杯中加入约10gNH4Cl晶体,并立即用玻璃棒迅速搅拌。写出实验过程中发生反应的化学方程式_________,该反应中反应物总能量_________生成物的总能量(填“大于”或“小于”),实验过程中立即用玻璃棒迅速搅拌的原因是_________。
高一化学填空题困难题查看答案及解析
科学家最新研制的利用氯化氢和氢气生产高纯硅的工艺流程如图所示:
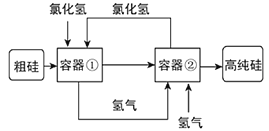
容器①中的反应为:Si(粗)+3HCl(g)=SiHCl3(l)+H2(g);容器②中进行的反应为:SiHCl3+H2=Si(纯)+3HCl,下列说法正确的是
A.反应①和②中HCl均作为氧化剂
B.该工艺流程的优点是部分反应物可循环使用
C.最好用分液的方法分离Si和SiHCl3
D.由反应①可知Si可与盐酸发生反应
高一化学单选题中等难度题查看答案及解析
(5分)晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl3 :Si + 3HCl(g) SiHCl3 + H2(g)
③SiHCl3与过量H2在1000-1100℃反应制得纯硅:
SiHCl3(g) + H2(g) Si(s)+ 3HCl(g)
已知SiHCl3能与H2O剧烈反应,且在空气中易自燃。
用SiHCI3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去)
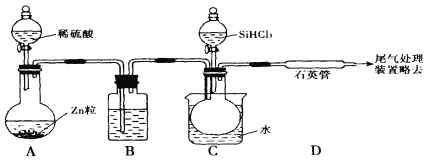
(1)装置B中的试剂是
(2)反应一段时间后,装置D中观察到的现象是 ,装置D不能采用普通玻璃管的原因是 。
(3)为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及 。
(4)为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂是 。(填写字母代号)
a.碘水 b.氯水 c. NaOH溶液 d. KSCN溶液 e. Na2SO3溶液
高一化学实验题中等难度题查看答案及解析