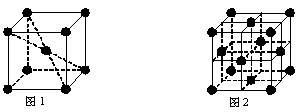-
(16分)下表为长式周期表的一部分,其中的编号代表对应的元素

试填空
(1)写出①、④两元素按原子个数比为1:1形成的化合物的电子式________;写出上表中元素⑨原子的外围电子排布式________;
(2)元素②与⑦形成的化合物的晶体类型是:___________________;
(3)元素⑤、⑥的第一电离能大小顺序是:________>________(用元素符号表示);元素③与元素①形成的X分子的空间构型为:________。请写出一种与N3—互为等电子体的分子的化学式________
(4)⑦、⑧两种元素能形成一种AB2型的共价分子,该分子属于________分子(填“极性”或“非极性”)⑤、⑦、 ⑾三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素的单质。请写出⑦、⑾两种元素形成的互化物的化学式________(正价元素写在前面)。
(5)元素⑩在元素周期表分区中属于________区元素,元素⑩在一定条件下形成的晶体的两种晶胞如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:________。
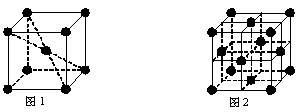
-
(18分)下表为长式周期表的一部分,其中的编号代表对应的元素。
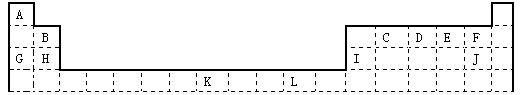
试填空。
(1)写出元素D与A形成的化合物的电子式 ,该化合物分子的空间构型是 ,其中元素D的杂化方式为 。
(2)J的离子结构示意图 ;K元素在周期表的位置 。元素L基态原子的电子排布式 。
(3)E、H、I 这三种元素的第一电离能由大到小的顺序是(填对应的元素符号) ;
(4)由D、J的氢化物相互作用所生成的物质所含化学键有下列的 。
A、离子键
B、非极性键
C、极性键
D、金属键
E、配位键
(5)用氢键表示式写出F的氢化物水溶液中所有氢键
-
下表为长式周期表的一部分,其中的编号代表对应的元素.
(1)写出上表中元素⑨原子的外围电子排布式______.
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为:______
(3)按要求完成下列各题
a.第一电离能:元素④______元素⑤(选填“>”、“=”、“<”).
b.与元素④所形成的单质互为等电子体的分子、离子的化学式______、______(各写一种).
c.元素④的气态氢化物X的水溶液在微电子工业中,可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______
d.由X与氧气、KOH溶液构成原电池,负极会产生元素④的单质.则其负极反应式为______.
(4)由元素③和⑧形成的液态化合物Z,是非极性的直线形分子.0.2mol的Z在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ.该反应的热化学方程式为______
(5)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:______.
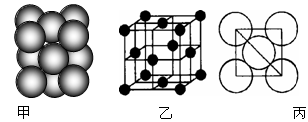
(6)元素⑩所形成的单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示. 已知该原子的半径为d,相对原子质量为M,NA代表阿伏加德罗常数,请回答:
晶体中该原子的配位数为______,一个晶胞中包含的原子数目为______;该晶体的密度为______
-
(9分)下表为周期表的一部分,其中的编号代表对应的元素。

(1)写出上表中的元素⑩原子的外围电子排布式。
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为________杂化,元素⑦与⑧形成的化合物的晶体类型是________。
(3)元素④的第一离能________元素⑤(填“>”、“=”或“<”)的第一电离能;元素④与元素①形成的X分子的空间构型为________。
(4)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是________。
(5)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,其离子方程式为________
-
(14分)下表为周期表的一部分,其中的编号代表对应的元素。

(1)写出上表中的元素⑩原子的外围电子排布式________。
(2)元素⑦与⑧形成的化合物的晶体类型是________。
(3)元素④的第一电离能________(填“>”、“=”或“<”)元素⑤的第一电离能;元素④与元素① 形成的X分子的空间构型为________。X沸点高于同族其它元素与元素①形成的化合物的沸点,其原因是________。
(4)第四周期所有元素的基态原子中,4p轨道半充满的是________(请填元素符号,下同),3d轨道半充满的原子是________,4s轨道半充满的是________。
(5)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,其离子方程式为________.
-
下表为长式周期表的一部分,其中的编号代表对应的元素。

根据上述表格中的十种元素填空:
1)表中属于ds区的元素是________(填编号)。
2)元素②与③形成的一种化合物是重要的化工原料,该化合物可用于人工降雨。有关该化合物分子的说法正确的是________。
A.分子中含极性共价键 B.含有1个σ键和2个π键
C.属于非极性分子 D.该化合物分子中,②原子采用sp2杂化
3)金属性最强的主族元素是________(填元素名称)。
4)⑤、⑥、⑦的离子半径由小到大的顺序是________(填化学式)。
5)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为________个; 该元素与元素①形成的分子X的空间构型为________。
-
下表为长式周期表的一部分,其中的编号代表对应的元素.
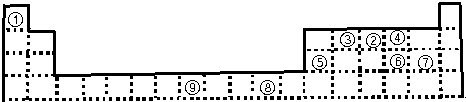
请回答下列问题:
(1)表中属于d区的元素是______(填编号).元素⑧的原子外围电子排布式______;
(2)③和⑦形成的常见化合物的晶体类型是______;②、③、④的电负性______>______>______ (用元素符号表示).判断依据______;
(3)某元素的特征电子排布式(价电子排布式)为nsnnpn+1,该元素为周期表中______(填编号);该元素与元素①形成的化合物x极易溶于水的原因是______;
(4)在⑧元素的硫酸盐溶液中加入过量的x的水溶液,可生成的配合物的化学式______,简要描述该配合物中化学键的成键情况______;
(5)②、③形成一种超硬、耐磨、耐高温的新型无机非金属材料,则其化学式为______,其硬度比金刚石______(填“大”或“小”).
-
下表为周期表的一部分,其中的编号代表对应不同的元素。
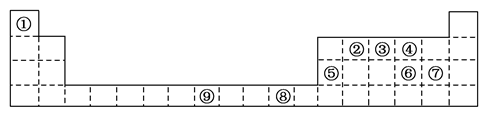
请回答下列问题。
(1)表中属于d区的元素是________(填编号);元素⑧的原子外围电子排布式是________。
(2)③和⑦形成的常见化合物的晶体类型是___ _____;②③④的电负性:________>________>________(用元素符号表示)。判断依据是__________________________,气态氢化物最稳定的是________(写化学式);
(3)某元素的特征电子排布式(价电子排布式)为nsnnpn+1,该元素为周期表中的________(填编号);该元素与元素①形成的化合物X极易溶于水的原因是________________________________。
(4)②⑥形成化合物的化学式为________,其熔点比金刚石的________(填“高”或“低”)。
(5)⑤的氧化物与⑥的最高价氧化物的水化物反应的方程式为_____________________________。
-
(16分)下表为长式周期表的一部分,其中的编号代表对应的元素。
(1)写出上表中元素⑨原子的外围电子排布式________。
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为:________
(3)按要求完成下列各题
a.第一电离能:元素④________元素⑤(选填“>”、“=”、“<”)。
b.与元素④所形成的单质互为等电子体的分子、离子的化学式________、________(各写一种)。
c.元素④的气态氢化物X的水溶液在微电子工业中,可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为________________________________
d.由X与氧气、KOH溶液构成原电池,负极会产生元素④的单质。则其负极反应式为_____________________________。
(4)由元素③和⑧形成的液态化合物Z,是非极性的直线形分子。0.2mol的Z在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ。该反应的热化学方程式为_________________________
(5)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:________。
(6)元素⑩所形成的单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。 已知该原子的半径为d pm,相对原子质量为M,NA代表阿伏加德罗常数,请回答:
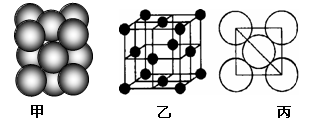
晶体中该原子的配位数为________,一个晶胞中包含的原子数目为 ________;该晶体的密度为________g·cm-3(用字母表示,不必化简)。
【解析】考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的物质可判断,①是H,②是Be,③是C,④是N,⑤是O,⑥是F,⑦是Mg,⑧S,⑨是Cr,⑩是Cu。
(1)因为全充满或半充满是稳定的,所以根据构造原理可知Cr的外围电子排布式3d54s1。
(2)③与①形成的水果催熟剂是乙烯,乙烯中含有碳碳双键,采用的是sp2杂化。
非金属性越强,第一电离能越大,所以N<O。氮气中含有14个电子,所以和氮气互为等电子体的分子是CO,离子是C22-。N的氢化物是氨气,N的化合价处于最低价态,被双氧水氧化生成氮气。原电池中负极失去电子,所以氨气在负极的电极反应式为2NH3-6e-+6OH-===N2+6H2O。
(4)S和C形成的非极性的直线形分子是CS2,所以反应的热化学方程式为CS2(l)+3O2(g)===CO2(g)+2SO2(g) ΔH=-1075 kJ/mol
(5)F是最活泼的非金属元素,H和F形成的氢化物中含有氢键,从而导致测得的值一般高于理论值。
(6)铜形成的是面心立方最密堆积,其配位数是12,根据乙中的结构特点可知一个晶胞中包含的原子数目为
 8×1/8+6×1/2=4。根据丙图可知该晶胞的边长为
8×1/8+6×1/2=4。根据丙图可知该晶胞的边长为 ,所以其密度为
,所以其密度为
-
(16分)下表为长式周期表的一部分,其中的编号代表对应的元素。
(1)写出上表中元素⑨原子的外围电子排布式________。
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为:________
(3)按要求完成下列各题
a.第一电离能:元素④________元素⑤(选填“>”、“=”、“<”)。
b.与元素④所形成的单质互为等电子体的分子、离子的化学式________、________(各写一种)。
c.元素④的气态氢化物X的水溶液在微电子工业中,可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为________________________________
d.由X与氧气、KOH溶液构成原电池,负极会产生元素④的单质。则其负极反应式为_____________________________。
(4)由元素③和⑧形成的液态化合物Z,是非极性的直线形分子。0.2mol的Z在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ。该反应的热化学方程式为_________________________
(5)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:________。
(6)元素⑩所形成的单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。 已知该原子的半径为d,相对原子质量为M,NA代表阿伏加德罗常数,请回答:
晶体中该原子的配位数为________,一个晶胞中包含的原子数目为 ________;该晶体的密度为________(用字母表示)