-
利用钛白工业的副产品FeSO4(含少量重金属离子)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:
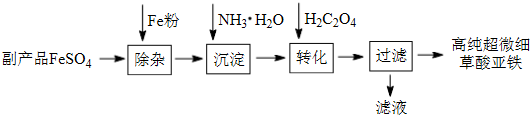
已知:①5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
②5C2O42-+2MnO4-+16H+═10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有___________;
(2)滤液经处理可得到副产品___________;
(3)实验室测定高纯超微细草酸亚铁组成的步骤依次为:
步骤1:准确称量一定量草酸亚铁样品,加入25mL 2mol/L的H2SO4溶解
步骤2:用0.2000mol/L标准KMnO4溶液与其反应,消耗其体积30.40mL。
步骤3:向滴定后的溶液中加入2g Zn粉和5mL 2mol/L的H2SO4溶液,将Fe3+还原为Fe2+
步骤4:过滤,滤液用上述标准KMnO4溶液进行反应,消耗溶液10.00mL.
则样品中C2O42-的物质的量为__________;(写出计算过程);
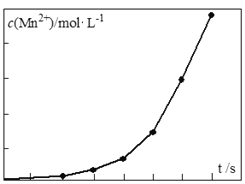
(4)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如图,其变化趋势的原因可能为__________;

-
利用钛白工业的副产品FeSO4(含Al2(SO4)3和少量重金属离子)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:
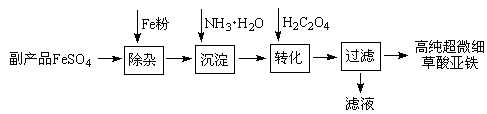
已知:①5Fe2++ MnO4-+8H+=5Fe3+ +Mn2++4H2O
5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有 。
(2)滤液经处理可得到副产品 。
(3)实验室测定高纯超微细草酸亚铁组成的步骤依次为:
步骤1:准确称量一定量草酸亚铁样品,加入25 mL 2 mol·L-1的H2SO4溶解。
步骤2:用0.2000 mol·L-1标准KMnO4溶液滴定,消耗其体积30.40 mL。
步骤3:向滴定后的溶液中加入2 g Zn粉和5 mL 2 mol·L-1的H2SO4溶液,将Fe3+还原为Fe2+。
步骤4:过滤,滤液用上述标准KMnO4溶液滴定,消耗溶液10.00 mL。
则样品中C2O42-的物质的量为 。(写出计算过程)
(4)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应 液中Mn2+的浓度随反应时间t的变化如图,其变化趋势的原因可能为 。

-
利用钛白工业的副产品FeS04[含A12(S04)3和少量重金属离子]可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:
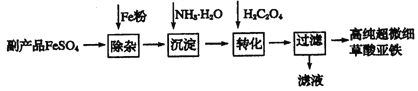
已知:
①5Fe2++MnO4﹣+8H+═5Fe3++Mn2++4H2O
②5C2O42﹣+2MnO4﹣+16H+═10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有_____。
(2)滤液经处理可得到副产品________,可作肥料。
(3)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如图,其变化趋势的原因可能为_________。

(4)实验室测定高纯超微细草酸亚铁组成的步骤依次为
步骤1:准确称量一定量草酸亚铁样品,加入的H2S04溶解。
步骤2:用0.200 0mol•L-1标准KMn04溶液滴定,消耗其体积30.40 mL。
步骤3:向滴定后的溶液中加入2gZn粉和5mL2mol•L-1的H2S04溶液,将Fe3+还原为Fe2+
步骤4:过滤,滤液用上述标准KMn04溶液滴定,消耗溶液10.00 mL.
计算样品中C2O42-的物质的量_________________。(写出计算过程)
-
利用钛白工业的副产品FeSO4(含TiO2+、Al3+)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:
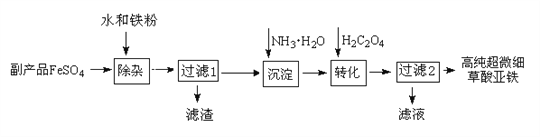
已知:
①过滤1得到的滤渣的主要成分是Al(OH)3、H2TiO3。
②5Fe2++ MnO4-+8H+=5Fe3+ +Mn2++4H2O
5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有_____。
(2)沉淀反应的离子方程式是______________。
(3)实验室测定高纯超微细草酸亚铁组成的步骤依次为:
步骤1:准确称量一定量草酸亚铁样品,加入30 mL 2 mol·L-1的H2SO4溶解。
步骤2:用0.2000 mol·L-1标准KMnO4溶液滴定,消耗其体积31.60 mL。
步骤3:向滴定后的溶液中加入3g Zn粉和8 mL 2 mol·L-1的H2SO4溶液,将Fe3+还原为Fe2+。
步骤4:过滤,滤液用上述标准KMnO4溶液滴定,消耗溶液10.00 mL。
则样品中C2O42-的物质的量为______。(写出计算过程)
(4)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如下图,其变化趋势的原因可能为________。
-
(09年江苏化学·16)(8分)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:

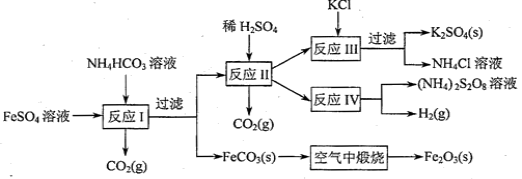
 (1)反应I前需在FeSO4溶液中加入 (填字母),以除去溶液中的Fe3+。
(1)反应I前需在FeSO4溶液中加入 (填字母),以除去溶液中的Fe3+。
 A.锌粉 B.铁屑 C.KI溶液 D.H2
A.锌粉 B.铁屑 C.KI溶液 D.H2
 (2)反应Ⅰ需控制反应温度低于35℃,其目的是 。
(2)反应Ⅰ需控制反应温度低于35℃,其目的是 。
 (3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是 。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是 。
 (4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为 。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为 。
-
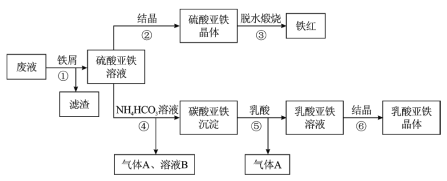
利用酸解法制钛白粉产生的废液[含有大量 和少量
和少量 、
、 ],生产铁红和补血剂乳酸亚铁。其生产步骤如下:
],生产铁红和补血剂乳酸亚铁。其生产步骤如下:
已知: 可溶于水,在水中可以电离为
可溶于水,在水中可以电离为 和
和 水解成
水解成 沉淀为可逆反应;乳酸亚铁晶体的化学式为:
沉淀为可逆反应;乳酸亚铁晶体的化学式为: 。请回答:
。请回答:
(1)步骤①加入铁屑的目的一是还原少量 ;二是使少量
;二是使少量 转化为
转化为 滤渣,用平衡移动的原理解释得到滤渣的原因________。
滤渣,用平衡移动的原理解释得到滤渣的原因________。
(2)硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为________。
(3)步骤④的离子方程式是______。
(4)步骤⑥所得溶液需隔绝空气______、________过滤、洗涤、干燥得乳酸亚铁晶体。该晶体存放时应____________。
-
钛白粉(TiO2)是重要的白色颜料,LiFePO4是锂离子电池的正极材料。一种利用钛铁矿( 主要成分为FeTiO3 和少量Fe2O3 )进行钛白粉和LiFePO4 的联合生产工艺如下图所示:
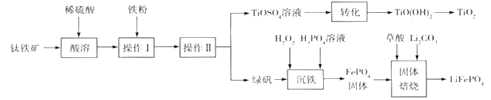
回答下列问题:
(1) LiFePO4中Fe的化合价是_______________________。
(2)钛铁矿“酸溶”前需要进行粉碎,粉碎的目的是__________________________________。
(3)用离子方程式表示操作I加入铁粉的目的:__________________________。操作II为一系列操作,名称是加热浓缩、冷却结晶、过滤,其中用到的陶瓷仪器的名称是___________。
(4)TiO2+易水解,则其水解的离子方程式为______________________;“转化”利用的是TiO2+的水解过程,需要对溶液加热,加热的目的是________________________________。
(5)“沉铁”的的是使Fe3+生成FePO4,当溶液中c(PO43-)= 1.0×10-17mol/L时可认为Fe3+ 沉淀完全,则溶液中Fe3+沉淀完全时的c(Fe3+)=_______mol/L[已知:该温度下,Ksp(FePO4)=1.0×10-22]。
(6)由“沉铁”到制备LiFePO4的过程中,所需17% H2O2溶液与草酸( H2C2O4)的质量比是_____。
-
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如下图所示:
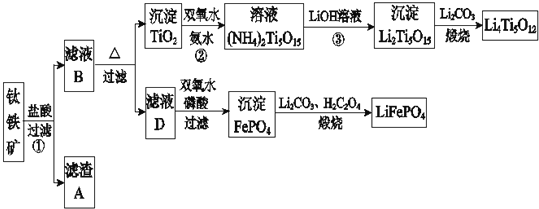
已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O。
(1)化合物FeTiO3中铁元素的化合价是_______。
(2)滤渣A的成分是______________。
(3)滤液B中TiOCl42-转化生成TiO2的离子方程式是___________________。
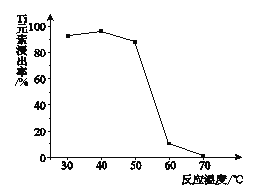
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如下图所示。反应温度过高时,Ti元素浸出率下降的原因是_______________。
(5)反应③的化学方程式是__________________。
(6)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)作电极组成电池,其工作原理为:Li4Ti5O12+3LiFePO4 Li7Ti5O12+3FePO4。该电池充电时阳极反应式是_____________________。
Li7Ti5O12+3FePO4。该电池充电时阳极反应式是_____________________。
-
乙二酸(HOOC—COOH)也称草酸,是一种重要的化工原料和化工产品。利用石油化工产品中的烷烃可以生成草酸,生产流程如下:

已知上述框图中有机物B的相对分子质量比有机物A的相对分子质量大79。
请回答下列问题:
(1)A的结构简式是_______________ ;D的名称__________________。
(2)写出有关的化学方程式:
B→C:________________________________________________________。
D→E:________________________________________________________。
(3)A生成B的反应类型是__________;C生成D的反应类型是___________。
-
乙二酸(HOOC—COOH)也称草酸,是一种重要的化工原料和化工产品。利用石油化工产品中的烷烃可以生成草酸,生产流程如下:

已知上述框图中有机物B的相对分子质量比有机物A的相对分子质量大79。
请回答下列问题:
(1)A的结构简式是_______________ ;D的名称__________________。
(2)写出有关的化学方程式:
B→C:________________________________________________________。
D→E:________________________________________________________。
(3)A生成B的反应类型是__________;C生成D的反应类型是___________。













