-
前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是_________(填元素符号,下同)。
(2)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式_________,黄血盐晶体中各种微粒间的作用力不涉及______________(填序号)。
a.金属键 b.共价键 c.配位键
d.离子键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为___________________,很多不饱和有机物在E催化下可与H2发生加成:如①CH2=CH2 ②HC≡CH ③ ④HCHO。其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为______________,它加成后产物甲醇的熔、沸点比CH4的熔、沸点高,其主要原因是____________。
④HCHO。其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为______________,它加成后产物甲醇的熔、沸点比CH4的熔、沸点高,其主要原因是____________。
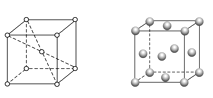
(4)金属C、F晶体的晶胞如下图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为_________。金属F的晶胞中,若设其原子半径为r,晶胞的边长为a,根据硬球接触模型,则r = _______a,列式表示F原子在晶胞中的空间占有率______________(不要求计算结果)。
-
前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于第四周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,C位于s区且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且位于同一族原子序数相差为2。
(1)六种元素中第一电离能最小的是__________(填元素符号,下同),电负性最大的是__________。
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式__________,1 mol AB+中含有π键的数目为____________,黄血盐晶体中各种微粒间的作用力不涉及__________(填序号)。
a.离子键 b.共价键 c.配位键
d.金属键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为____________,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③ 、④HCHO。其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为____________,它与氢气的加成产物熔、沸点比CH4的熔、沸点高,其主要原因是______________________________________(须指明加成产物是何物质)。
、④HCHO。其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为____________,它与氢气的加成产物熔、沸点比CH4的熔、沸点高,其主要原因是______________________________________(须指明加成产物是何物质)。
-
(18分)A、B、C、D、E、F为原子序数依次增大的短周期元素,G为第四周期元素,B、C相邻且同周期,A、D同主族。A、C能形成两种化合物甲和乙,原子个数比分别为2∶1和1∶1,甲为常见的溶剂。E是地壳中含量最多的金属元素。F元素为同周期电负性最大的元素。D和F可形成化合物丙,E和F可形成化合物丁。G为第四周期未成对电子数最多的元素。请回答下列问题:
(1)写出G基态原子的电子排布式
(2)B和C比较,第一电离能较大的元素是 (填元素符号),其原因为
(3)A与B形成的化合物易溶于化合物甲,其主要原因是
(4)甲、乙两分子中含有非极性共价键的是 (填分子式),它中心原子的杂化方式是
(5)已知化合物丁熔点190℃,沸点183℃,结构如右图所示。
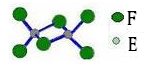
①丙和丁比较,熔点较低的化合物是 (填化学式),其原因为
②则丁含有的作用力有 (填序号)。
A.离子键 B.共价键 C.金属键
D.配位键 E.范德华力
-
前四周期原子序数依次增大的六种元素A、B、C、DE、、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2.
(1)六种元素中第一电离能最小的是______________;(填元素符号,下同)
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂);请写出黄血盐的化学式____________,1mol AB-中含有π键的数目为____________(阿伏加德罗常数的值为NA),黄血盐晶体中各种微粒间的作用力不涉及____________(填序号);
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.分子间的作用力
(3)很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③ 、④HCHO.其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为___________形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是___________________。
、④HCHO.其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为___________形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是___________________。
-
X、Y、Z、W为原子序数依次增大的短周期主族元素,已知X、Y为同周期的相邻元素且形成的某种二元化合物能形成光化学烟雾,Z为金属元素且Z原子的L层电子数比其它各层上电子数之和大5,W的最高价氧化物对应水化物和其氢化物均为强酸。下列说法不正确的是
A. X、Y、Z、W原子半径大小:W>Z>Y>X B. 最简单氢化物的稳定性:X<Y
C. WY2能对自来水进行杀菌消毒 D. Z单质在Y单质和W单质中均可燃烧
-
已知 X、Y、Z、W 四种短周期元素的原子序数依次增大。其中 X 与 Y、Z、W 所形成的常见化合 物(10e 或 18e)在常温下均为气态,在元素周期表中 Z 与 W 相邻,Y 的最高价氧化物的水化物与其氢化 物反应生成盐,且 Y 的核电荷数与 W 的最外层电子数相同。
(1)Z 离子的结构示意图是_____。
(2) X、Y、W 可组成一种化合物,原子个数比为 4:1:1,该化合物的化学式是_____,其中含有的化学键 有_____。
(3)X 与 Y 所形成的分子的电子式为_____,它比同主族其他元素的氢化物沸点高的原因是______。
(4)请从 Z、W 的结构上说明 Z、W 两种元素非金属性的强弱_____。
-
A、B、C、D、E、F为原子序数依次增大的短周期元素,B、C相邻且同周期,A、D同主族。A、C能形成两种化合物甲和乙,原子个数比分别为2∶1和1∶1,甲为常见的溶剂。E是地壳中含量最多的金属元素。F元素为同周期电负性最大的元素。D和F可形成化合物丙,E和F可形成化合物丁。G为第四周期未成对电子数最多的元素
请回答下列问题:
(1)写出G基态原子的外围电子排布式________。
(2)B和C比较,第一电离能较大的元素是________(填元素符号),其原因为________。
(3)甲、乙两分子中含有非极性共价键的是________(填分子式)。
(4)已知化合物丁熔点190℃,沸点183℃,结构如图所示。
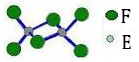
①丙和丁比较,熔点较低的化合物是________(填化学式),其原因为________。
②则丁晶体中含有的作用力有________(填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力
(5)G3+与元素A、C、F构成配合物戊,在含有0.001mol戊的溶液中加入过量AgNO3溶液,经过滤、洗涤、干燥后,得到287mg白色沉淀。已知该配合物的配位数为6,则戊的化学式为________。
(6)三聚氰胺(结构如图)由于其含氮量高被不法奶农添加到牛奶中来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石。三聚氰胺中N原子的杂化形式是________。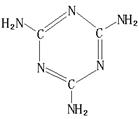
-
已知X、Y、Z、W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物(10e或18e)在常温下均为气态,在元素周期表中Z与W相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的外成层电子数相同。
(1)Z离子的结构示意图是_____________________________。
(2)X、Y、W可组成一种化合物,原子个数比为4:1:1,该化合物的化学式是_______,其中含有的化学键有__________________。
(3)X与Y所形成的分子的电子式为__________,它比同主族其他元素的氢化物沸点高的原因是__________________。
(4)请从Z、W的结构上说明Z、W两种元素非金属性的强弱_________________。
-
已知X、Y、Z、W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物(10e或18e)在常温下均为气态,在元素周期表中Z与W相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的外成层电子数相同。
(1)Z离子的结构示意图是_____________________________。
(2)X、Y、W可组成一种化合物,原子个数比为4:1:1,该化合物的化学式是_______,其中含有的化学键有__________________。
(3)X与Y所形成的分子的电子式为__________,它比同主族其他元素的氢化物沸点高的原因是__________________。
(4)请从Z、W的结构上说明Z、W两种元素非金属性的强弱_________________。
-
(12分)已知X,Y,Z,W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物(10e或18e)在常温下均为气态,在元素周期表中Z与W相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的最外层电子数相同。
(1)Z离子的结构示意图是 。
(2)X、Y、W可组成一种化合物,原子个数比为4:1:1,该化合物的化学式是 ,其中含有的化学键有 。
(3)X与Y所形成的分子的电子式为 ,它比同主族其他元素的氢化物沸点高的原因是 。
(4)请设计一个简单的实验,说明Z、W两种元素非金属性的强弱,写出实验方法和现象: ___。



