-
某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol/L的MgCl2溶液中各加入10滴2 mol/L NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
实验序号
加入试剂
实验现象
Ⅰ
4 mL 2 mol/L NH4Cl 溶液
沉淀溶解
Ⅱ
4 mL蒸馏水
沉淀不溶解
(1)测得实验Ⅰ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因 。
(2)同学们猜测实验Ⅰ中沉淀溶解的原因有两种:
猜想1:氢氧化镁电离出OH-离子,与氯化铵电离出来的铵根离子反应生成氨水.
猜想2: 。
(3)为验证猜想,又设计了以下实验
序号
实验内容
结 果
1
测定醋酸铵溶液的pH
pH约为7,溶液呈中性
2
取少量的相同质量的氢氧化镁分别盛放在试管中,分别向其中滴加醋酸铵溶液和氯化铵溶液
固体均溶解
①用醋酸铵溶液与氢氧化镁反应的原因是 。
②实验证明猜想正确的是 (填“1”或“2”)。
(4)实验Ⅱ观察到沉淀不溶解。该实验的目的是 。
高二化学实验题困难题查看答案及解析
-
某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
(查阅资料)25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
(实验探究)向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀。
(1)分别向两支试管中加入不同试剂,记录实验现象如表:(表中填空填下列选项中字母代号)
试管编号
加入试剂
实验现象
Ⅰ
2滴0.1mol/LFeCl3溶液
①_____
Ⅱ
4mL2mol/LNH4Cl溶液
②_____
A、白色沉淀转化为红褐色沉淀 B、白色沉淀不发生改变
C、红褐色沉淀转化为白色沉淀 D、白色沉淀溶解,得无色溶液
(2)测得试管Ⅰ中所得混合液pH=6,则溶液中c(Fe3+)=______________。
(3)同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
猜想2:____________。
(4)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明猜想正确的是__________(填 “1”或“2”)。
高二化学综合题中等难度题查看答案及解析
-
实验是化学学习中非常重要的内容,根据下面两个实验回答问题。
(一)某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
(查阅资料)25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
(实验探究)向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀。
(1)分别向两支试管中加入不同试剂,记录实验现象如表:(表中填空填下列选项中字母代号)
试管编号
加入试剂
实验现象
Ⅰ
2滴0.1mol/LFeCl3溶液
①_____
Ⅱ
4mL2mol/LNH4Cl溶液
②_____
A.白色沉淀转化为红褐色沉淀 B.白色沉淀不发生改变
C.红褐色沉淀转化为白色沉淀 D.白色沉淀溶解,得无色溶液
(2)同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
猜想2:____________________________________________________________。
(3)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明猜想正确的是____(填 “1”或“2”)。
(二)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量。准确称取5.000 0 g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI===3K2SO4+3I2+3H2O),充分反应后将混合溶液稀释至250 mL,然后取25.00 mL用5.0×10-4 mol·L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+2S2O32-===2I-+S4O62-)。有关实验数值如下表所示。
滴定次数
待测液的体积(mL)
滴定前的读数(mL)
滴定后的读数(mL)
第一次
25.00
0.00
15.90
第二次
25.00
0.00
14.99
第三次
25.00
0.00
15.01
该碘盐中碘元素的百分含量为________。(保留三位有效数字)下列操作中,会导致所测得的碘元素的百分含量偏大的是________。
a.滴定终点时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水
高二化学填空题简单题查看答案及解析
-
(1)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成 沉淀(填化学式),生成该沉淀的离子方程式为 。已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
高二化学填空题中等难度题查看答案及解析
-
(1)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成 沉淀(填化学式),生成该沉淀的离子方程式为 。已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
高二化学填空题中等难度题查看答案及解析
-
某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、
、
、
、Cl-中的几种,现进行如下实验:
①取少量原溶液,滴加氢氧化钠溶液的过程中无沉淀生成;
②另取少量原溶液,逐滴加入5 mL 0.2 mol·L-1盐酸,开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失;
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液得到沉淀0.43 g。
下列说法中正确的是( )。
A.该溶液中一定不含Ba2+、Al3+、Mg2+、
、Cl-
B.该溶液中一定含有K+、
、
、Cl-
C.该溶液中是否含有K+需做焰色反应(透过蓝色钴玻璃片观察)进行判断
D.该溶液中可能含有Cl-
高二化学单选题简单题查看答案及解析
-
将一定质量的Mg-Al合金投入到100mL一定物质的量浓度的HCl中,合金全部溶解,向所得溶液中滴加5mol/LNaOH溶液至过量,生成沉淀质量与加入NaOH溶液的体积关系如下图所示。 求:
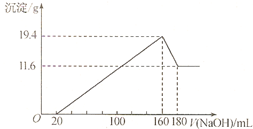
(1)写出20ml-160ml阶段的离子反应方程式 ;
(2)160ml-180ml阶段的离子反应方程式 ;
(3)原合金分别与足量的稀硫酸和氢氧化钠溶液反应产生气体的在同温同压下的体积比为___________。
(4)HCl的物质的量浓度为 mol/L。
高二化学填空题困难题查看答案及解析
-
将Mg、Cu组成的2.64 g混合物投入到100 mL稀硝酸中完全溶解,并收集还原产物NO气体(还原产物只有一种)。然后向反应后的溶液中逐滴加入2 mol·L-1 NaOH溶液,下图是生成沉淀的质量与滴入NaOH溶液体积间的关系图。以下说法不正确的是( )
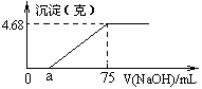
A.稀硝酸的浓度为1.9 mol/L
B.生成的NO在标况下的体积为0.896 L
C.a的值为15
D.Cu的物质的量为0.02 mol
高二化学选择题困难题查看答案及解析
-
将Mg、Cu组成的2.64 g混合物投入到100 mL稀硝酸中完全溶解,并收集还原产物NO气体(还原产物只有一种)。然后向反应后的溶液中逐滴加入2 mol·L-1 NaOH溶液,下图是生成沉淀的质量与滴入NaOH溶液体积间的关系图。以下说法不正确的是( )

A.稀硝酸的浓度为1.9 mol/L
B.生成的NO在标况下的体积为0.896 L
C.a的值为15
D.Cu的物质的量为0.02 mol
高二化学选择题简单题查看答案及解析
-
实验小组同学对乙醛与新制的Cu(OH)2反应的实验进行探究。
实验Ⅰ:取2mL 10%的氢氧化钠溶液于试管中,加入5滴2%的CuSO4溶液和5滴5%的乙醛溶液,加热时蓝色悬浊液变黑,静置后未发现红色沉淀。
实验小组对影响实验Ⅰ成败的因素进行探究:
(1)探究乙醛溶液浓度对该反应的影响。
编号
实验Ⅱ
实验Ⅲ
实验方案


实验现象
加热,蓝色悬浊液变红棕色,静置后底部有大量红色沉淀
加热,蓝色悬浊液变红棕色,静置后上层为棕黄色油状液体,底部有少量红色沉淀
已知:乙醛在碱性条件下发生缩合反应:CH3CHO+CH3CHO
CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
① 能证明乙醛被新制的Cu(OH)2 氧化的实验现象是______。
② 乙醛与新制的Cu(OH)2 发生反应的化学方程式是______。
③ 分析实验Ⅲ产生的红色沉淀少于实验Ⅱ的可能原因:______。
(2)探究NaOH溶液浓度对该反应的影响。
编号
实验Ⅳ
实验Ⅴ
实验方案


实验现象
加热,蓝色悬浊液变黑
加热,蓝色悬浊液变红棕色,
静置后底部有红色沉淀
依据实验Ⅰ→Ⅴ,得出如下结论:
ⅰ. NaOH溶液浓度一定时,适当增大乙醛溶液浓度有利于生成Cu2O。
ⅱ. 乙醛溶液浓度一定时,______。
(3)探究NaOH溶液浓度与乙醛溶液浓度对该反应影响程度的差异。
编号
实验Ⅵ
实验Ⅶ
实验方案


实验现象
加热,蓝色悬浊液变黑
加热,静置后底部有红色沉淀
由以上实验得出推论: ______。
高二化学实验题中等难度题查看答案及解析