-
利用废旧锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO的一种制备流程图如下:

已知:Ksp[Zn(OH)2]= 1.2×10—17;Zn(OH)2既能溶于强酸,又能溶于强碱.还能溶于氨水,生成[Zn(NH3)4]2+.
(1)溶液A中加稀H2SO4生成Zn(OH)2的离子方程式为_________。
(2)常温下,Zn(OH)2饱和溶液中c(Zn2+)=3×10—6mol/L,若溶液A中加入稀H2SO4过量,会溶解产生的Zn(OH)2,Zn(OH)2开始溶解的pH为_________,为防止Zn(OH)2溶解,可将稀H2SO4改为_________。(lg2=0.3)
(3)“部分氧化”阶段,NaClO3被还原为Cl—,还原剂与氧化剂反应的物质的量之比是_________。
(4)①由溶液B制得Fe3O4胶体粒子的过程中通入N2的原因是_________。
②Fe3O4胶体粒子的直径的范围是_________。
③确定滤液B中含有Fe2+的试剂是_________。
(5)试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因_________。
-
利用废旧锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO的一种制备流程图如下:
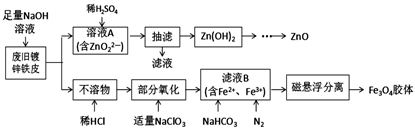
已知:Ksp[Zn(OH)2]= 1.2×10—17;Zn(OH)2既能溶于强酸,又能溶于强碱.还能溶于氨水,生成[Zn(NH3)4]2+.
(1)溶液A中加稀H2SO4生成Zn(OH)2的离子方程式为_________。
(2)常温下,Zn(OH)2饱和溶液中c(Zn2+)=3×10—6mol/L,若溶液A中加入稀H2SO4过量,会溶解产生的Zn(OH)2,Zn(OH)2开始溶解的pH为_________,为防止Zn(OH)2溶解,可将稀H2SO4改为_________。(lg2=0.3)
(3)“部分氧化”阶段,NaClO3被还原为Cl—,还原剂与氧化剂反应的物质的量之比是_________。
(4)①由溶液B制得Fe3O4胶体粒子的过程中通入N2的原因是_________。
②Fe3O4胶体粒子的直径的范围是_________。
③确定滤液B中含有Fe2+的试剂是_________。
(5)试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因_________。
-
利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下:
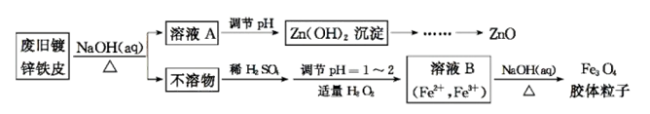
已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有 。(填字母序号)
A.去除油污  B.溶解镀锌层 C.去除铁锈 D.钝化
B.溶解镀锌层 C.去除铁锈 D.钝化
(2)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,其原因是 。
(3)? (填“能”或“不能”)。
(4)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.010 00 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取 g K2Cr2O7(保留4位有效数字,已知M(K2Cr2O7)=294.0 g·mol-1)。配制该标准溶液时,下列仪器中不必要用到的有 (用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(5)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将 (填“偏大”“偏小”或“不变”)。
-
利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下:

已知:Zn及其化合物的性质与Al及其化合物的性质相似,请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有________。
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是________。
(3)由溶液B制取Fe3O4胶体粒子的过程中,须持续通入N2,其原因是
_______________________________________________________________
(4)Fe3O4胶体粒子能否用减压过滤法实现固液分离?__________(填“能”或“不能”),理由是________________________________。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.010 00 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取________ g K2Cr2O7(保留4位有效数字,已知MK2Cr2O7=294.0 g·mol-1)。配制该标准溶液时,下列仪器中不必要用到的有________(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒
⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6) 滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将________(填“偏大”、“偏小”或“不变”)。
-
利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下:
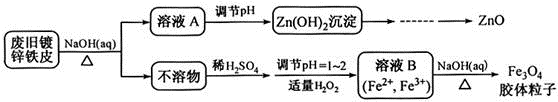
已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有_________。
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是____。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通N2,其原因是____________________。
(4)Fe3O4胶体粒子能否用减压过滤法实现固液分离?___(填“能”或“不能”),理由是_____。
(5)用重铬酸钾法(一种氧化还原滴定法)可测得产物Fe3O4中二价铁含量。若需配制浓度为0.01000 mol/L的K2Cr2O7的标准溶液250 mL,应准确称取______g K2Cr2O7 (保留4位有效数字,已知M(K2Cr2O7)= 294.0 g/mol。配制该标准溶液时,下列仪器不必要用到的有____________(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将_________(填“偏大”、“偏小”或“不变”,下同),到达滴定终点时俯视液面读数,则测定结果将___________。
-
利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下:
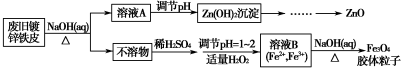
已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有________。
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是______________________________________________________________。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,其原因是_________________________________________________________。
(4)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.010 00 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取________g K2Cr2O7(保留4位有效数字,已知MK2Cr2O7=294.0 g·mol-1)。配制该标准溶液时,下列仪器中不必要用到的有________(用编号表示)。
①电子天平;②烧杯;③量筒;④玻璃棒;⑤容量瓶;⑥胶头滴管;⑦移液管
(5)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将________(填“偏大”“偏小”或“不变”)。
-
利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程如下:
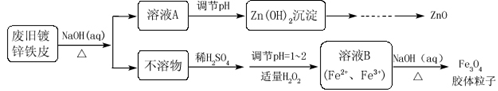
已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮可以去除油污,还可以____________________。
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是_____→洗涤→_____。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,其原因是________________。
(4)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。请写出酸性条件下K2Cr2O7与Fe2+反应的离子方程式________(K2Cr2O7被还原为Cr3+)。
(5)若需配制浓度为0.01000 mol·L-1的K2Cr2O7标准溶液250mL,应准确称取K2Cr2O7________g(保留四位有效数字,已知M(K2Cr2O7)=294.0 g·mol-1)。配制该标准溶液时,下列仪器一定不要用到的有________(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤250 mL容量瓶 ⑥胶头滴管 ⑦托盘天平
(6)若配制K2Cr2O7标准溶液时,俯视刻度线,则测定结果_______(填“偏大”、“偏小”或“不变”,下同);滴定操作中,若滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则滴定结果将________。
-
利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程如下:

已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有 。
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是 。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,其原因是 。
(4)Fe3O4胶体粒子能否用减压过滤法实现固液分离 (填“能”或“不能”),理由是 。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.01000mol·L-1的K2Cr2O7标准溶液250mL,应准确称取K2Cr2O7 g(保留4位有效数字,已知M(K2Cr2O7)=294.0g·mol-1)。配制该标准溶液时,下列仪器不必要用到的有 。(用编号表示)
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则滴定结果将 (填“偏大”、“偏小”或“不变”)。
-
利用废旧锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO.制备流程图如下:

已知:Zn及化合物的性质与Al及化合物的性质相似.请回答下列问题:
(1)用NaOH溶液处理废旧锌铁皮的作用有______.
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是______.
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,原因是______.
(4)Fe3O4胶体粒子能否用减压过滤发实现固液分离?______(填“能”或“不能”),理由是______.
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量.若需配制浓度为0.01000mol•L-1的K2Cr2O7标准溶液250mL,应准确称取______g K2Cr2O7(保留4位有效数字,已知M(K2Cr2O7)=294.0g•mol-1).
配制该标准溶液时,下列仪器中不必要用到的有______.(用编号表示).
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将______(填“偏大”、“偏小”或“不变”).
-
利用废旧锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下:

已知:Zn及化合物的性质与Al及化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧锌铁皮的作用有________。
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是________。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,原因是________。
(4)Fe3O4胶体粒子能否用减压过滤发实现固液分离?________(填“能”或“不能”),理由是________。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.01000 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取________g K2Cr2O7(保留4位有效数字,已知M(K2Cr2O7)=294.0 g·mol-1)。
配制该标准溶液时,下列仪器中不必要用到的有________。(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将________(填“偏大”、“偏小”或“不变”)。









