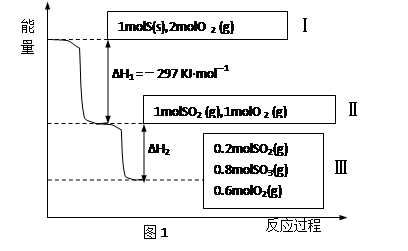-
在773 K,体积为V L的恒温恒容的容器中,硫和氧气可以发生如下转化,其反应过程和能量的关系如图1所示。其中状态III为平衡状态。
已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ/mol。
2SO3(g) ΔH=-196.6 kJ/mol。
请回答下列问题:
(1)写出表示硫的燃烧热的热化学方程式: 。
(2)状态II到状态III放出的热量为 。
(3)在另一个温度和容积相同的容器中,1 mol SO2和2 mol O2充分反应,放出的热量比∣ΔH2∣ (填“大”、“小”或“相等”)。
(4)恒容条件下,对状态III采取下列措施,能使n(SO3)/n(SO2)增大的有 。
A.降低温度
B.充入He气
C.再充入1 mol SO2(g)和1 mol O2(g) D.使用催化剂
(5)某SO2(g)和O2 (g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t2时引起平衡移动的条件可能是 。
(6)图2中表示平衡混合物中SO3的含量最高的一段时间是 。
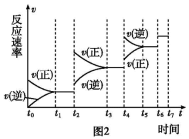
A. t1~t2 B. t3~t4 C. t5~t6 D. t6~t7
-
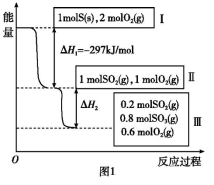
在一个温度和体积不变的容器中,硫可以发生如下转化,其反应过程和能量关系如图1所示。(SO2(g)+1/2O2(g) SO3(g) ΔH=-98.45kJ·mol-1)
SO3(g) ΔH=-98.45kJ·mol-1)
(1)硫燃烧的热化学方程式为:__________________。
(2)恒容条件下,下列措施中能使n(SO2)/ n(SO3)比图1所示情况减小的有____________。
A.降低温度 B.充入He C.再充入1 mol SO2(g)和1 mol O2(g) D.使用催化剂
(3)恒温恒容时,图1中II到III反应放出的热量比1 mol SO2和2 mol O2充分反应放出的热量__________
(填 “多”、“少”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t2时引起平衡移动的条件可能是_____________;图中表示平衡混合物中SO3的含量最高的一段时间是_____________。(如t1~t2、t3~t4、t5~t6 、t6~t7等)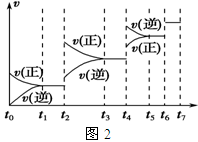
-
(已知:2 SO2 (g)+O2(g)  2SO3(g) △H = -196.6 KJ·mol- 1), 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示。以下叙述错误的是( )
2SO3(g) △H = -196.6 KJ·mol- 1), 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示。以下叙述错误的是( )
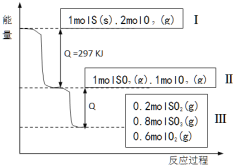
A.表示硫的燃烧热的热化学方程式:S(s)+O2(g)=SO2(g) ΔH=-297 KJ·mol-1
B.由Ⅱ到Ⅲ的过程放出的热量为98.3KJ
C.恒温恒容时,1molSO2和2molO 2 充分反应,放出热量的数值大于78.64KJ
D.将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为 2mol
-
恒温、容积为1 L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示[已知:2SO2(g) + O2(g)  2SO3(g) △H = - 196.6 kJ/mol ]。
2SO3(g) △H = - 196.6 kJ/mol ]。
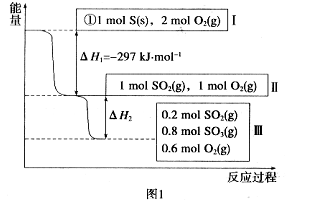
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:____________________。
(2)△H2 = ____________ kJ/mol。
(3)在相同条件下,充入1 mol SO3和0.5 mol O2,则达到平衡时SO3的转化率为_________;此时该反应_______(填“放出”或“吸收”)________ kJ的能量。
-
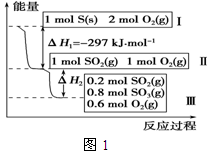
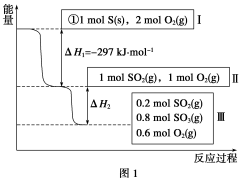
(本题共14分)恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。请回答下列问题:
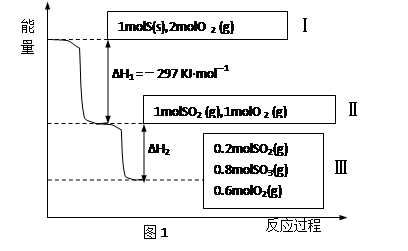
(1)写出能表示硫的燃烧热的热化学方程式:________。
(2)已知在450℃并有催化剂存在下:2 SO2 (g)+O2(g)  2SO3(g) △H = -196.6 KJ·mol- 1,
2SO3(g) △H = -196.6 KJ·mol- 1,
①该热化学反应方程式的意义是。
②图1中的ΔH2 =________KJ·mol-1
③恒温恒容时,1molSO2和2molO 2 充分反应,放出热量的数值比∣ΔH2 ∣________(填“大”“小”或“相等”)
④)恒容条件下,下列措施中能使n(SO3)/ n(SO2 )增大的有________。
a.升高温度 b.充入He气
c.再充入1molSO2 (g)和1molO 2 (g) d.使用催化剂
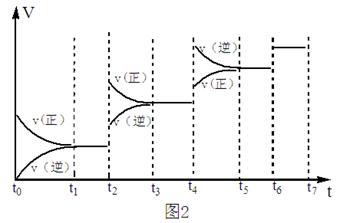
(3) 某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率 与时间t的关系如图2所示,若不改变SO2 (g)和O 2 (g)的量,则:
与时间t的关系如图2所示,若不改变SO2 (g)和O 2 (g)的量,则:
①图中t4时引起平衡移动的条件可能是________;
②图中表示平衡混合物中SO3的含量最高的一段时间是____________。
A、t1~t2 B、t3~t4 C、t5~t6 D、t7~t8
-
恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示
[已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1]:
2SO3(g) ΔH=-196.6 kJ·mol-1]:
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:____________________。
(2)ΔH2=_____________________。
(3)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比|ΔH2|________(填“大”、“小”或“相等”)。
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为__________,若溶液中发生了氧化还原反应,则该过程的离子方程式为______________________。
(5)向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2 和1 mol O2;(乙) 1 mol SO2 和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是( )
A.容器内压强p:p甲=p丙>2p乙
B.SO3的质量m:m甲=m丙>2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙>k乙
D.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
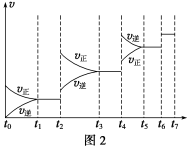
(6)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是__________;图中表示平衡混合物中SO3的含量最高的一段时间是____________。
(7)各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 | t3~t4 | t5~t6 | t6~t7 |
| K1 | K2 | K3 | K4 |
K1、K2、K3、K4之间的关系为__________________。
-
(已知:2SO2(g)+O2(g) 2SO3(g)△H=-196.6KJ·mol-1),恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示。以下叙述错误的是( )
2SO3(g)△H=-196.6KJ·mol-1),恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示。以下叙述错误的是( )
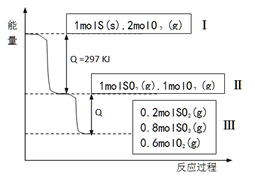
A.表示硫的燃烧热的热化学方程式:S(s)+O2(g)==SO2(g)ΔH=-297KJ·mol-1
B.由Ⅱ到Ⅲ的过程放出的热量为98.3KJ
C.恒温恒容时,1molSO2和2molO2充分反应,放出热量的数值大于78.64KJ
D.将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为2mol
-
已知 和
和 可以相互转化
可以相互转化
 。现将一定量
。现将一定量 和
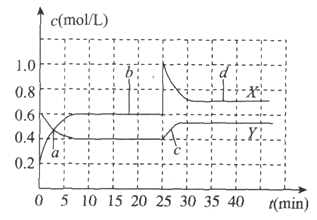
和 的混合气体通入体积为1L的恒温恒容的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是
的混合气体通入体积为1L的恒温恒容的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是

A. 反应进行至25min时,曲线发生变化的原因是加入0.4mol
B. a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d
C. 图中共有两条曲线X和Y,其中曲线X表示 浓度随时间的变化
浓度随时间的变化
D. 若要达到与d相同的状态,在25min时还可以采取的措施是适当缩小容器体积
-
已知 和
和 可以相互转化
可以相互转化
 。现将一定量
。现将一定量 和
和 的混合气体通入体积为1L的恒温恒容的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是
的混合气体通入体积为1L的恒温恒容的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是
A. 反应进行至25min时,曲线发生变化的原因是加入0.4mol
B. a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d
C. 图中共有两条曲线X和Y,其中曲线X表示 浓度随时间的变化
浓度随时间的变化
D. 若要达到与d相同的状态,在25min时还可以采取的措施是适当缩小容器体积
-
在一个温度和体积不变的容器中,硫可以发生如下变化,其反应过程和能量关系如图1所示。(SO2(g)+1/2O2(g) SO3(g) △H=-98.45kJ·mol-1)
SO3(g) △H=-98.45kJ·mol-1)
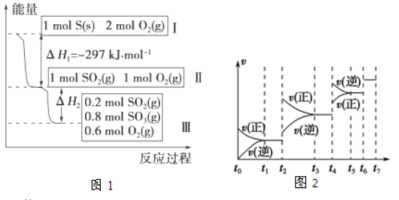
(1)硫燃烧的热化学方程式为 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有 。
A.降低温度 B.充入He C.再充入1mol SO2(g)和1mol O2(g) D.使用催化剂
(3)恒温恒容时,图1中II到III反应放出的热量比1mol SO2和2mol O2充分反应放出的热量 (填
“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t2时引起平衡移动的条件可能是 ;图中表示平衡混合物中SO3的含量最高的一段时间是 。(如t1~t2、t3~t4、t5~t6、t6~t7等)

2SO3(g) ΔH=-196.6 kJ/mol。