-
某同学用含少量硫酸铁的硫酸钠固体,制取芒硝(Na2SO4·10H2O),操作流程图如下所示,请回答下列问题:
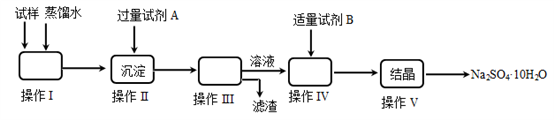
(1)操作I的名称是________;操作III所需的玻璃仪器有________________________。
(2)试剂A为__________;试剂B为__________,加入试剂B的目的是__________________,实验中加入适量试剂B的实验方案为___________________。
(3)操作V的步骤依次是________(用编号填入)
a.过滤 b.冷却 c.蒸发浓缩 d.蒸发至接近蒸干
-
(15分)四川省钙芒硝矿(主要成分CaSO4•Na2SO4)资源丰富。钙芒硝矿可生产具有广泛用途的芒硝(Na2SO4•10H2O)和元明粉(Na2SO4),其简要生产流程如下图所示。

请回答下列问题:
(1)浸取Na2SO4时,加入少量Na2CO3可使钙芒硝矿中的部分CaSO4转化为CaCO3,破坏钙芒硝矿结构,从而促进Na2SO4的浸取。CaSO4能转化为CaCO3的原因是_________________________。
(2)向Na2SO4的浸取液中加入适量烧碱和纯碱,Ca2+和Mg2+分别生成①________、②_________(填化学式)被过滤除去。
(3)根据下图溶解度曲线,可采用冷却结晶法从含少量NaCl的Na2SO4饱和溶液中制得芒硝的原因是___________________________________________________________________________。

(4)已知:25℃、101kPa时,
2C(s) + O2(g) == 2CO(g) ΔH1 = —222kJ/mol
4Na2SO3(s) == 3Na2SO4(s) + Na2S(s) ΔH2 = —122kJ/mol
2Na2SO3(s) + O2(g) == 2Na2SO4(s) ΔH 3= —572kJ/mol
元明粉经碳还原制备Na2S的热化学方程式是__________________________________________________。
(5)如图,用惰性电极电解Na2SO4溶液,阳极区制得H2SO4溶液,阴极区制得NaOH溶液。其电解总反应的化学方程式是:______________________________。

(6)芒硝加热至70℃时,得到Na2SO4的饱和溶液(结晶水作溶剂,忽略加热过程中水的蒸发)和无水Na2SO4。若3220kg芒硝加热至70℃时,可析出元明粉(Na2SO4)的质量是________kg。
-
铵明矾(NH4Al(SO4)2•12H2O)是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备。用芒硝(Na2SO4•10H2O)制备纯碱和铵明矾的生产工艺流程图如图1:
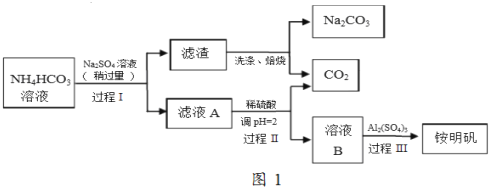
完成下列填空:
(1)铵明矾溶液呈_________性,它可用于净水,原因是_______________;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是__________________。
(2)写出过程Ⅰ的化学反应方程式_______________。
(3)若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是___________。
(4)已知铵明矾的溶解度随温度升高明显增大.加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、___________、过滤洗涤、干燥。
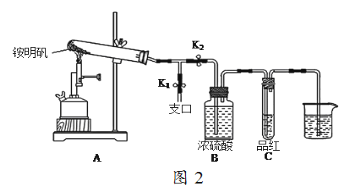
(5)某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份。
①夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是______________;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是___________(任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式_______________。
②该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=_____。
-
铵明矾【NH4Al(SO4)2•12H2O】是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备.用芒硝(Na2SO4•10H2O)制备纯碱和铵明矾的生产工艺流程图如图1:
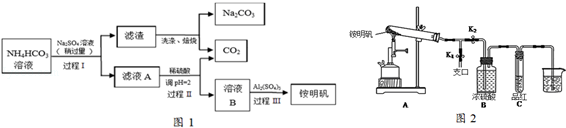
完成下列填空:
(1)铵明矾溶液呈 性,它可用于净水,原因是 ;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是 .
(2)写出过程Ⅰ的化学反应方程式 .
(3)若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是 .
(4)已知铵明矾的溶解度随温度升高明显增大.加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、 、过滤洗涤、干燥.
(5)某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份.
①夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧.实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是 ;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是 (任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式 .
②该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)= .
-
铵明矾【NH4Al(SO4)2·12H2O】是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备。用芒硝(Na2SO4·10H2O)制备纯碱和铵明矾的生产工艺流程图如图1:
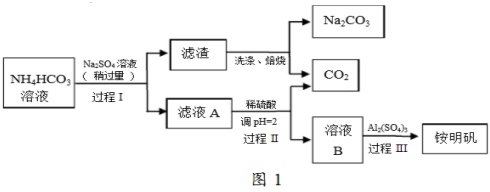
完成下列填空:
31.铵明矾溶液呈 性,它可用于净水,原因是 ;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是 。
32.写出过程Ⅰ的化学反应方程式 。
33.若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是 。
34.已知铵明矾的溶解度随温度升高明显增大。加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、 、过滤洗涤、干燥。
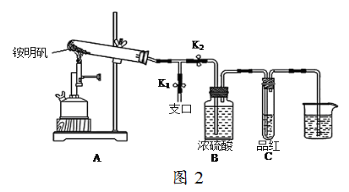
35.某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份。
(1)夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是 ;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是 (任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式 。
(2)该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)= 。
-
某溶液中含有较多的Na2SO4和少量的 Fe2(SO4)3。若用该溶液制取芒硝(Na2SO4·10H2O),可供选择的操作有:①加适量H2SO4溶液;②加金属钠;③结晶;④加过量NaOH;⑤加强热脱结晶水;⑥过滤。正确的操作步骤是
A.②⑥③ B.④⑥①③ C.④⑥③⑤ D.②⑥①③⑤
-
SPC(2Na2CO3•3H2O2)具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO4•10H2O)、H2O2等为原料制备SPC的工艺流程如下:

回答下列问题:
(1)步骤I产生的滤渣为__________________(填名称)。
(2)步骤II中发生反应的离子方程式为_________________。其中生成的__________(填化学式)可以循环使用。
(3)步骤V中,合成时需选择温度为15℃,其原因是_____________________。
(4)抽滤后用乙醇洗涤的作用是_______________________________________。
(5)SPC的保存方法是______________________________。
(6)过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600 g样品,置于250 mL锥形瓶中,并用100 mL 0.5 mol•L-1硫酸溶解完全,立即用0.02000mol•L-1KMnO4标准溶液滴定,滴定至终点时溶液颜色为_____,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56 mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24 mL。该样品的活性氧含量为______%。
-
SPC(2Na2CO3∙3H2O2)具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO4∙10H2O)、H2O2等为原料制备SPC的工艺流程如下:

回答下列问题:
⑴步骤Ⅰ中________ 填“有”或“没有”
填“有”或“没有” 发生氧化还原反应。
发生氧化还原反应。
⑵步骤Ⅱ中会生成一种可以循环使用的物质,该物质的化学式为________。
⑶步骤Ⅲ中需要加热,发生反应的化学方程式为_________________________________。
⑷步骤Ⅴ中,合成时需选择温度为15℃,其目的是___________。
⑸SPC的保存方法是_____________________________。
⑹过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600g样品,置于250mL锥形瓶中,并用100mL 0.5 mol·L-1硫酸溶解完全,立即用0.02000mol·L-1 KMnO4标准溶液滴定,滴定至终点时溶液颜色为________,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24mL。该样品的活性氧含量为_______%。
-
SPC(2Na2CO3•3H2O2具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO4•10H2O)、H2O2等为原料制备SPC的工艺流程如下:
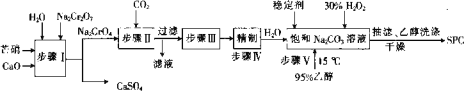
回答下列问题:
(1)步骤I中_____(填“有”或“没有”)发生氧化还原反应。
(2)步骤II中会生成一种可以循环使用的物质,该物质的化学式为_____。
(3)步骤Ⅲ中需要加热,发生反应的化学方程式为______。
(4)步骤Ⅳ中,合成时需选择温度为15℃,其目的是_____,从环境保护的角度看,诙流程中存在的缺点是_______。
(5)SPC的保存方法是________。
(6)过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600 g样品, 置于250 mL锥形瓶中,并用100 mL 0. 5 mol•L-1硫酸溶解完全,立即用0.02000mol•L-1KMnO4标准溶液滴定,滴定至终点时溶液颜色为_____,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56 mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24 mL。该样品的活性氧含量为______%。
-
过碳酸钠(2Na2CO3·3H2O2)广泛用于化工、造纸、纺织、食品等行业,一种以芒硝(Na2SO4·10H2O)、H2O2等为原料制备过碳酸钠的工艺流程如下:
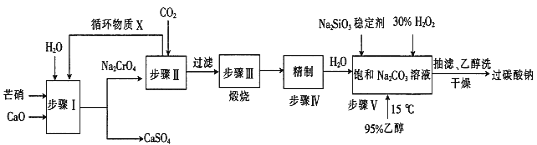
已知:2CrO42-+2H+ Cr2O72-+H2O,pH小于5时几乎均以Cr2O72-形式存在,pH大于8.5时几乎均以CrO42-形式存在。回答下列问题:
Cr2O72-+H2O,pH小于5时几乎均以Cr2O72-形式存在,pH大于8.5时几乎均以CrO42-形式存在。回答下列问题:
(1)由步骤I可知:Ksp(CaCrO4)_____Ksp(CaSO4)(填“>”或“<”)。
(2)流程中循环物质X的主要溶质为____________(填化学式)。
(3)步骤II后的溶液过滤得到一种酸式盐固体,其发生反应的离子方程式为________________。
(4)步骤III是为了制得纯碱,其化学方程式为 _________________________________。
(5)步骤V合成时,调节温度为15℃并加入95%乙醇的目的是____________________。
(6)测定产品活性氧的实验步骤如下:准确称取mg产品,用硫酸溶解后,用c mol· L-1的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液V mL。
①该滴定过程不需要外加指示剂的原因是_________________________________ 。
②滴定到终点时,溶液最终呈________(填“无色”或“浅红色”)。












