-
某同学对SO2和亚硫酸的性质进行了探究。回答下列问题:
I.探究SO2性质
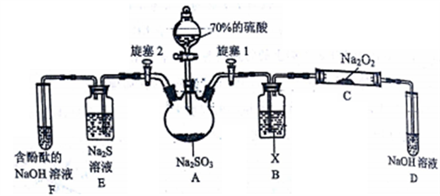
(1)关闭旋塞2,打开旋塞1,注入硫酸至浸没三颈烧瓶中固体,检验SO2与Na2O2 反应是否有氧气生成的方法是______________________________。
(2)装置B中试剂X是____________,实验结束后D溶液中的阴离子可能是_______________。
(3)设计实验检验C中固体产物的阴离子:___________________________ (简要描述操作步骤、实验现象、结论)。
(4)关闭旋塞1后,打开旋塞2,E用于验证SO2的____性,F中的现象是_______________。
II.探究H2SO3的酸性强于HC1O。
请你利用下面装置达成实验目的。
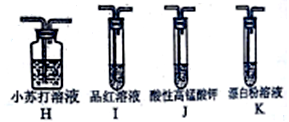
(5)装置的连接顺序为:
纯净SO2→__________(选填字母),K中反应的离子方程式是_________________________。
(6)可证明H2SO3的酸性强于HC1O的实验现象是_________________________。
-
SO2是一种有毒气体,但可用于酒精的防腐剂,可以抵抗微生物的侵袭。甲同学用Na2SO4制备SO2,并验证SO2的部分性质。设计了如下实验步骤及装置:
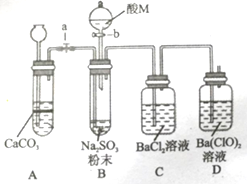

II.关闭活塞a再打开旋塞b,分次加入酸M。
III.待试管B中充分反应后,打开活塞a,从长颈漏斗加入适量盐酸。
[实验现象]
打开活塞a前,C中溶液有少量固体生成,长导管口有气泡。D中溶液有大量固体生成;当C中长导管口无气泡后,D中液面上气体逐渐变为浅黄绿色。
回答下列问题:
(1)盛放酸M的仪器名称是___________________。
(2)查阅资料:①常温常压下,在1L水中大约最多能溶40L SO2,②H2SO3是中强酸。与亚硫酸钠反应制SO2的酸A最好用_________(填标号)。
a.稀盐酸 b.pH=1的硫酸 c.2mol/L的硝酸 d.12mol/L的硫酸
(3)实验过程中,D中发生反应的离子方程式为_______、________________。
(4)实验步骤III的目的是__________________________________________________。
【问题探究】
(5)乙同学认为:
①甲同学的实验步骤设计不严谨,所以装置C中的少量固体可能是:亚硫酸钡、硫酸钡或亚硫酸钡和硫酸钡。为确定C中固体的成分,乙同学在不改变实验装置的条件下,只对实验步骤加以改进便能准确判断出装置C中的固体的成份。乙同学对实验步骤改进的具体操作是___________________________________。
②甲同学的实验装置有明显不足,你认为不足之处是_____________________________。
-
如图是某研究性学习小组设计的SO2与Na2O2反应的探究装置.

(1)实验开始时,打开旋塞K,通入N2排尽整套装置中的空气,关闭旋塞K。点燃酒精灯,A中反应的化学方程式是________。
(2)B装置的作用是________。
(3)反应过程中,观察到:A中出现黑色不溶物;C中固体由淡黄色逐渐至完全转化为白色;若将带火星木条伸入D试管口内,火星显得更明亮。
①停止加热后,再通入N2至整套装置冷却,其目的是________。
②取少量C中白色固体,溶于蒸馏水得无色溶液W 。若向W中滴加几滴酸性KMnO4溶液,振荡,紫色褪去;若向W中加入用盐酸酸化的BaCl2溶液,出现大量白色沉淀;则说明C中白色固体有________。
③D装置中发生反应的离子方程式是________。
④过滤出A装置中的黑色不溶物,洗涤后将其溶于浓硝酸,得到蓝色溶液并产生红棕色气体;向蓝色溶液中滴加BaCl2溶液,产生白色沉淀;则黑色物质可能是___________。
a.Cu b. CuO c.CuS d.Cu2S
-
某同学对教材中铜与浓硫酸的实验作了如下改进。实验装置如图所示(加热和夹持装置己略去)。
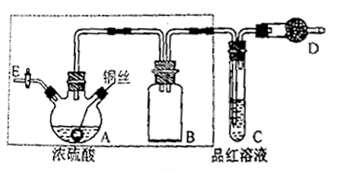
实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A,观察C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
(1)检査虚线框内装置气密性的方法是____________________。
(2)仪器A的名称是_________________,仪器B的作用是_________________,仪器D中所盛药品是_________________。
(3)装置A中发生反应的化学方程式为_________________。
(4)实验后,拆除装置前,为避免有害气体的泄漏,应当采取的操作是_______________。
(5)实验后仪器A中有白色固体产生,将仪器A中固液混合物缓慢转移至盛有少量水的烧杯中,可观察到的现象是_____________,用所得溶液做焰色反应实验时,观察到的火焰颜色为___________。不可直接向仪器A中加水的原因是_________________。
-
下列说法不正确的是( )。
A.利用分液漏斗进行分液操作时,先打开分液漏斗旋塞,使下层液体慢慢流出,待下层液体完全流出后,关闭旋塞,上层液体再从上面倒出
B.用玻璃棒蘸取新制氯水,滴在pH 试纸上,然后与比色卡对照,可测定新制氯水的pH
C.在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、环形玻璃搅拌棒进行搅拌、酸和碱正好反应、取2~3 次的实验平均值,以达到良好的实验效果
D.固体药品取用:块状固体用镊子夹取,粉末状的用药匙或纸槽转移
-
下列说法不正确的是
A.利用分液漏斗进行分液操作时,先打开分液漏斗旋塞,使下层液体慢慢流出,待下层液体完全流出后,关闭旋塞,上层液体再从上面倒出
B.固体药品取用:块状固体用镊子夹取,粉末状的用药匙或纸槽转移
C.在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、环形玻璃搅拌棒进行搅拌、酸和过量的碱充分反应、取2—3 次的实验平均值,以达到良好的实验效果
D.用标准浓度的盐酸滴定未知浓度NaOH溶液时,酸式滴定管未用同浓度盐酸润洗,将导致测定结果偏低
-
下列说法不正确的是( )
A.利用分液漏斗进行分液操作时,先打开分液漏斗旋塞,使下层液体慢慢流出,待下层液体完全流出后,关闭旋塞,再将上层液体从上口倒出
B.用镊子夹取金属钠固体,切割取用后剩余的钠放回原试剂瓶中
C.用标准浓度的盐酸滴定未知浓度NaOH溶液时,酸式滴定管用蒸馏水洗净后未用同浓度盐酸润洗,将导致测定结果偏低
D.溶液配制、中和滴定实验中,容量瓶、锥形瓶用蒸馏水洗净后即可使用;而滴定管、移液管用蒸馏水洗净后,须再用待盛液润洗2~3次后方可使用
-
下列说法不正确的是
A.利用分液漏斗进行分液操作时,先打开分液漏斗旋塞,使下层液体慢慢流出,待下层液体完全流出后,关闭旋塞,再将上层液体从上口倒出
B.用镊子夹取金属钠固体,切割取用后剩余的钠放回原试剂瓶中
C.用标准浓度的盐酸滴定未知浓度 NaOH溶液时,酸式滴定管用蒸馏水洗净后未用同浓度盐酸润洗,将导致测定结果偏低
D.溶液配制、中和滴定实验中,容量瓶、锥形瓶用蒸馏水洗净后即可使用;而滴定管、移液管用蒸馏水洗净后,须再用待装液润洗2~3 次后方可使用
-
下列说法正确的是
A.用分液漏斗分液时,先打开旋塞,待下层液体完全分出后,关闭旋塞,再从上口倒出上层液体
B.准确量取25.00 mL的液体可选用移液管、量筒或滴定管等量具
C.在中和热测定实验中,盐酸和NaOH溶液的总质量m g,反应前后体系温度变化,反应液的比热容为c J·g-1·℃-1,则生成1 mol水放出的热量为kJ
D.在抽滤装置中洗涤晶体时,为减少晶体溶解损失,应使洗涤剂快速通过滤纸
-
I.某学习小组设计如下图装置制取SO2,研究其性质,并进一步探究不同浓度硫酸的氧化性
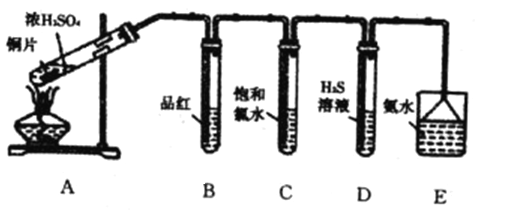
请回答下列问题:
(1)B、C、D分别用于检验SO2的性质,写出C中反应的离子方程式________________。
(2)实验中观察到D中有浑浊出现,有同学提出此现象不能证明SO2具有氧化性。
请简述理由:______________________________________________。
(3)E装置的作用为_____________________________。
Ⅱ.某学习小组设计并完成如下实验:称取一定量的还原铁粉放入一定体积的浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。经检验,气体Y中含有SO2、H2。
(4)溶液X中一定大量含有的金属阳离子是___________,简述如何检验溶液X中该离子______________________。
(5)为了测定气体Y中SO2的含量,将2.24L(标准状况)气体Y通入到200.00mL 0.2000mol/L酸性高锰酸钾溶液中,充分反应后,取出20.00mL溶液转入锥形瓶中进行滴定,消耗浓度为0.0500mol/L的KHC2O4标准液20.00mL。
①室温下,0.05mol/L KHC2O4溶液中,c(C2O42-)>c(H2C2O4)。滴定操作时,标准液应装在
___________(填仪器名称)中;滴定终点的现象为______________________________。
②气体Y中SO2的物质的量分数为____________________。






