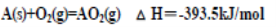-
CH4、NH3、H2O、H2S、NH4NO3和ZnS是中学化学常见的六种化合物。回答下列问题:
(1)基态S原子有__________种不同能量的电子,与Zn同属ds区且同周期的元素基态原子核外电子排布式为____________________。
(2)H2O和H2S中,沸点较高的是__________,原因是___________________________________。
(3)CH4、NH3和H2O3种氢化物中,键角由大到小的顺序为_______________,其中NH3的VESEPR模型名称为____________。
(4)NO3-离子的几何构型为__________,NO3-离子的电子体有_____________(任写一种)。
(5)ZnS晶体结构有多种,其中一种晶体的晶胞结构如图所示,晶体中与S2-等距离且最近的S2-有_____个。已知该晶体的晶胞参数为anm,其密度为 ρg·cm-3,则阿伏加德罗常数的数值为____________________________(用含字母a、ρ的表达式表示,列出计算式即可)。
-
碳、硫、氧、氮是中学常见元素,下列说法正确的是( )
A.CO2、SO2、NH 3都是直线形分子
B.CO2、NH3、H2S 的键角依次减小
C.H2O2、N2H4分子的中心原子都是sp3杂化
D.C、N、F元素的电负性依次减小
-
(16分)C、N、O、S、Mg、Fe等是中学化学中的常见元素。按要求回答下列问题:
(1)N元素在元素周期表中的位置是______________。
(2) H2S的沸点比H2O的沸点低的主要原因是__________________。
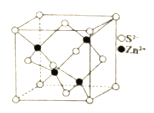
(3)已知:2 SO2(g) +O2(g)- 2 SO3(g) △H=-196.6 kJ·mol-l
2 SO3(g) △H=-196.6 kJ·mol-l
2 NO(g) +O2(g)  2 NO2(g) AH=-113.0 kJ·mol-l
2 NO2(g) AH=-113.0 kJ·mol-l
则反应NO2(g) +SO2(g)  SO3(g)+NO(g)的△H= kJ·mol-l
SO3(g)+NO(g)的△H= kJ·mol-l
(4)CO在催化剂作用下可以与H2反应生成甲醇:CO(g)+2 H2(g)  CH3OH(g),在2L密闭容器中充人lmol CO与2 mol H2,CO的平衡转化率与温度、压强的关系如右图所示。则M、N、Q三点的平衡常数KM、KN、Ko的大小关系为 ;Pl P2(填“>、<或=”);平衡常数KM=__________。
CH3OH(g),在2L密闭容器中充人lmol CO与2 mol H2,CO的平衡转化率与温度、压强的关系如右图所示。则M、N、Q三点的平衡常数KM、KN、Ko的大小关系为 ;Pl P2(填“>、<或=”);平衡常数KM=__________。

(5) Mg和Fe组成的合金是目前已发现的储氢密度最(高的储氢材料之一,其晶胞结构如图甲(白球代表Mg,黑球代表Fe)。则该合金的化学式为 。若该合金用M表示,某种储氢镍电池(MH - Ni电池)的结构如图乙所示。其电池反应为:MH+NiOOH Ni( OH)2 +M。下列有关说法不正确的是________。
Ni( OH)2 +M。下列有关说法不正确的是________。

A.放电时正极反应为:NiOOH+H2O+e-= Ni(OH)2 +OH-
B.放电时电子由b极到a极
C.充电时负极反应为:MH+ OH- - e-= H20+M
D.M的储氢密度越大,电池的比能量越高
-
(14分)已知A、B、C、D、E为中学化学常见的五种物质,均含元素R,R在A、B、C、D、E中所呈化合价依次递增,其中只有B为单质。常温下,A、B、C、D为气体,且D+H2O→C+E。
请回答下列问题:
⑴元素R在元素周期表中的位置为_____________________; B分子的电子式为__________。
⑵已知气体D与NaOH溶液1:1恰好完全反应,生成R的两种含氧酸盐,所得溶液中各离子浓度大小关系________。
⑶将22.4L某R的氧化物与足量的灼热铜粉完全反应后,气体体积变为11.2L(体积均在相同条件下测定),则该氧化物的化学式可能为________。(填序号)
①、RO2 ②、R2O3 ③、RO ④、R2O
⑷科学家制备的另一种化合物,与A的组成元素相同,具有很高的热值,可用作火箭和燃料电池的燃料。该化合物可由次氯酸钠溶液和A反应得到,写出该反应的化学方程式________。
⑸M为E的钠盐,一定条件下可发生如下反应:
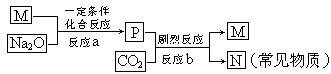
①设计实验方案,鉴定常见物质N。
②此外,科学家还制备了另一种钠盐X,其与P的组成元素完全相同,X中的阴离子与P中的阴离子表观形式相同(元素种类和原子个数均相同),但X中阴离子的结构中含有一个过氧键:-O-O- ,电导实验表明,同条件下其电导能力与NaCl相同,钠盐X的阴离子与水反应生成过氧化氢的离子方程式为________。
| 25℃平衡体系(苯、水、HA) | 平衡常数 | 焓变 | 起始总浓度 |
| 在水中,HA H++A- H++A- | K1 | △H1 | 3.0×10-3 mol·L-1 |
| 在苯中,2HA (HA)2 (HA)2 | K2 | △H2 | 4.0×10-3 mol·L-1 |
-
如图是中学化学中常见的有机化合物转化关系。其中A可以提供生命活动所需的能量;E是B的同系物,0.1molE完全燃烧生成4.4g CO2和3.6g H2O。

回答下列问题:
(1)E的分子式为__________,D与E反应生成F的反应类型_______;
(2)下列说法正确的是_______;
A. “煤→混合气”属于煤的干馏 B.A与C均能发生银镜反应
C.D、F均能与氢氧化钠溶液反应 D.D、E、F都能与水任意比互溶
(3)写出“A→B”的化学方程式_______________。
-
CO、BF3、CCl4、CH4都是非极性分子,而NH3、H2S、H2O都是极性分子。由此推出ABn型分子是非极性分子的经验规律正确的是 ( )
A.所有原子在同一平面内
B.分子中不含氢原子
C.A的原子量小于B
D.在ABn分子中A原子化合价的绝对值等于其最外层电子数
-
中学化学很多“规律”都有其适用范围,下列根据有关规律推出的结论合理的是( )
A.CH4的沸点比SiH4低,同理,H2O的沸点也比H2S低
B.氯化铁溶液中加稀盐酸可抑制Fe3+的水解,同理,硫酸铁溶液中也加稀盐酸来抑制Fe3+的水解
C.CH4中混有SO2可通过酸性高锰酸钾溶液除去,同理,CH4中混有C2H4也可以通过酸性高锰酸钾溶液除去
D.CO2能使足量的澄清石灰水出现浑浊,同理,SO2能使足量的澄清石灰水出现浑浊
-
已知CO2、BF3、CH4、SO3都是非极性分子,NH3、H2S、H2O、SO2都是极性分子,由此可推知ABn型分子是非极性分子的经验规律是( )
A.分子中所有原子在同一平面内
B.分子中不含氢原子
C.在ABn分子中,A元素为最高正价
D.在ABn型分子中,A原子最外层电子都已成键
-
根据杂化理论回答下列问题:
| 分子 | CH4 | H2O | NH3 | CO2 | C2H4 |
| 键角 | 109.5° | 104.5° | 107.3° | 180° | 120° |
(1)上表中各种物质中心原子是否以杂化轨道成键?以何种类型杂化轨道成键?
(2)NH3和H2O的键角为什么比CH4小?CO2键角为何是180°?乙烯的键角又为何为120°?
-
(8分)某同学从资料上查到以下反应
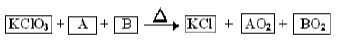
A、B为中学常见单质,AO2、BO2是能使澄清石灰水变浑浊的气体。回答下列问题:
(1)元素A、B可形成化合物AB2,则A元素的原子结构示意图为 ,AB2中的化学键是
(2)若反应中A和B的质量比为3:4,则n(KClO3):n(AO2)=
(3)已知: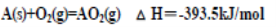

写出AB2(l)在O2中完全燃烧的热化学方程式为