-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
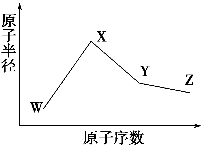
(1)X位于元素周期表中第________周期第________族;W的基态原子核外有________个未成对电子。
(2)Z的气态氢化物和溴化氢相比,较稳定的是________________(写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是____________________________________________________。
-
(15分)W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为14,中子数为7;X的离子与N 具有相同的质子、电子数目:W与Y的氧化物均能导致酸雨的形成;Z的非会属性在同周期主族元素中最强。
具有相同的质子、电子数目:W与Y的氧化物均能导致酸雨的形成;Z的非会属性在同周期主族元素中最强。
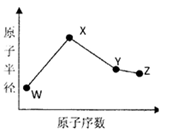
(1)Y在周期表中的位置是 。
(2)用电子式表示化合物X3W的结构 。
(3)X3W遇水可释放出使酚酞溶液变红的气体A,该反应的化学方程式是 。
(4)同温同压下,将a L W的简单氢化物和b LZ的氢化物通入水中,若所得溶液的pH=7则a b(填“>”或“<”或“=”)。
(5)用惰性电极电解化合物XZ溶液从阴极释放出气休B,该反应的离子方程式是 。
(6)已知W的单质与气体B在一定条件下可形成气体A,即:
 △H=—92.4kJ·mo1-1
△H=—92.4kJ·mo1-1
在某温度时,一个容积固定的密闭容器中,发生上述反应。在不同时间测定的容器内各物质的浓度如下表:
| 时间 | 浓度(mo1/L) |
| c(W2) | c(B) | c(A) |
| 第0 min | 4.0 | 9.0 | 0 |
| 第10 min | 3.8 | 8.4 | 0.4 |
| 第20 min | 3.4 | 7.2 | 1.2 |
| 第30 min | 3.4 | 7.2 | 1.2 |
| 第40 min | 3.6 | 7.8 | 0.8 |
| | | |
①0min~10min,W2的平均反应速率 。
②反应在第l0min改变了反应条件,改变的条件可能是 。
a.更新了催化剂 b.升高温度 c.增大压强 d.增加B的浓度
③若反应从第30min末又发生了一次条件改变,改变的反应条件可能是 。
a.更新了催化剂 b.升高温度 c.增大压强 d.减小A的浓度
-
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的元素(不考虑稀有气体的原子半径);Y的单质呈黄色,常见于火山口附近。下列说法正确的是
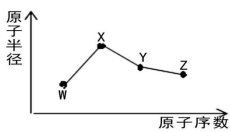
A. 氧化物的水化物酸性:Y<Z
B. 简单离子半径:W<X<Z
C. W的简单气态氢化物的沸点高于同族其它元素的简单气态氢化物
D. 将标况下等体积的Z单质与Y的低价氧化物同时通入品红溶液中,品红溶液迅速褪色
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知 W 的一种核素的质量数为 18,中子数为 10;X 和 Ne 的核外电子数相差 1;在Z所在的周期中,Z 元素的原子得电子能力最强;四种元素的最外层电子数之和为18。请回答下列问题:
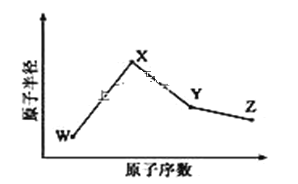
(1)X 元素位于元素周期表中位置为______。
(2)X 的单质和Y的单质相比,熔点较高的是_____(写化学式)。 Z 所在族的简单氢化物中,沸点最高的是____(写化学式),原因为______。
(3)W、X、Z 三种元素形成的化合物中化学键类型为_____;X2W2的电子式为____。
(4)Y 与 Z 形成的化合物在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为______。
(5)Z 的氧化物很多,其中一种黄绿色气体M,其氧含量为 47.41%,可用于水处理,M在液态和浓缩气态时具有爆炸性。M的化学式为______。M可与 NaOH溶液反应生成两种稳定的盐,它们的物质的量之比为1︰5,该反应的化学方程式为________。
(6)在25°C、101kPa 下,已知 Y 的简单气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移 1mol 电子放热 190kJ,该反应的热化学方程式为_____。
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知 W 的一种核素的质量数为 18,中子数为 10;X 和 Ne 的核外电子数相差 1;在Z所在的周期中,Z 元素的原子得电子能力最强;四种元素的最外层电子数之和为18。请回答下列问题:
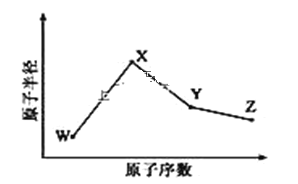
(1)X 元素位于元素周期表中位置为______。
(2)X 的单质和Y的单质相比,熔点较高的是_____(写化学式)。 Z 所在族的简单氢化物中,沸点最高的是____(写化学式),原因为______。
(3)W、X、Z 三种元素形成的化合物中化学键类型为_____;X2W2的电子式为____。
(4)Y 与 Z 形成的化合物在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为______。
(5)Z 的氧化物很多,其中一种黄绿色气体M,其氧含量为 47.41%,可用于水处理,M在液态和浓缩气态时具有爆炸性。M的化学式为______。M可与 NaOH溶液反应生成两种稳定的盐,它们的物质的量之比为1︰5,该反应的化学方程式为________。
(6)在25°C、101kPa 下,已知 Y 的简单气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移 1mol 电子放热 190kJ,该反应的热化学方程式为_____。
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化趋势如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期中金属性最强的元素;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法正确的是( )
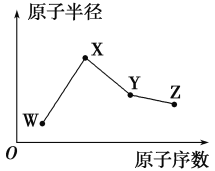
A.对应气态氢化物的稳定性:Y>W
B.对应简单离子的半径:W>Z
C.化合物XZW中既含离子键也含共价键
D.Y的氧化物能与Z的最高价氧化物对应的水化物反应
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是
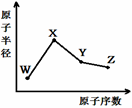
A.化合物XZW既含离子键也含共价键
B.对应气态氢化物的稳定性Y>Z
C.对应简单离子半径:X>W
D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是
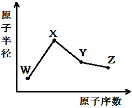
A.化合物XZW既含离子键也含共价键
B.对应气态氢化物的稳定性Y>Z
C.对应简单离子半径:X>W
D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
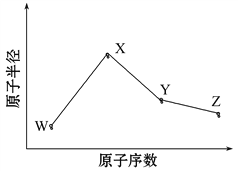
(1)X位于元素周期表中第________周期第________族;W的基态原子核外有________个未成对电子。
(2)Z的气态氢化物和溴化氢相比,较稳定的是________(写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是____________________________________________________。
(4)在25 ℃、101 kPa下,已知Y的气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移1 mol电子放热190.0 kJ,该反应的热化学方程式是_________________________________________________________________。
-
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化关系如图所示。已知X的原子半径在所有原子中最小;Y的一种核素的质量数为15,中子数为8;W的最高价氧化物的水化物在含氧酸中酸性最强。下列说法不正确的是( )
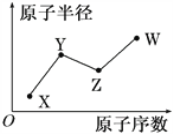
A. X元素有多种核素
B. X与Y可形成YX3型共价化合物
C. Y元素的电负性一定小于Z元素
D. W元素的单质有强氧化性,它不可能与水发生氧化还原反应
具有相同的质子、电子数目:W与Y的氧化物均能导致酸雨的形成;Z的非会属性在同周期主族元素中最强。

△H=—92.4kJ·mo1-1








