-
I .氯及其化合抝在生活中应用广泛。
(1)指出氯元素在周期表中的位置_____________。
(2)净水丸能对饮用水进行快速的杀菌消毒,外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等) 除去。
① 优氯净中氯元素的化合价为___________。
② 亚硫酸钠将水中多余次氯酸除去的离子方程式为___________________。
II.某无机盐M是一种优良的氧化剂,为确定其化学式,设计如下探究实验:
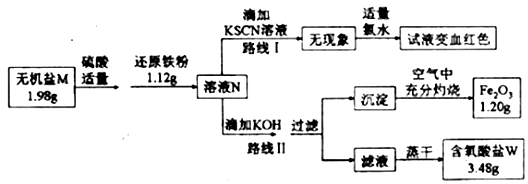
已知:
①无机盐M仅由钾离子和一种含氧酸根组成,其分子中的原子个数比为2:1:4;
②该小组同学将溶液N分为二等份,分别按路线I、路线II进行实验。每步部反应完全。
请按要求回答下列问题:
(1)由路线I的现象可知,溶液N中含有的阳离子是_________。
(2)由实验流程图可推得.含氧酸盐W的化学式是_______;由路线II可知,1.98g无机盐M中所含钾元素的质量为_______g。
(3)无机盐M与1.12g还原铁粉恰好完全反应生成溶液N的化学反应方程为 _______________。
-
Ⅰ(6分)氯及其化合物在生活中应用广泛。
(1)指出氯元素在周期表中的位置
(2)将铁片插入盛有少量新制氯水试管中,无气泡产生,用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,然后红色消失。显红色的离子方程式为__________。
(3)向新制氯水加入碳酸钙固体,可以收集2种气体(水蒸汽除外),写出分子式__________。
Ⅱ(12分)某科研小组为开发新型净水剂,合成中间体物质A,A可以看成由氯化铝和一种盐按物质的量之比1:2组成,有下列变化:
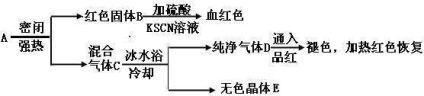
实验发现,加热4.375克A,可得到1.6克B、2.135克E和0.01mol的D。
(1)写出D的化学式__________。
(2)写出A强热发生的化学方程式__________。
(3)E晶体中某种物质在一定条件能和KI固体反应,写出该方程式__________。
将E晶体配成溶液,逐滴加入稀NaOH溶液,现象__________。
(4)若在高温下长时间煅烧A,在气体D中还能检验出另一种气体,分子式是__________。
-
(1)氯及其化合物在生活中应用广泛。
①指出氯元素在周期表中的位置__________。
②将铁片插入盛有少量新制氯水试管中,无气泡产生,用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,然后红色消失。显红色的离子方程式为____________。
③向新制氯水加入碳酸钙固体,可以收集2种气体(水蒸汽除外),写出化学式____________。
(2)净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。
①优氯净中氯元素的化合价为______________。
②亚硫酸钠将水中多余次氯酸除去的化学反应方程式为________________。
(3)某无机盐M是一种优良的氧化剂,为确定其化学式,某小组设计并完成了如下实验:
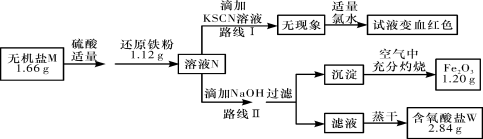
已知:
①无机盐M仅由钠离子和一种含氧酸根组成,其化学式中的原子个数比为1∶2∶4;
②如图中,将1.66 g该无机盐溶于水,滴加适量稀硫酸后,再加入1.12 g还原铁粉,恰好完全反应得混合溶液N;
③该小组同学将溶液N分为二等份,分别按路线Ⅰ、路线Ⅱ进行实验;
④在路线Ⅱ中,首先向溶液N中滴加适量NaOH至元素X刚好沉淀完全,过滤后将沉淀在空气中充分灼烧得纯净的Fe2O3粉末1.20 g;再将滤液在一定条件下蒸干,只得到2.84 g纯净的不含结晶水的正盐W。
请按要求回答下列问题:
①由路线Ⅰ的现象可知,溶液N中含有的阳离子是______________。
②由实验流程图可推得,含氧酸盐W的化学式是______________。
③无机盐M的溶液与1.12 g还原铁粉恰好完全反应生成溶液N的离子反应方程式为_______________。
-
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
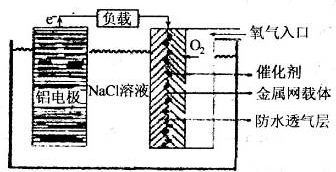
①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为 。
(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
-
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为
(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
-
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是____ 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
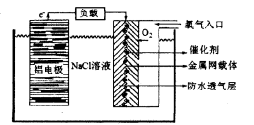
①该电池的总反应化学方程式为____ ;
②电池中NaCI的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCI溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为 。(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
-
铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛.
(1)铁元素在元素周期表中的位置是______.
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示.
①该电池的总反应化学方程式为______;
②电池中NaCl的作用是______.
(3)用铝电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为______,此时向溶液中加入8g CuO固体后可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为______L.
(4)氯化铝广泛用于有机合成和石油工业的催化剂.将铝土矿粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式______ 2AlCl3+3CO.

-
铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛。
(1)铁元素在元素周期表中的位置是__________。
(2)铝电池性能优越,铝-空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

①该电池的总反应化学方程式为____________________________________________。
②电池中NaCl的作用是___________________________________________________。
(3)用铝电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为___________________,此时向溶液中加入SgCuO固体后可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为_______L。
(4)氯化铝广泛用于有机合成和石油工业的催化剂。将铝土矿粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式______________。
(5)三氧化二铁和氧化亚铜(Cu2O)都是红色粉末,常用作燃料。已知氧化亚铜溶于稀硫酸生成Cu和CuSO4。取少量Fe2O3和Cu2O组成的混合物放入足量稀硫酸中。
①此过程中发生的反应有(用离子方程式表示):Fe2O3+6H+=Fe3++3H2O;____________________;____________________。
②设计实验证明反应后所得溶液中铁元素可能存在形式_____________________。
③若实验中观察到溶液变为蓝色且有固体剩余,则n(Cu2O) __________n(Fe2O3)。(填“>”、“<”或“=”)。
-
Co、Ni的化合物在生产生活中有着广泛的应用。
(1)Co元素在周期表中的位置是4周期________族。基态Co原子的简化电子排布式为_________。
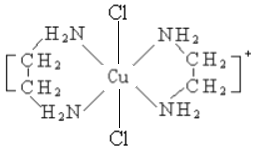
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为________杂化。en可以与Co形成配合物[Co(en)2Cl2]Cl·HCl·2H2O,配离子结构如下左图所示,中心离子的配位数为_______,配合物晶体中可能存在的作用力有___________。
A 离子键 B 极性共价键 C 非极性共价键 D 配位键 E 氢键
(3)天然氧化镍晶体中总是存在晶体缺陷,如图所示。NixO晶体中x值为 ,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。
,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。

(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列, Ni2+填充其中(如图),己知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为_____g(用a、NA表示)。

-
镁合金及镁的化合物在生产、生活中有着广泛的应用。
(1)镁在元素周期表中的位置是____________。
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

① 一段脱水后,残留固体质量占原样品质量的64.5%,试确定生成物的化学式__________。② 二段脱水时,溶入H2和Cl2燃烧产物的目的是__________。
③ 该工艺中可循环使用的物质有_____________
(3)储氢材料Mg(AlH4)2在110-200℃的反应为:Mg(AlH4)2 =MgH2 +2Al+3H2↑,每转移6mol电子生成氢气的物质的量为__________mol。
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。
① 40℃时,复盐开始热解生成MgCO3·3H2O,并有气体产生,该反应的化学方程式为________。
② 制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000g产品用适量硝酸溶解,经稀释等步骤最终配得500mL 的溶液。
a.准确量取25.00mL 待测液,用0.1000 mol/ L AgNO3 标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为______________mL。

b.
| AgCl | AgBr | AgI | Ag2CrO4 |
| Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白 | 淡黄 | 黄 | 砖红 |
参照上表数据及信息分析,滴定时可以作指示剂的是________(填数字序号)。
① CaCl2 ② NaBr ③ NaI ④ K2CrO4
c.滴定时,应将溶液调成中性,不能是强酸性或强碱性,其中不能是强碱性的原因是________。
d.产品中氯的质量分数为___________(保留三位有效数字)。












