-
某同学设计下表所示实验,探究金属铜对H2O2分解速率的影响.
| 操 作 | 装 置 | 现 象 |
| 1.取一个铜丝网,卷成筒形,固定在铁丝上. | 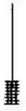 | |
| 2.分别向①和②中注入15mL、30%的H2O2溶液,并放入盛有热水的③中. | 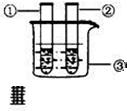 | 约1min后可观察到①和②中都有少量气泡产生. |
| 3.把铜丝网插入①中. | 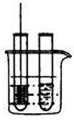 | ①中有大量气泡产生,5min后不再有气泡产生;此时②中仍然不断有少量气泡产生. |
回答下列问题:
(1)仪器①的名称是______;仪器③的名称是______.
(2)仪器②中实验的目的是______.
(3)能否可以得出铜可以加快H2O2分解的速率______(填“是”或“否”),理由是______
(4)如果用上述实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是______.
A.称量实验前铜丝网的质量和实验后干燥铜丝网的质量
B.向仪器②中加入二氧化锰
C.将实验后的铜丝网插入AgNO3溶液中
D.将铁丝换成铜丝
E.将过氧化氢溶液加水稀释.
-
某同学设计下表所示实验,探究金属铜对过氧化氢分解速率的影响。
| 操作 | 装置 | 现象 |
| 1.取一个铜丝网,卷成筒形,固定在铁丝上 | 
| |
| 2.分别向①和②中注入15 mL、30%的过氧化氢溶液,并放入盛有热水的③中 | 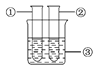
| 约1 min后可观察到①和②中都有少量气泡产生 |
| 3.把铜丝网插入①中 | 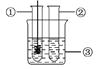
| ①中有大量气泡产生,5 min后不再有气泡产生;此时②中仍然不断有气泡产生 |
回答下列问题:
(1)在操作3中仪器②的实验目的是____________。
(2)是否可以得出铜可以加快过氧化氢分解的速率____________ (选填“是”或“否”)。
(3)如果用上述实验探究铜是不是过氧化氢分解的催化剂,需要对上述实验方案进行补充,其中必要的是____________。(填序号)
A.将铁丝换成铜丝
B.向仪器②中加入二氧化锰
C.将过氧化氢溶液加水稀释
D.检验铜的化学性质是否发生变化
E.称量实验前铜丝网的质量和实验后干燥铜丝网的质量
-
某学习小组的同学对过氧化氢分解进行探究。
Ⅰ.(探究一)影响过氧化氢分解快慢的因素
某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。(实验装置如图所示,夹持仪器已略去)
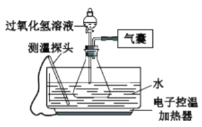
(猜想与假设)影响过氧化氢分解速率的因素可能有
温度、溶液的浓度、催化剂种类。
(实验记录)同学们进行6组实验,实验记录如下:
| 实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 过氧化氢溶液的浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
| 过氧化氢溶液的体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
| 水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
| 锥形瓶中的物质 | ----- | ----- | ----- | ----- | 0.5 gNaCl | 0.5 gFeCl3 |
| 60 min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(解释与结论)
(1)实验②中应加入过氧化氢溶液的体积x是______mL。
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定______来比较过氧化氢的分解速率。
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是_____(填序号)。
(4)通过实验①、②、④可得出的结论是______。
(反思与评价)
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是______(答两点)。
(6)某同学改用如图所示装置代替气囊完成实验②,

正确的实验操作顺序是______。
a将导管伸入量筒,开启控温加热器,滴入过氧化氢溶液
b开启控温加热器,将导管伸入量筒,滴入过氧化氢溶液
c开启控温加热器,滴入过氧化氢溶液,待导管口有连续均匀气泡冒出时将导管伸入量筒
Ⅱ、(探究二)探究Fe2O3是否对过氧化氢分解起催化作用
| 操作步骤 | 实验情况记录 | 结论 |
| ① | 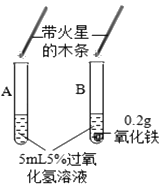
| A试管上方带火星的木条未复燃 B中出现气泡快,带火星的木条复燃 | Fe2O3_____(填“不影响”、“减慢”或“加快”)过氧化氢分解 |
| ② | 将B试管中的混合物过滤,把滤渣烘干、_____。 | 固体质量0.2g | Fe2O3质量未变 |
小组的同学认为要证明Fe2O3是催化剂,上述实验还不够,还需要再增加一个实验,
a、该实验的目的是:_____
b、请你设计实验证明,简要的写出实验步骤及实验现象:_____。
-
现欲探究Fe2O3能否加快H2O2的分解,并与MnO2的催化效果进行比较,甲、乙和丙三位同学同时进行H2O2的分解与气体的收集实验.实验时间均以30秒为准(H2O2均未全部分解),其他可能影响实验的因素均已忽略.相关数据如下:
同学
序号 | 质量分数相同的H2O2溶液 | 溶液中加入的物质 | 收集到的气体体积 |
| 甲 | 100ml | 未加其他物质 | a ml |
| 乙 | 100ml | Fe23 0.5g | b ml |
| 丙 | 100ml | MnO2O.5g | c ml |
欲探究Fe23在实验中是否起催化作用,首先应比较______; (选填a、b、c)的大小,其次需补充做如下实验(无需写出具体操作);①______;②Fe23的化学性质有没有改变.
-
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
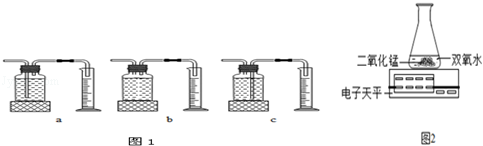
(1)为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g 10%H2O2溶液与1.0g MnO2均匀混合
Ⅱ.将x g 10%H2O2溶液与1.0g CuO均匀混合
在相同温度下,比较两组实验产生O2的快慢.Ⅱ中x的值应为 .
(2)乙探究了影响双氧水分解速度的某种因素.实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
本实验中,测量O2体积的装置是 (填编号)
(3)丙用如图2装置进行实验,通过比较 也能达到实验目的.
-
为探究分子的运动及影响分子运动速率的因素,某同学设计了以下三种实验方案,请回答有关问题(注:酚酞是一种酸碱指示剂,遇碱性物质变红色,遇酸性物质不变色,氨水呈碱性;石蕊溶液也是一种酸碱指示剂,遇碱性物质变蓝色,遇酸性物质变红色,浓盐酸呈酸性)

(1) [实验方案一]如图1。
①观察到的实验现象是_____________________________________________________________________________。
②该方案的不足之处是____________________________________________________________________________。 (说出一点即可)。
(2) [ 实验方案二]如图2、图3。
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40°的热水中。
有①观察到的现象是______________________________________________________________________。
②若图4中的小纸花上喷有___________________________________,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
-
小丽同学在一次课外实验探究酸的化学性质时误将过氧化氢(H2O2)溶液当作酸与氧化铁(Fe2O3)粉末混合,发现有大量气泡产生。她联想到二氧化锰(MnO2)可作为H2O2分解的催化剂,那么,Fe2O3能否作为H2O2分解的催化剂呢?请你一起参与探究,并填写下列空白。
(猜想)Fe2O3能否作为H2O2分解的催化剂。
(实验验证)小丽同学一次设计了三个实验
实验一 取一定量的过氧化氢(H2O2)溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,观察到木条没有复燃,说明H2O2溶液常温下分解缓慢。
实验二 在实验一的试管中加入wg 氧化铁(Fe2O3)粉末,有大量气泡产生,然后伸入带火星的木条,观察到木条复燃,说明_______。
实验三 待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为wg,说明_________。
(实验结论)小丽同学认为,Fe2O3粉末可以作为H2O2分解的催化剂。
(反思评价)小江同学认为要证明小丽同学的结论正确,仅做这三个实验还不充分,需要补充一个探究实验,探究_______。
(拓展)下表是同学们探究影响H2O2分解因素时所记录的部分数据:
用足量等体积H2O2溶液制取相同体积O2所需时间
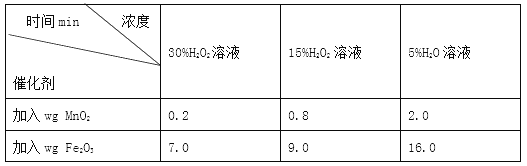
通过对表格中的数据进行分析,你能得出的结论是________。
-
甲同学误把 溶液当作酸与
溶液当作酸与 粉末混合,发现有大量气泡产生.他联想到
粉末混合,发现有大量气泡产生.他联想到 可作为
可作为 分解的催化剂,那么
分解的催化剂,那么 能否作为
能否作为 分解的催化剂呢?请你一起参探究,并填写下列空白:
分解的催化剂呢?请你一起参探究,并填写下列空白:
 能作为
能作为 分解的催化剂.
分解的催化剂.
[实验验证]甲同学依次设计了三个实验:
实验一;取一定量的 溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,没有复燃.说明常温下
溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,没有复燃.说明常温下 溶液缓慢分解.
溶液缓慢分解.
实验二 在实验一的试管中加入 粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃.说明________.
粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃.说明________.
实验三 待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为 .说明________.
.说明________.
[实验结论]甲同学认为, 粉末可以作为
粉末可以作为 分解的催化剂.
分解的催化剂.
[反思评价]乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验.这一探究实验的目的是:________.
-
小雨同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验:
| 实验操作 |  实验现象 实验现象
| 实验结论或总结 |
| 结论 | 总结 |
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 木条不复燃 | 过氧化氢分解产生氧气,但是 。 | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | | |
| 实验三 | | | 二氧化锰能加快过氧化氢的分解 |
| | | | |
(1)请你帮小雨同学填写上表中未填完的空格。
(2)在小雨的探究实验中,“实验 一”和“实验二”起的作用是 。
一”和“实验二”起的作用是 。
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
第一方面的实验操作中包含了两次称量,其目的是: ;
第二方面的实验是利用“实验三”完全反应后试管内的剩余物继续实验。接下来的实验操作、现象和结论是: ;
-
小林同学发现铜制眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称铜绿,主要成分是Cu2(OH)2CO3。为探究铜在空气中生锈的条件,利用图5-5甲装置实验,过近一个月观察,发现B中铜丝生锈,而A、C中铜丝无明显变化。由此小林同学得出结论:铜生锈的主要原因是铜与空气中氧气、水蒸气接触。
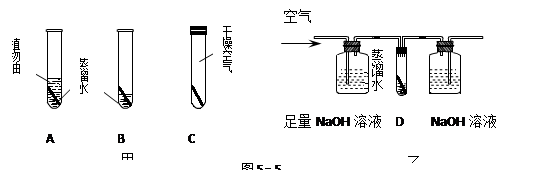
试回答:
(1)该同学得出的结论正确吗?
(2)你认为参与铜生锈的物质还可能有 ,理由是 。
(3)为验证你的判断,可用图中乙所示的装置进行实验,其中NaOH溶液的作用是除去空气中的二氧化碳,通过近一个月的观察发现,D中铜丝基本无变化。由此可认为:铜在 条件下难于生锈,故参与铜生锈的物质有