如图为阳离子交换膜法电解饱和食盐水原理示意图,其中的阳离子交换膜仅允许Na+通过。下列说法错误的是( )

A. a极的电极反应式为:2 H+ + 2 eH2 ↑
B. D口导出的是NaOH溶液
C. C口导出的是NaOH和NaCl的混合溶液
D. 浓盐水从A口注入
高一化学选择题中等难度题
如图为阳离子交换膜法电解饱和食盐水原理示意图,其中的阳离子交换膜仅允许Na+通过。下列说法错误的是( )

A. a极的电极反应式为:2 H+ + 2 eH2 ↑
B. D口导出的是NaOH溶液
C. C口导出的是NaOH和NaCl的混合溶液
D. 浓盐水从A口注入
高一化学选择题中等难度题
如图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是

A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 LCl2,便产生2 mol NaOH
D.F电极材料为金属铁
高一化学选择题简单题查看答案及解析
如图为阳离子交换膜法电解饱和食盐水原理示意图,下列说法不正确的是( )

A.从E口逸出的气体是H2
B.从D口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH
D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,精制时先加Na2CO3溶液
高一化学单选题中等难度题查看答案及解析
目前世界上比较先进的电解制碱技术是离子交换法,如图为阳离子交换膜法电解饱和食盐水的原理示意图。
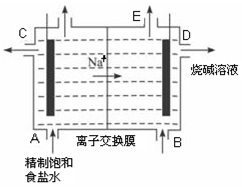
(1)下列说法不正确的是( )
A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH
D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,精制时先加 Na2CO3溶液
(2)现有离子交换膜A和B将电解槽分为I、II、III三个区域(下图所示),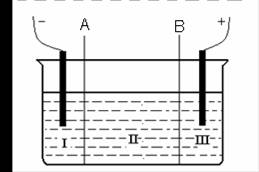
在这种电解池中电解Na2SO4溶液可制得氢氧化钠、硫酸等物质。
A为________离子交换膜、B为________离子交换膜(填“阴”或“阳”),电极均为惰性电极。Na2SO4溶液应该在________区(填“I”、“II”、“III”)加入。通电电解时阴极的电极反应式为________,在III区得到________。当外电路总共通过30 mol电子时,生成的NaOH 960克,则电解过程中能量的转化率为:________
高一化学填空题中等难度题查看答案及解析

高一化学填空题中等难度题查看答案及解析
如图为阳离子交换膜法电解饱和食盐水原理示意图,其中的阳离子交换膜仅允许Na+通过。下列说法错误的是( )

A. a极的电极反应式为:2 H+ + 2 eH2 ↑
B. D口导出的是NaOH溶液
C. C口导出的是NaOH和NaCl的混合溶液
D. 浓盐水从A口注入
高一化学选择题中等难度题查看答案及解析
阳离子交换膜法电解饱和食盐水具有综合能耗低、环境污染小等优点。生产流程如下图所示:

(1)电解饱和食盐水的化学方程式为______。
(2)电解结束后,能够脱去阳极液中游离氯的试剂或方法是_____(填字母序号)。
a.Na2SO4 b.Na2SO3
c.热空气吹出 d.降低阳极区液面上方的气压
(3)在酸性条件下加入NaClO溶液,可将食盐水中的I-转化为I2,再进一步除去。通过测定体系的吸光度,可以检测不同pH下I2的生成量随时间的变化,如下图所示。已知:吸光度越高表明该体系中c(I2)越大。

①结合化学用语解释10 min时不同pH体系吸光度不同的原因:______。
②pH=4.0时,体系的吸光度很快达到最大值,之后快速下降。吸光度快速下降的可能原因:____。
③研究表明食盐水中I-含量≤0.2 mg•L-1时对离子交换膜影响可忽略。现将1m3含I- 浓度为1.47 mg•L-1 的食盐水进行处理,为达到使用标准,理论上至少需要0.05 mol•L-1 NaClO溶液_____L。(已知NaClO的反应产物为NaCl,溶液体积变化忽略不计)
高一化学综合题中等难度题查看答案及解析
工业上电解制碱的技术是用阳离子交换膜法,主要原料是饱和食盐水。下图为阳离子交换膜法电解原理示意图:
请回答下列问题:

(1)A极为电解槽的________极,B极的材料工业上常采用的是生活中常见的金属,但有大量损耗,其主要原因是 。(填“吸氧腐蚀”或“析氢腐蚀”)
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号)。
①H2,②Cl2,③H+,④Cl-,⑤Na+,⑥OH-。
(3)若上述电解过程中用阴离子交换膜代替阳离子交换膜(已知:3Cl2 +6OH-==5Cl-+ClO3-+3H2O),下列说法正确的组合是 。
A.电解结束时,右侧溶液中含有ClO3—
B.电解槽内发生反应的总化学方程式为:NaCl + 3H2O NaClO3 + 3H2↑
C.用阴离子交换膜后,电解槽内两个电极发生的电极反应与原来一样
D.用阴离子交换膜后,阳离子的定向移动方向与原来相反
(4)已知某电解槽每小时加入10%的氢氧化钠溶液a kg,每小时能产生标准状况下的氯气b L,则电解后流出的氢氧化钠溶液(密度为d g·cm-3)的物质的量浓度为(理论计算,需化简) mol/L。
高一化学填空题中等难度题查看答案及解析
下列叙述正确的是
A.电解饱和食盐水制烧碱采用离子交换膜法,可以阻止阳离子通过
B.在铁上镀锌时,锌棒作阴极,且电解液硫酸锌的浓度是不变的
C.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1: 2
D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH
高一化学选择题中等难度题查看答案及解析
如图所示表示的是电解饱和食盐水的装置,阴极材料、阳极材料都是碳棒,饱和食盐水中含有少量酚酞。
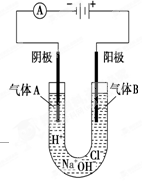
(1)接通电源后,饱和食盐水中的阳离子的移动方向是:向________极移动。
(2)电极上生成了气体A和B,生成气体A的电极反应式是 ________。
(3)随着气体的生成,饱和食盐水中产生了两种不同的颜色:一种是 ________色,其产生的位置是 ________(填“阴极区”或“阳极区”);另一种是 ________色,其产生的位置是 ________(填“阴极区”或“阳极区”)。
高一化学填空题中等难度题查看答案及解析
目前电解法制烧碱通常采用离子交换膜法,阳(阴)离子交换膜不允许阴(阳)离子通过。则下列叙述中错误的是( )

A. NaOH、H2均在Ⅰ区产生
B. 图中a为阴离子交换膜
C. 使用离子交换膜可以有效地隔离NaOH和Cl2,阻止二者之间的反应
D. 电解时往Ⅲ区的溶液中滴加几滴甲基橙,溶液先变红后褪色
高一化学选择题中等难度题查看答案及解析