-
(15分,除标明外,其余每空2分)物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2 2(t-BuNO)
2(t-BuNO)
(1)当(t-BuNO)2的起始浓度(c0)为0.50mol·L-1时,实验测得20℃时的平衡转化率(α)是60%。20℃时上述反应的平衡常数K= 。
(2)一定温度下,随着(t-BuNO)2的起始浓度增大,其平衡转化率 (填“增大”、“不变”或“减小”)。已知20℃时该反应在CCl4溶剂中的平衡常数为1.70mol·L-1,若将反应溶剂正庚烷改成CCl4,并保持(t-BuNO)2起始浓度相同,则它在CCl4溶剂中的平衡转化率 (填“大于”、“等于”或“小于”)其在正庚烷溶剂中的平衡转化率。
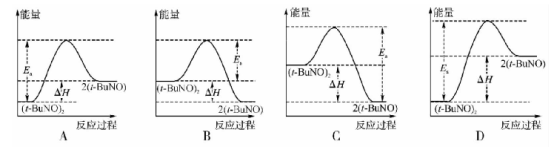
(3)实验测得该反应的ΔH=+50.5kJ·mol-1,活化能Ea=90.4kJ·mol-1。下列能量关系图合理的是 (填字母)。

(4)该反应的ΔS (填“>”、“<”或“=”)0。在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(5)通过比色分析得到30℃时(t-BuNO)2浓度随时间的变化关系如图所示,请在同一图中绘出t-BuNO浓度随时间的变化曲线

-
物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2 2(t-BuNO)
2(t-BuNO)
(1)当(t-BuNO)2的起始浓度(c0)为0.50mol·L―1时,实验测得20℃时的平衡转化率(α)是60%。20℃时上述反应的平衡常数K= 。
(2)一定温度下,随着(t-BuNO)2的起始浓度增大,其平衡转化率 (填“增大”、“不变”或“减小”)。已知20℃时该反应在CCl4溶剂中的平衡常数为1.70mol·L―1,若将反应溶剂正庚烷改成CCl4,并保持(t-BuNO)2起始浓度相同,则它在CCl4溶剂中的平衡转化率 (填“大于”、“等于”或“小于”)其在正庚烷溶剂中的平衡转化率。
(3)实验测得该反应的ΔH=+50.5kJ·mol―1,活化能Ea=90.4kJ·mol―1。下列能量关系图合理的是 (填字母)。
(4)该反应的ΔS (填“>”、“<”或“=”)0。在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(5)通过比色分析得到30℃时(t-BuNO)2浓度随时间的变化关系如右图所示,请在同一图中绘出t-BuNO浓度随时间的变化曲线。

-
物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2
 2(t-BuNO).
2(t-BuNO).
(1)当(t-BuNO)2的起始浓度(c)为0.50mol•L-1时,实验测得20℃时的平衡转化率(α)是65%.列式计算20℃时上述反应的平衡常数K=______.
(2)一定温度下,随着(t-BuNO)2的起始浓度增大,其平衡转化率______(填“增大”、“不变”或“减小”).
已知20℃时该反应在CCl4溶剂中的平衡常数为1.9,若将反应溶剂正庚烷改成CCl4,并保持(t-BuNO)2起始浓度相同,则它在CCl4溶剂中的平衡转化率______(填“大于”、“等于”或“小于”)其在正庚烷溶剂中的平衡转化率.
(3)实验测得该反应的△H=50.5kJ•mol-1,活化能Ea=90.4kJ•mol-1.下列能量关系图合理的是______.

(4)该反应的△S______0(填“>”、“<”或“=”).在______(填“较高”或“较低”)温度下有利于该反应自发进行.
(5)随着该反应的进行,溶液的颜色不断变化,分析溶液颜色与反应物(或生成物)浓度的关系(即比色分析),可以确定该化学反应的速率.用于比色分析的仪器是______.
A.pH计B.元素分析仪 C.分光光度计 D.原子吸收光谱仪
(6)通过比色分析得到30℃时(t-BuNO)2浓度随时间的变化关系如图所示,请在同一图中绘出t-BuNO浓度随时间的变化曲线.

-
物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2 2(t-BuNO)。在20℃时,向2 L正庚烷中加入(t-BuNO)2 1.0 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为75%(假设反应过程中溶液体积始终为2 L)。下列说法正确的是
2(t-BuNO)。在20℃时,向2 L正庚烷中加入(t-BuNO)2 1.0 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为75%(假设反应过程中溶液体积始终为2 L)。下列说法正确的是

A.反应在前10 min内的平均速率为ν(t-BuNO)=0.0375 mol·L-1·min-1
B.保持其他条件不变,若此时再向正庚烷反应体系中加入正庚烷,平衡向生成(t-BuNO)2的方向移动
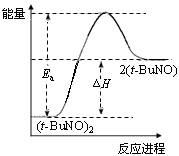
C.保持其他条件不变,升高温度,(t-BuNO)2的平衡转化率大于75%,则其能量关系可用右图表示
D.保持其他条件不变,若该反应在CCl4中进行,其平衡常数为1.9,则(t-BuNO)2的平衡转化率大于75%
-
物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2 2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
A.反应在前10 min内的平均速率为ν(t-BuNO)=0.0325 mol·L-1·min-1
B.保持其他条件不变,若此时再向溶液中加入0.50 mol (t-BuNO)2,重新达平衡时(t-BuNO)2的百分含量减小
C.保持其他条件不变,若该反应在CCl4中进行,其平衡常数为1.9,则(t-BuNO)2的平衡转化率小于65%
D.保持其他条件不变,升高温度, (t-BuNO)2的平衡转化率大于65%,则其能量关系可用下图表示
-
在相同温度下,将H2和N2两种气体按不同比例通入相同的恒容密闭容器中,发生反应:3H2+N2 2NH3。
2NH3。 表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等。下列图像正确的是( )
表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等。下列图像正确的是( )


-
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,2SO2+O2 2SO3,其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
2SO3,其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
| 甲 | 乙 | 丙 | 丁 |
| 密闭容器体积/L | 2 | 2 | 2 | 1 |
| 起始物质的量 | n(SO2)/ mol | 0.40 | 0.80 | 0.80 | 0.40 |
| n(O2)/ mol | 0.24 | 0.24 | 0.48 | 0.24 |
| SO2的平衡转化率% | 80 | α1 | α2 | α3 |
A.甲中反应的平衡常数小于乙
B.该温度下,该反应的平衡常数K为400
C.SO2的平衡转化率:α1>α2=α3
D.容器中SO3的物质的量浓度:丙=丁<甲
-
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,
2SO2+O2 2SO3,其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
2SO3,其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
| 甲 | 乙 | 丙 | 丁 |
| 密闭容器体积/L | 2 | 2 | 2 | 1 |
| 起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 |
| SO2的平衡转化率% | 80 |  1 1
|  2 2
|  3 3
|
| | | | | |
A.甲中反应的平衡常数小于乙
B.该温度下,该反应的平衡常数K为400
C.SO2的平衡转化率: 1>
1> 2 =
2 =  3
3
D.容器中SO3的物质的量浓度:丙=丁<甲
-
某温度下,三个容积均为2.0 L恒容密闭容器中发生反应2NO(g)+2CO(g) N2(g)+2CO2(g),各容器中起始物质的量浓度与反应温度如下表所示:
N2(g)+2CO2(g),各容器中起始物质的量浓度与反应温度如下表所示:
| 容器 | 温度/℃ | 起始物质的量浓度/(mol·L-1) |
| NO(g) | CO(g) | N2 | CO2 |
| 甲 | T1 | 0.10 | 0.10 | 0 | 0 |
| 乙 | T2 | 0 | 0 | 0.10 | 0.20 |
| 丙 | T2 | 0.10 | 0.10 | 0 | 0 |
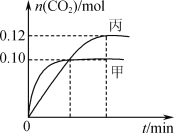
反应过程中甲、丙容器中CO2的物质的量随间变化关系如图所示。下列说法正确的是
A.该反应的正反应为放热反应,平衡常数K(T1)<K(T2)
B.达到平衡时,乙容器中的压强一定大于甲容器的2倍
C.乙容器中反应达到平衡时,N2的转化率大于40%
D.丙容器中反应达到平衡后,再充入0.10 mol NO和0.10 mol CO2,此时v(正)>v(逆)
-
在VL密闭容器中,通入0.2mol SO2和0.2mol SO3气体,在一定条件下发生反应:2SO2+O2 2SO3。平衡时SO3为amol;在相同温度下按下列配比在VL密闭容器中放入起始物质,平衡时有关SO3的正确叙述是
2SO3。平衡时SO3为amol;在相同温度下按下列配比在VL密闭容器中放入起始物质,平衡时有关SO3的正确叙述是
A.放入0.2mol SO2、0.1molO2、0.1mol SO3,达到平衡时SO3必小于amol
B.放入0.2mol SO2、0.1molO2、0.2mol SO3,达到平衡时SO3必小于amol
C.放入0.4mol SO2、0.1molO2,达到平衡时SO3会等于0.4mol
D.放入0.2mol SO2、0.1molO2,达到平衡时SO3必小于amol
2(t-BuNO)










