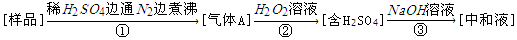-
(15分)亚硫酸盐是一种常见食品添加剂。为检验某食品中亚硫酸盐含量(通常1kg样品中含SO2的质量计),某研究小组设计了如下两种实验流程:
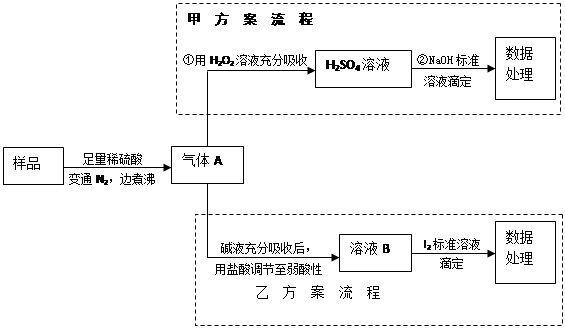
(1)气体A的主要成分是________,为防止煮沸时发生暴沸,必须先向烧瓶中加入________
________;通入N2的目的是。
(2)写出甲方案第①步反应的离子方程式:________。
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是________
________。
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果________(填“偏高”、“偏低”或“无影响”)
(5)若取样品wg,按乙方案测得消耗0.01000mol·L—1I2溶液VmL,则1kg样品中含SO2的质量是________g(用含w、V的代数式表示)。
-
亚硫酸盐是一种常见食品添加剂.为检验某食品中亚硫酸盐含量(通常1kg样品中含SO2的质量计),某研究小组设计了如下两种实验流程:
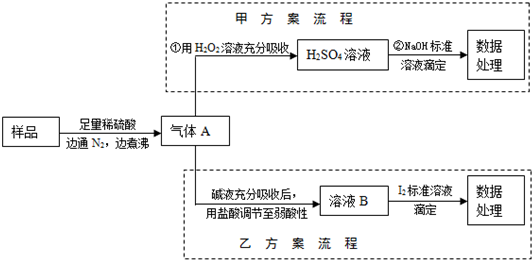
(1)气体A的主要成分是________,为防止煮沸时发生暴沸,必须先向烧瓶中加入________;通入N2的目的是________.
(2)写出甲方案第①步反应的离子方程式:________.
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是________.
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果________(填“偏高”、“偏低”或“无影响”)
(5)若取样品wg,按乙方案测得消耗0.01000mol•L-1I2溶液VmL,则1kg样品中含SO2的质量是________g(用含w、V的代数式表示).
-
亚硫酸盐是一种常见食品添加剂.为检验某食品中亚硫酸盐含量(通常1kg样品中含SO2的质量计),某研究小组设计了如下两种实验流程:

(1)气体A的主要成分是________,为防止煮沸时发生暴沸,必须先向烧瓶中加入________;通入N2的目的是________.
(2)写出甲方案第①步反应的离子方程式:________.
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是________.
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果________(填“偏高”、“偏低”或“无影响”)
(5)若取样品wg,按乙方案测得消耗0.01000mol•L-1I2溶液VmL,则1kg样品中含SO2的质量是________g(用含w、V的代数式表示).
-
亚硫酸盐是一种常见的食品添加剂。用如图实验可检验某食品中亚硫酸盐含量(含量通常以1kg样品中含SO2的质量计;所加试剂均足量),下列说法不正确的是( )
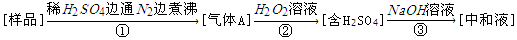
A.亚硫酸盐作为食品添加剂作用是防腐、抗氧化
B.反应①中通入N2的作用是将生成的气体全部赶出
C.测定样品质量及③中耗碱量,可测定样品中亚硫酸盐含量
D.若仅将②中的氧化剂“H2O2溶液”替换为碘水,对测定结果无影响
-
亚硝酸盐是一种常见的食品添加剂,使用时必须严格控制其用量。为检测某食品中亚硝酸盐含量(通常以1kg样品中含NaNO2的质量计,假定食品本身不参与反应),某研究小组设计了如下实验方案:

(1)实验过程中需配制500 mL 0.0010 mol/L (NH4)2Fe(SO4)2标准溶液,如下图所示的仪器中肯定不需要的是 (填序号),配制上述溶液还需要用到的玻璃仪器是 (填仪器名称)。配制溶液时,定容的操作方法是 。
(2)已知亚硝酸钠(NaNO2)的水溶液呈弱碱性,则亚硝酸的电离方程式为 .
(3)完成并配平实验方案中反应①的离子方程式,并用单线桥表示电子转移的方向和数目:
□MnO + □ NO
+ □ NO + □
+ □  □ Mn2+ + □ NO
□ Mn2+ + □ NO + □ ,
+ □ ,
(4)若称取样品a g进行测定,准确量取12.00 mL 0.0005 mol/L的酸性KMnO4溶液(过量)与溶液
A反应。反应后溶液用0.0010 mol/L (NH4)2Fe(SO4)2 标准溶液滴定至紫色溶液刚好褪去;重复上述实验2次,平均消耗(NH4)2Fe(SO4)2溶液10.00 mL,则1 kg样品中 NaNO2的质量为_______mg (用含a的代数式表示).
-
亚硫酸盐是一种常见的食品添加剂,用如图实验可检验某食品中亚硫酸盐含量(含量通常以1kg样品中含SO2的质量计;所加试剂均足量)。下列说法不正确的是

A. 葡萄酒酿造时通入SO2起到了杀菌和增酸的作用
B. 反应①中若不通入N2则测得的SO2含量偏低
C. 反应①中煮沸的目的是加快亚硫酸的分解,降低SO2的溶解度
D. 若仅将②中的氧化剂“H2O2溶液”替换为“溴水”,对测定结果无影响
-
(14分)亚硝酸盐是一种常见的食品添加剂,使用时必须严格控制其用量。为检测某食品中亚硝酸盐含量(通常以1kg样品中含NaNO2的质量计),某研究小组设计了如下两种实验方案:(提示 : 无色气体B遇空气显红棕色)
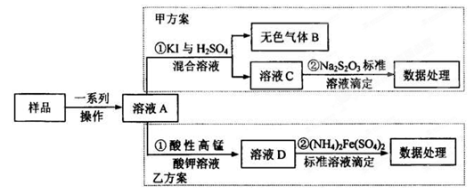
(1)甲方案②中常用 做指示剂。若需配制80 mL0.001 mol·L-1的Na2S2O3标准溶液。现给出下列仪器(配制过程中可能用到):①50 mL烧杯②胶头滴管③天平④80 mL容量瓶⑤100 mL容量瓶⑥玻璃棒,按使用仪器的先后顺序排列正确的是
A.③①⑤⑥② B.③①⑥④② C.③①⑥⑤② D.③①④⑥②
请写出配制Na2S2O3标准溶液时定容的操作
(2)已知酸性条件下MnO4—被还原为Mn2+,请写出乙方案①的离子方程式
(3)若取样品ag,按乙方案进行测定,准确量取12.00mL0.0005mol/L的酸性KMnO4溶液(过量)与溶液A反应。反应后溶液用0.0010mol/L(NH4)2Fe(SO4)2标准溶液滴定至溶液紫色刚好褪去;重复上述实验2次,平均消耗(NH4)2Fe(SO4)2溶液10.00mL.则1kg样品中 NaNO2的质量为_______mg.
(4)若乙方案②中使用的(NH4)2Fe(SO4)2溶液暴露在空气中时间过长,则会导致测定出的NaNO2含量 (填“偏高”、“偏低”或“不影响”)
(5)小组经过讨论,认为 方案更佳,原因是 。
-
亚硝酸盐是一祌常见的食品添加剂,使用时必须严格控制其用量。为检测某食品中亚硝酸盐含量(通常以1kg样品中含NaNO2的质量计),某研究小组设计了如下两种实验方案: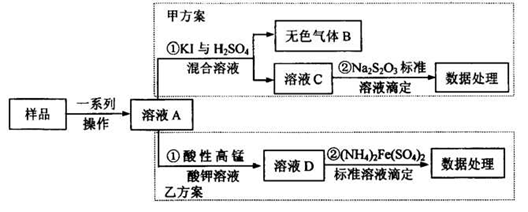
(1)无色气体B遇空气显红棕色,B的化学式为_______写出甲方案①中反应的离子方程式_______
(2)完成并配平乙方案①中反应的离子方程式
MnO4-+ NO2-+ ________= Mn2++ NO3-+ ________,
(3)乙方案②中需配置100mL0.0010mol/L(NH4)2Fe(SO4)2标准溶液,在已准确称量样品的质量后,还需要的仪器有:量筒、烧杯、_______配制溶液时,定容的操作方法是______
(4)若取样品ag,按乙方案进行测定,准确量取12.00mL0.0005mol/L的酸性高锰酸钾 溶液(过童)与溶液A反应。反应后溶液用0.0010mol/L(NH4)2Fe(SO4)2标准溶液滴定至紫色 溶液刚好褪去;重复上述实验2次,平均消耗(NH4)2Fe(SO4)2溶液10.00mL.则1kg样品中 NaNO2的质量为_______mg.
-
亚硫酸盐是一种常见食品添加剂。为检测某食品中亚硫酸盐含量(通常以1 kg样品中含SO2的质量计)。某研究小组设计了如下两种实验流程:
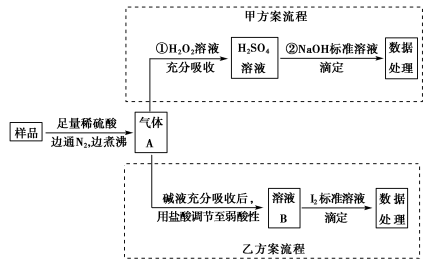
(1)气体A的主要成分是________。为防止煮沸时发生暴沸,必须先向烧瓶中加入________;通入N2的目的是________。
(2)写出甲方案第①步反应的离子方程式:________________________。
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是__________________________________________________________。
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果________(填“偏高”“偏低”或“无影响”)。
(5)若取样品w g,按乙方案测得消耗0.010 00 mol·L-1I2溶液V mL,则1 kg样品中含SO2的质量是________g(用含w、V的代数式表示)。
-
为检测某食品中亚硫酸盐含量(通常以1kg样品中含SO2的质量计),某研究小组设计了如下实验流程:
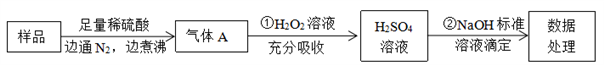
(1)通入N2的目的是_______________________
(2)第①步反应的离子方程式是______________________
(3)滴定实验若选择酚酞作指示剂,则滴定终点的标志是________滴定过程中以下操作使测定结果偏高的是________(填编号)
a. 洗净的滴定管未用标准液润洗
b. 滴定中向锥形瓶内壁加少量水
c. 滴定前滴定管正常,滴定后尖嘴部分有气泡
d. 锥形瓶用待测液洗涤2-3次
(4)若实验室欲制取SO2可选用试剂__________(填编号)
a. 铜和浓硫酸 b. 硫和氧气
c. 亚硫酸钠和浓度70%的硫酸 d. 亚硫酸钙和硝酸
(5)往BaCl2溶液中通入SO2至饱和,无明显现象,再通入NH3后出现白色沉淀,此时溶液中一定有的溶质是_________。请用电离平衡解释上述实验现象:_________________
(6)H2O2是一种绿色氧化剂。某NH4Cl样品中含少量Fe2+、SO42-,将产品溶解,加入H2O2,加热至沸,再加入BaCl2溶液,过滤,蒸发结晶,即得到工业氯化铵。
滤渣的主要成分是_______________________