-
(1)SiO4-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子排布图是____________________。
②写出与SiO4-具有相同空间构型和键合形式的微粒,分子和离子各写一个_______。
③下图为一种硅氧组群的结构示意图,其离子符号为____,其中Si原子的杂化方式为_____。
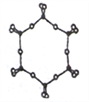
④电负性:Si____O(填“>”、“=”或“<”) 。
(2)2017年,我国科学家又在碳原子研究上获得突破:由中科院大学物理学院苏刚教授等人通过理论计算预言的一种三维碳结构T-碳(T-carbon) 诞生,中外科学家联合研究团队成功合成了T-碳,从而使T-碳成为可与石墨和金刚石比肩的碳的另一种三维新结构。T碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代形成碳的一种新型三维立方晶体结构,如下图。T-碳属于_____晶体。已知T-碳晶胞参数为a pm,阿伏伽德罗常数为NA,则T碳的密度的表达式为_______g/cm3。(写出表达式即可)

-
某硅酸盐研究所在硅酸盐材料和闪烁晶体等领域研究上取得了重大的成就。
(1)[SiO4]4-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子的轨道表示式是_____________。
②与[SiO4]4-互为等电子体的微粒符号是_____________任写一种)。
③右图为一种硅氧组群的结构示意图,其离子符号为_____________,其中Si原子的杂化方式为_____________。
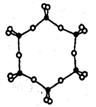
④电负性:Si ______O (填“>”、 “=”或“<” )。
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如右图所示。
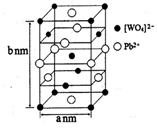
①PWO中钨酸根结构式为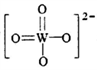 ,该离子中,σ键和π键的个数比是_____________。
,该离子中,σ键和π键的个数比是_____________。
②PWO晶体中含有的微粒间作用力是_____________ (填标号)。
A.范德华力 B.离子键 C.共价键 D.金属键
③己知PWO的摩尔质量为Mg·mol-1,则该晶体的密度d=_____________g·cm-3。
-
某硅酸盐研究所在硅酸盐材料和闪烁晶体等领域研究上取得了重大的成就。
(1)[SiO4]4-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子的轨道表示式是_____________。
②与[SiO4]4-互为等电子体的微粒符号是_____________任写一种)。
③右图为一种硅氧组群的结构示意图,其离子符号为_____________,其中Si原子的杂化方式为_____________。
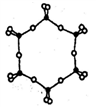
④电负性:Si ______O (填“>”、 “=”或“<” )。
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如右图所示。

①PWO中钨酸根结构式为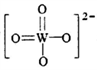 ,该离子中,σ键和π键的个数比是_____________。
,该离子中,σ键和π键的个数比是_____________。
②PWO晶体中含有的微粒间作用力是_____________ (填标号)。
A.范德华力 B.离子键 C.共价键 D.金属键
③己知PWO的摩尔质量为Mg·mol-1,则该晶体的密度d=_____________g·cm-3。
-
[化学—选修3:物质结构与性质]某硅酸盐研究所在硅酸盐材料和闪烁晶体等领域研究上取得了重大的成就。
(1)SiO44-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子排布图是________。
②与SiO44-互为等电子体的微粒符号是______(任写一种)。
③下图为一种硅氧组群的结构示意图,其离子符号为______,其中Si原子的杂化方式为____。

④电负性:Si______O(填“>”、“=”或“<”) 。
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如图所示。
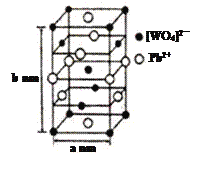
①PWO中钨酸根结构式式为 ,该离子中δ键和π键的个数比是______。
,该离子中δ键和π键的个数比是______。
②PWO晶体中含有的微粒间作用力是______(填标号)。
A.范德华力 B.离子键
C.共价键 D.金属键
③己知晶体的摩尔质量为Mg·mol-1,则该晶体的密度d=_______g·cm-3。(阿伏加德罗常数用NA表示)
-
(12分)现有部分前四周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| A | 原子的电子排布图为 |
| B | 常温下单质为双原子分子,原子间形成三对共用电子对 |
| C | 原子的s轨道电子数等于p轨道电子数,元素的最低负价为-2价 |
| D | 二价阳离子与C的阴离子具有相同的电子层结构 |
| E | 原子序数是D两倍, |
根据以上情况,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的电负性由小到大的顺序为________;
(2)B的氢化物的分子空间构型是________,该氢化物的等电子体是________;
(3)E的价电子排布式是________,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界,ECl3形成的配合物的化学式为________;
(4)AC2在高温高压下所形成的晶胞如图所示。该晶体的类型属于________(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中A原子的杂化形式为________;

(5)D 的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:________。
-
硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元.硅氧四面体可以用投影图表示成
 ,其中O表示氧原子,中心黑点表示硅原子.硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子.图示为某无限长单链的多聚硅酸根离子(见图),试确定该阴离子中硅原子与氧原子的个数之比为( )
,其中O表示氧原子,中心黑点表示硅原子.硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子.图示为某无限长单链的多聚硅酸根离子(见图),试确定该阴离子中硅原子与氧原子的个数之比为( )

A.1:2
B.1:3
C.1:4
D.2:5
-
硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以用投影图表示成 ,其中O表示氧原子,中心黑点表示硅原子。硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子。下图为某无限长单链的多聚硅酸根离子:
,其中O表示氧原子,中心黑点表示硅原子。硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子。下图为某无限长单链的多聚硅酸根离子:

试确定该阴离子中硅原子与氧原子的个数之比为
A.1︰2 B.1︰3 C.1︰4 D.2︰5
-
B元素和N元素对植物生长及人体健康有着十分重要的作用,也广泛应用于新型材料的制备。
(1)基态氮原子的外围电子排布图为________________;晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的__________________性。
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,与氨硼烷互为等电子体的分子、离子的化学式分别是______________、________________。 (各举一例),第二周期元素中第一电离能介于B和N之间的元素是______________(填元素符号)。
(3)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如下图:
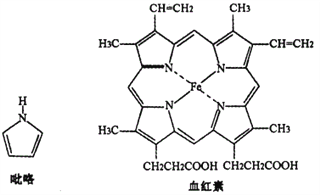
①己知吡咯中的各个原子均在同一平面内;则吡咯分子中N原子的杂化类型为________________。
②1mol吡咯分子中所含的σ键总数为__________个;分子中的大π键可用Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为____________。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为____________。
③C、N、O三种元素的简单氢化物键角由小到大的顺序为_____________(填化学式),原因是__________________。
④血液中的O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过___________键相结合。
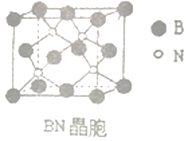
(4)氮化硼(BN)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。已知该晶体密度为ag/cm3,根据硬球接触模型计算晶体中两个最近的N原子间的距离为:_________pm。(用含a的代数式表示,NA表示阿伏加德罗常数)
-
(12分)⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为▲ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为▲ 。在四大晶体类型中,GaN属于▲ 晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有▲ 的原子或离子
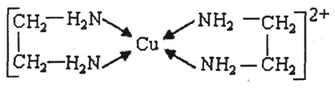
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:

① H、N、O三种元素的电负性由大到小的顺序是▲ 。
②SO2分子的空间构型为▲ 。与SnCl4互为等电子体的一种离子的化学式为▲
③乙二胺分子中氮原子轨道的杂化类型为▲ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是▲ 。
④⑶中所形成的配离子中含有的化学键类型有▲ 。
a.配位键 b.极性键 c.离子键 d.非极性键
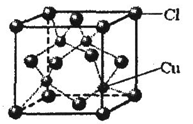
⑤CuCl的晶胞结构如上图所示,其中Cl原子的配位数为▲ 。
-
⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为▲ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为▲ 。在四大晶体类型中,GaN属于▲ 晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有▲ 的原子或离子
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
① H、N、O三种元素的电负性由大到小的顺序是▲ 。
②SO2分子的空间构型为▲ 。与SnCl4互为等电子体的一种离子的化学式为▲
③乙二胺分子中氮原子轨道的杂化类型为▲ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是▲ 。
④⑶中所形成的配离子中含有的化学键类型有▲ 。
a.配位键 b.极性键 c.离子键 d.非极性键
⑤CuCl的晶胞结构如右图所示,其中Cl原子的配位数为▲ 。





 ,该离子中,σ键和π键的个数比是_____________。
,该离子中,σ键和π键的个数比是_____________。

 ,该离子中,σ键和π键的个数比是_____________。
,该离子中,σ键和π键的个数比是_____________。


 ,其中O表示氧原子,中心黑点表示硅原子.硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子.图示为某无限长单链的多聚硅酸根离子(见图),试确定该阴离子中硅原子与氧原子的个数之比为( )
,其中O表示氧原子,中心黑点表示硅原子.硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子.图示为某无限长单链的多聚硅酸根离子(见图),试确定该阴离子中硅原子与氧原子的个数之比为( )






