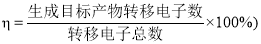-
乙炔(CH≡CH)是重要的化工原料,广泛应用于焊割、燃料电池及有机合成等。
(1)乙炔-空气燃料电池是一种碱性(20%-30%的KOH溶液)燃料电池。电池放电时,负极的电极反应式为_____________;
(2)科学家利用“组合转化技术”,将乙炔燃烧产物CO2转化成乙烯,反应式为:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g)下图为温度对CO2平衡转化率、催化剂催化效率的影响。下列说法正确的是_____(填序号)
CH2=CH2(g)+4H2O(g)下图为温度对CO2平衡转化率、催化剂催化效率的影响。下列说法正确的是_____(填序号)

①250℃时,催化剂的催化效率最大
②随着温度升高,乙烯的产率增大
③M点平衡常数比N点平衡常数大
④N点正反应速率一定大于M点正反应速率
⑤增大压强可提高乙烯的体积分数
(3)甲烷裂解法制取乙炔的反应方程式为:2CH4(g) C2H2(g)+3H2(g)。已知:
C2H2(g)+3H2(g)。已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1= a kJ·mol-1
C2H2(g)+2.5O2(g)=2CO2(g)+H2O(l) △H2= b kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H3= c kJ·mol-1
则2CH4(g) C2H2(g)+3H2(g) △H=______kJ·mol-1
C2H2(g)+3H2(g) △H=______kJ·mol-1
(4)哈斯特研究发现:甲烷裂解时,几种气体平衡时分压(Pa)与温度(℃)之间的关系如图所示。甲烷裂解可能发生的反应有:2CH4(g) C2H2(g)+3H2(g),2CH4(g)
C2H2(g)+3H2(g),2CH4(g) C2H4(g)+2H2(g)。
C2H4(g)+2H2(g)。
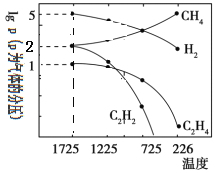
①1725℃时,向1L恒容密闭容器中充入0.3molCH4,达到平衡时,测得c(C2H2)=c(CH4)。则CH4生成C2H2的平衡转化率为_______;
②1725℃时,反应2CH4(g) C2H2(g)+3H2(g)的平衡常数Kp=_________(用平衡分压代替平衡浓度);
C2H2(g)+3H2(g)的平衡常数Kp=_________(用平衡分压代替平衡浓度);
③由图可知,甲烷裂解制乙炔有副产物乙烯生成。为提高甲烷制乙炔的产率,除改变温度外,还可采取的措施有_______。
-
(共14分)氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料。
(1)以氨为燃料可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用。若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为 。
(2)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2 2NH3。该可逆反应达到平衡的标志是________________。
2NH3。该可逆反应达到平衡的标志是________________。
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时消耗3m mol H2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间变化
E.a molN≡N键断裂的同时,有6amolN—H键断裂
F.N2、H2、NH3的分子数之比为1∶3∶2
(3)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入1molN2和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则从反应开始到25min时,以N2表示的平均反应速率= ;该温度下平衡常数K= ;
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g) == NH2CO2 NH4(s) △H= —l59.5 kJ/mol
②NH2CO2NH4(s)  CO(NH2)2(s)+H2O(g) △H=+116.5 kJ/mol
CO(NH2)2(s)+H2O(g) △H=+116.5 kJ/mol
③H2O(1) == H2O(g) △H=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式 ;
对于上述反应②在密闭容器中将过量NH2CO2NH4固体于300K下分解,平衡时P[H2O(g)]为a Pa,若反应温度不变,将体系的体积增加50%,则P[H2O(g)]的取值范围是_________________(用含a的式子表示)。(分压=总压×物质的量分数)
-
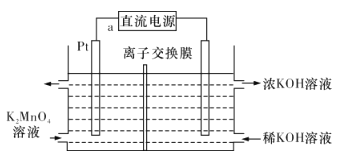
高锰酸钾在化工医药、水处理等很多方面有重要应用,可以用电解法制备,装置如下。直流电源采用乙烷—空气的碱性燃料电池。下列说法不正确的是(已知电流效率η=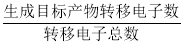 ×100%)
×100%)
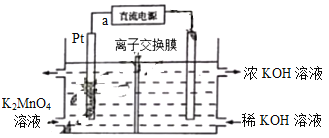
A. 电源负极的电极反应式为C2H6-14e-+18OH-=2CO32-+12H2O
B. 该离子交换膜为阴离子交换膜
C. a极为直流电源的正极
D. 若消耗0.02mo1 ,产生0.055mol
,产生0.055mol ,则
,则
-
高锰酸钾在化工医药、水处理等很多方面有重要应用,可以用电解法制备,装置如图所示。直流电源采用乙烷一空气的碱性燃料电池。下列说法正确的是
(已知电流效率η= ×100%)
×100%)
A.电源负极的电极反应式为C2H6- 14e- +6H2O=2CO32-+ 18H+
B.该离子交换膜为阴离子交换膜
C.a极为直流电源的负极
D.若消耗0. 02 mol O2,产生0.055 mol KMnO4,则η=68.75%
-
高锰酸钾在化工医药、水处理等很多方面有重要应用,可以用电解法制备,装置如图所示。直流电源采用乙烷 空气的碱性燃料电池。下列说法正确的是
空气的碱性燃料电池。下列说法正确的是 已知电流效率
已知电流效率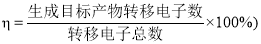



A.电源负极的电极反应式为
B.该离子交换膜为阳离子交换膜
C.透过离子交换膜的离子是
D.若 ,阴极产生氢气0.02mol,则产生
,阴极产生氢气0.02mol,则产生
-
乙炔广泛用于焊接、焊割及有机合成等方面。
(1)已知下列热化学方程式:
4CH4 (g)+3O2(g)==2C2H2(g)+6H2O(g) △H1=a kJ•mol-1;
2H2(g)+O2(g)==2H2O(g) △H2=b kJ•mol-1;
2CH4(g)==C2H2(g)+3H2 (g) △H3
①△H3=____________________ (用含a、b的代数式表示)kJ•mol-1。
②已知下列共价健的键能数据:
| 共价键 | C—H | H—H | C C C |
| 键能/ kJ•mol-1 | 413.4 | 436 | 812 |
则△H3=____________________ (填数值)kJ•mol-1。
(2)氯仿(CHCl3)与金属银共热可以制取乙炔,该反应的化学方程式为__________________________。
(3)向压强为1.0×104 kPa的恒压密闭容器中充入1 mol乙炔和1 mol HC1气体,在催化剂作用下乙炔与HC1发生反应:HC CH(g)+HCl(g)
CH(g)+HCl(g) CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
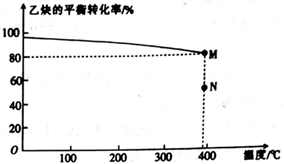
①该反应的△H__________(填“>”或“<”)0,N点时乙炔的反应速率v(正)________(填“>”或“<” 或“=”) v(逆)。
② M点对应温度下,该反应的平衡常数Kp=_________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(kPa)-1,
-
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
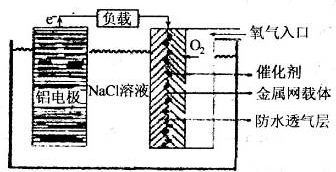
①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为 。
(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
-
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为
(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
-
神舟十号飞船,神舟飞船的统一双组元,推进系统采用肼作为燃料,简化了增压系统的设计,工作更为可靠。 肼——空气燃料电池是一种碱性燃料电池,电解质溶液是20% ~ 30%的KOH 溶液,总反应式为N 2H4+O2=N2+2H2O,下列说法中,错误的是
A.该电池放电时,通入肼的一极为负极
B.电池每释放1molN2转移的电子数为4NA
C.电池工作一段时间后,电解质溶液的pH将不变
D.通入空气的一极的电极反应式是:O2+2H2O+4e-=4OH-
-
(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%~30%的KOH溶液.电池总反应为:N2H4+O2=N2+2H2O.下列关于该燃料电池工作时的说法正确的是( )
A.负极的电极反应式是:N2H4+4OH-→4H2O+N2↑+4e-
B.正极的电极反应式是:O2+4H++4e-→2H2O
C.溶液中阴离子向正极移动
D.电解后电解质溶液的碱性增强
CH2=CH2(g)+4H2O(g)下图为温度对CO2平衡转化率、催化剂催化效率的影响。下列说法正确的是_____(填序号)

C2H2(g)+3H2(g)。已知:
C2H2(g)+3H2(g) △H=______kJ·mol-1
C2H2(g)+3H2(g),2CH4(g)
C2H4(g)+2H2(g)。

C2H2(g)+3H2(g)的平衡常数Kp=_________(用平衡分压代替平衡浓度);
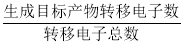 ×100%)
×100%)

 ×100%)
×100%)