-
锂离子电池广泛用作便携式电源,其正极材料是决定锂离子电池可逆容量与循环寿命的关键因素之一。锂二次电池一般以LiCoO2、LiFePO4等为正极材料,以石墨碳为负极材料,以溶有LPF6、LiBF4等的碳酸二乙酯(DEC) 为电解液。充电时,Li+ 从正极层状氧化物的晶格间脱出进入有机电解液,有机电解液中的Li+则进入负极,得电子后以原子形式嵌入到石墨材料的晶格中,即: 6C+xLi++xe-=LixC6,如图所示:

(1)如图所示,已知该电池电极总反应:LiCoO2+C Li1-xCoO2+CLix,充电时,该电池的正极上的反应为_______________________。
Li1-xCoO2+CLix,充电时,该电池的正极上的反应为_______________________。
(2)放电时负极材料质量________(填“增加”、“减小”或“不变”)
(3)在实验室中,可用下列方案从废旧锂离子电池的正极材料中(主要含有LiCoO2、炭粉及少量Al、Fe等) 回收钴和锂。

①溶解过程中,通入SO2时所发生反应的化学方程式为________________________;
②除杂过程中,所得沉淀的主要成分是___________________;(写化学式)
③常温下,已知Ksp[Co(OH)2]=1.09×10-15,若沉淀钴时pH=9.5,则溶液中Co2+是否沉淀完全? 请列式计算说明。 _______________________________________________。
-
锂离子电池己被广泛用作便携式电源。正极材料为LiCoO2、LiFePO4等,负极材料一般为石墨碳,以溶有LiPF6、LiBF4等的碳酸二乙酯(DEC)作电解液。
(1)Fe2+基态核外电子排布式为 ________。
(2)PO43-的空间构型为 ________ (用文字描述)。
(3) 中
中 的配位数为6,该配合物中的配位原子为 _____。
的配位数为6,该配合物中的配位原子为 _____。
(4)碳酸二乙酯(DEC)的分子结构如图所示,分子中碳原子的轨道杂化类型为_____,1mol碳酸二乙酯(DEC)中含有σ键的数目为_____。

(5)氮化锂是一种新型无机贮氢材料,其晶胞结构如图所示,该晶体的化学式为_______。

-
铁、钴、镍具有相似的性质,在化学上称为铁系元素。回答下列问题:
(1)LiCoO2、 LiFePO4常用作锂离子电池的正极材料。
基态Co原子核外电子排布式为___________________,第四电离能I4(Co) _________I4(Fe)(填“>”或“<”),PO43-的空间构型为___________________。
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基配合物。在CO分子中,σ键与π键数目之比为_________。
(3)铁与K2O、 (环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,配体配位数为 ________。二茂铁熔点为446K,不溶于水,易溶于乙醚、苯、乙醇等有机溶剂,373K即升华;从各种性质看,都表明它是典型的_________晶体。
(环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,配体配位数为 ________。二茂铁熔点为446K,不溶于水,易溶于乙醚、苯、乙醇等有机溶剂,373K即升华;从各种性质看,都表明它是典型的_________晶体。
(4)与铁同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种,往其溶液中加BaCl2溶液时,有白色沉淀;加入AgNO3溶液时,没有沉淀生成;加入氢氧化钠溶液时,无气体生成。则此种配合物的化学式为 _________________________。
(5)铁单质的堆积方式有两种,其剖面图分别如图a、b所示。
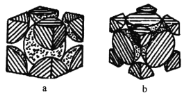
在图a所示堆积方式里铁原子的堆积方式为___________________________。
在图b所示堆积方式里铁原子的总体积占晶体体积的比例为(空间利用率)_________。
-
钴酸锂电池应用广泛,电池正极材料主要含有LiCoO2、导电剂乙炔黑、铝箔及少量Fe,可通过下列实验方法回收钴、锂。
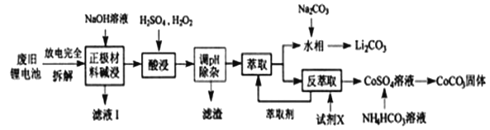
几种金属离子沉淀完全(离子浓度为10-5mo/L) 的pH如下表:
| 离子 | Fe3+ | Al3+ | Fe2+ | Co2+ |
| 溶液pH | 3.2 | 4.7 | 9.0 | 9.2 |
回答下列问题:
(1)滤液I的主要成分是_________。
(2)已知: 氧化性Co3+>H2O2>Fe3+,“酸浸”过程中H2O2所起主要作用是________不能用盐酸代替硫酸,原因是:__________。“调节pH”除去的离子主要有Al3+和_____。
(3)酸浸时浸出率随温度变化如图所示,温度升高至50℃以上时浸出率下降的原因是_________。

(4)“萃取”和“反萃取“可简单表示为: Co2++2( HA)2 Co(HA2)2+2H+,则反萃取过程加入的试剂X是____________。
Co(HA2)2+2H+,则反萃取过程加入的试剂X是____________。
(5)向CoSO4溶液中加入NH4HCO3溶液,发生反应的离子方程式为_________。
-
钻酸锂电池成用广泛,电池正极材料主要含有LiCoO2、导电剂乙炔黑。铝箔及少量Fe,可通过下列实验方法回收钴、锂。
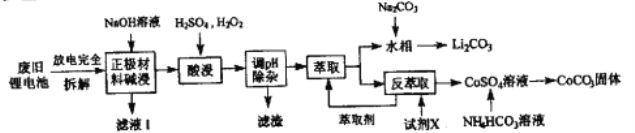
几种金属离子沉淀完全(离子浓度为10-5mol/L)的pH如下表:
| 离子 | Fe3+ | Al3+ | Fe2+ | Co2+ |
| 溶液pH | 3.2 | 4.7 | 9.0 | 9.2 |
回答下列问题:
(1)LiCoO2中,Co 元素的化合价为_______,滤液I的主要成分是______。
(2)已知: 氧化性Co3+>H2O2>Fe3+,“酸浸”过程中H2O2所起主要作用是______。“调节pH”除去的离子主要有Al3+和____。
(3)酸浸时浸出率随温度变化如图所示,温度升高至50℃以上时浸出率下降的原因是________。

(4)“萃取”和“反萃取“可简单表示为: Co2++2(HA)2  Co(HA2)2+2H+则反萃取过程加入的试剂X是_______。
Co(HA2)2+2H+则反萃取过程加入的试剂X是_______。
(5)向CoSO4溶液中加入NH4HCO3溶液,发生反应的离子方程式为__________。
-
随新能源汽车的发展,新能源电池技术也在不断创新,典型的锂离子电池一般以LiCoO2或LiFePO4等为正极材料,以石墨碳为负极材料,以溶有LiPF6等的有机溶液为电解质溶液。
(1)P原子的电子排布式为_________。Fe2+中未成对电子数为___________。
(2)N、O、F原子的第一电离能由小到大的顺序为_______。
(3)等电子体具有相似的化学键特征,它们的许多性质是相近的。ClO4-与PO43-互为等电子体,ClO4-的立体构型为_______,中心原子的杂化轨道类型为________。
(4)烷烃同系物中,CH4的沸点最低,原因是______________。
(5)向CuSO4溶液中加入氨水,首先形成蓝色沉淀,继续加氨水,沉淀溶解,得到深蓝色溶液,在此溶液中加入乙醇,析出深蓝色的晶体。由蓝色沉淀得到深蓝色溶液的离子方程式为_______________;深蓝色晶体中存在的化学键类型有__________ 。(填代号)
A.离子键
B.σ键
C.非极性共价键
D.配位键
E.金属键
F.氢键
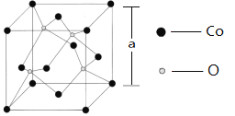
(6)如图所示为Co的某种氧化物的晶胞结构图,则该氧化物的化学式为______;若该晶胞的棱长为a pm,则该晶体的密度为_____________g/cm3。(NA为阿伏加德罗常数的值)
-
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钻(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为 ,下列说法正确的是( )
,下列说法正确的是( )
A.充电时,电池的负极反应为LiC6-e-=Li+C6
B.放电时,电池的正极反应为CoO2+Li++e-=LiCoO2
C.羧酸、醇等含活泼氢气的有机物可用作锂离子电池的电解质
D.锂离子电池的比能量(单位质量释放的能量)低
-
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li 被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为CoO2+LiC6 LiCoO2+C6,下列说法正确的是
LiCoO2+C6,下列说法正确的是
A.充电时,电池的阳极反应为LiC6 — e— = Li+ + C6
B.放电时,电池的正极反应为 CoO2 +Li++ e— = LiCoO2
C.乙酸、乙醇等含活泼氢的有机物可做该锂离子电池的电解质
D.该锂离子电池的比能量(消耗单位质量电极所释放的电量)比铅蓄电池低
-
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为CoO2+LiC6 LiCoO2+C6,下列说法正确的是( )
LiCoO2+C6,下列说法正确的是( )
A.充电时,电池的负极反应为LiC6-e- Li++C6
Li++C6
B.放电时,电池的正极反应为CoO2+Li++e- LiCoO2
LiCoO2
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D.锂离子电池的比能量(单位质量释放的能量)低
-
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为LiCoO2+ C6 CoO2+ LiC6,下列说法正确的是
CoO2+ LiC6,下列说法正确的是
A. 充电时,电池的负极反应为 LiC6- e-="=" Li + C6
B. 放电时,电池的正极反应为 CoO2+ Li++ e-="=" LiCoO2
C. 羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D. 锂离子电池的比能量(单位质量释放的能量)低

Li1-xCoO2+CLix,充电时,该电池的正极上的反应为_______________________。







 Co(HA2)2+2H+则反萃取过程加入的试剂X是_______。
Co(HA2)2+2H+则反萃取过程加入的试剂X是_______。