-
(14分)镁及其化合物在生产生活中有重要的作用。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:

(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为________。指出该物质在工农业生产中的一种用途:________。
(2)写出预氨化时发生的主要反应的离子方程式:。
(3)沉淀镁时反应的温度不宜过高,原因是________。
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③________;④________;⑤称量MgO。
18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a=________;b =________;c =________。
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁。有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则。你同意该同学的想法吗?为什么?你的观点是________。理由是________。
-
镁及其化合物在生产生活中有重要的作用.以水氯镁石为原料生产碱式碳酸镁的主要流程如下:

(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为______.指出该物质在工农业生产中的一种用途:______.
(2)写出预氨化时发生的主要反应的离子方程式:______.
(3)沉淀镁时反应的温度不宜过高,原因是______.
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3•bMg(OH)2•cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③______;④______;⑤称量MgO.18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:a=______;b=______;c=______.
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁.有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则.你同意该同学的想法吗?为什么?你的观点是______.理由是______.
-
以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
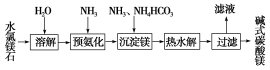
(1)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp=1.8×10-11,若溶液中c(OH-)=3.0×10-6 mol·L-1,则溶液中c(Mg2+)= 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式
(3)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数 (填“升高”、“降低”或“不变”)。
-
碱式碳酸镁不溶于水,用途广泛,主要用作橡胶制品的填充剂,能增强橡胶的耐磨性和强度。也可用作油漆和涂料的添加剂,也可用于牙膏、医药和化妆品等工业。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:

(1)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Ksp(Mg(OH)2)=1.8×10-11,表示Mg(OH)2沉淀溶解平衡的方程式为_______________,Mg(OH)2达到沉淀溶解平衡时溶液的pH______(已知:lg36≈1.5)。
(2)已知:常温下Ka1(H2CO3)=4.4×10-7,Ka2(H2CO3)=4.7×10-11,Kb(NH3·H2O)=1.8×10-5,则NH4HCO3溶液显________性,c(NH4+)________c(HCO3-)(选填“大于”、“小于”、“等于”),该溶液物料守恒表达式为________________。
(3)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为____________。
(4)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁晶体4.84 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO20.896 L,则碱式碳酸镁的化学式为________________,写出氯化镁、氨、碳酸氢铵热水解生成碱式碳酸镁的离子方程式________________________。
-
碱式碳酸镁不溶于水,用途广泛,主要用作橡胶制品的填充剂,能增强橡胶的耐磨性和强度。也可用作油漆和涂料的添加剂,也可用于牙膏、医药和化妆品等工业。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:

(1)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Ksp(Mg(OH)2)=1.8×10-11,表示Mg(OH)2沉淀溶解平衡的方程式为 ,Mg(OH)2达到沉淀达到沉淀溶解平衡时溶液的pH (已知:lg36≈1.5)。
(2)已知:常温下Ka1(H2CO3)=4.4×10-7,Ka2(H2CO3)=4.7×10-11,Kb(NH3·H2O)=1.8×10-5,则NH4HCO3溶液显 性,c(NH) c(HCO)(选填“大于”、“小于”、“等于”),该溶液物料守恒表达式为 。
(3)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为____________。
(4)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁晶体4.84 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,则碱式碳酸镁的化学式为 ,写出氯化镁、氨、碳酸氢铵热水解生成碱式碳酸镁的离子方程式 。
-
碱式碳酸镁不溶于水,用途广泛,主要用作橡胶制品的填充剂,能增强橡胶的耐磨性和强度。也可用作油漆和涂料的添加剂,也可用于牙膏、医药和化妆品等工业。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
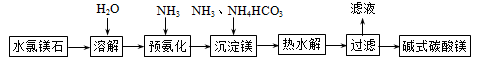
(1)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Ksp(Mg(OH)2)=1.8×10-11,表示Mg(OH)2沉淀溶解平衡的方程式为 ,Mg(OH)2达到沉淀达到沉淀溶解平衡时溶液的pH (已知:lg36≈1.5)。
(2)已知:常温下Ka1(H2CO3)=4.4×10-7,Ka2(H2CO3)=4.7×10-11,Kb(NH3·H2O)=1.8×10-5,则NH4HCO3溶液显 性,c(NH) c(HCO)(选填“大于”、“小于”、“等于”),该溶液物料守恒表达式为 。
(3)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为____________。
(4)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁晶体4.84 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,则碱式碳酸镁的化学式为 ,写出氯化镁、氨、碳酸氢铵热水解生成碱式碳酸镁的离子方程式 。
-
用碱式溴化镁废渣[主要成分为Mg(OH)Br,还含有少量有机溶剂及高分子化合物]生产C2H5Br(不溶于水,密度为1.46g/cm3)和MgCl2·6H2O,既可减少污染又可得化工原料,有关工艺流程如图所示:

回答下列问题:
(1)碱式溴化镁溶于盐酸时,1molMg(OH)Br消耗0.5mol/L的盐酸体积为_______________。
(2)分离Ⅰ操作为_______________(操作名称);分离Ⅱ操作时所需的玻璃仪器为_______________。
(3)提溴时,溶液预热至60℃时开始通入氯气,一段时间后,溶液的温度会自然升高到100℃,说明提溴反应为_______________(填“放热”或“吸热”)反应。提溴废液需减压蒸发浓缩,目的是_______________。
(4)在浓硫酸催化下,合成溴乙烷粗品的化学方程式为_______________;
(5)精制溴乙烷的步骤为水洗、Na2SO3溶液洗涤、水洗及干燥,其中Na2SO3溶液洗涤的目的是_______________。
(6)用惰性电极在一定条件下电解MgCl2溶液可制取催熟剂氯酸镁,该电解反应的化学方程式为_______________。
-
镍及其化合物在生产生活中有着极其重要的作用。现以低品位镍红土矿(主要成分为镍的氧化物、Fe2O3·H2O和SiO2等)为原料制备兰尼镍的工艺流程如图所示:
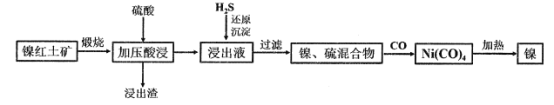
已知加压酸浸过程中的相关影响因素如下:
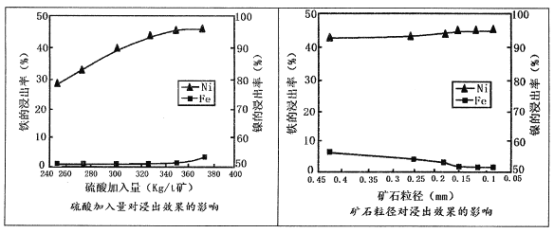
请回答:
(1)请根据图示,选择加压酸浸过程中硫酸的加入量和矿石粒径的最适宜条件为_______
A.260Kg/t矿;0.45mm B.320 Kg/t矿:0.25mm
C.350Kg/t矿;0.15mm D.380 Kg/t矿;0.05mm
(2)①已知镍红土矿煅烧后生成Ni2O3,而加压酸浸后浸出液中含有Ni2+,写出加压酸浸过程中镍元素所涉及的化学反应方程式____________。
②甲同学取该浸出液,控制pH为2~3,经过-系列操作,制取少量NiSO4·7H2O晶体。其控制pH为2~3的目的为____________________________________________________。
③乙同学取该浸出液,经多次处理,得到一定浓度的NiSO4溶液,往其中加入适量的NaClO和NaOH混合液,制得碱性镍电池电极材料NiOOH,该反应的离子方程式为____________。
(3)向浸出液中通入H2S气体,该反应的离子方程式为__________。
(4)下列说法正确的是________________
A.在煅烧过程中,空气宜选择从下往上的通入方式,使镍红土矿燃烧更充分
B.加压酸浸中,为加快反应速率,可选用浓硫酸
C.加压酸浸中,在最适宜条件下,浸出渣中的主要成份为SiO2和Fe2O3·H2O
D.CO为无色无味的有毒气体,故从镍硫混合物到镍的过程中,需注意通风并及时检测操作过程中是否有CO泄露
-
光卤石是化工生产中一种重要的中间产物,其化学成分是KCl•MgCl2•6H2O.当用光卤石为原料制取金属镁时,一共有下列几步:①过滤 ②溶解 ③加入适量Ca(OH)2 ④蒸发 ⑤用盐酸溶解 ⑥电解熔融MgCl2 ⑦在HCl气流中强热MgCl2•6H2O晶体,正确的顺序是( )
A.⑤③①②④⑥⑦
B.②③①⑤④⑦⑥
C.②④①③⑦⑤⑥
D.⑤③①④②⑦⑥
-
锶(Sr)为第五周期IIA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
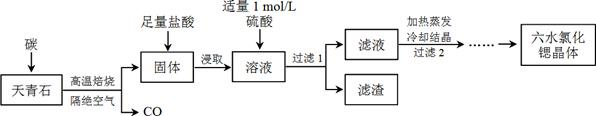
(1)工业上天青石焙烧前先研磨粉碎,其目的是_______________________________。
(2)工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:__________________________。
(3)加入硫酸的目的是____________________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol/L[注:此时滤液中Ba2+浓度为1×10−5 mol/L,Ksp(BaSO4)=1.1×10−10,Ksp(SrSO4)=3.3×10−7]。
(4)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10−2 mol的AgNO3溶液(溶液中除Cl−外,不含其它与Ag+反应的离子),待Cl−完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______________(保留4位有效数字)。
(5)工业上常用电解熔融SrCl2制锶单质。由SrCl2·6H2O制取无水氯化锶的方法是____________。









