-
用NH3催化还原NxOy可以消除氮氧化物的污染。
已知:反应I: 4NH3(g)+6NO(g)  5N2(g)+6H2O(l) ΔH1
5N2(g)+6H2O(l) ΔH1
反应II: 2NO(g)+O2(g)  2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
反应III:4NH3(g)+6NO2(g)  5N2(g)+3O2(g)+6H2O(l) ΔH3
5N2(g)+3O2(g)+6H2O(l) ΔH3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 |
| 398 | K1′ | K2′ |
(1)ΔH3=____________(用ΔH1、ΔH2的代数式表示);推测反应III是________反应(填“吸热”或“放热”)。
(2)相同条件下,反应I在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①计算0~4分钟在A催化剂作用下,反应速率v(NO)=______________。
②下列说法不正确的是_______。
A.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如右。溶液中OH−向电极____移动(填a或b),负极的电极反应式为________________。

-
用NH3催化还原NxOy可以消除氮氧化物的污染。
已知:反应I:4NH3(g)+6NO(g) 5N2(g)+6H2O(l) ΔH1
5N2(g)+6H2O(l) ΔH1
反应II:2NO(g)+O2(g) 2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
反应III:4NH3(g)+6NO2(g) 5N2(g)+3O2(g)+6H2O(l) ΔH3
5N2(g)+3O2(g)+6H2O(l) ΔH3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 |
| 398 | K1′ | K2′ |
(1)ΔH3=_________(用ΔH1、ΔH2的代数式表示);推测反应III是________反应(填“吸热”或“放热”)。
(2)相同条件下,反应I在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。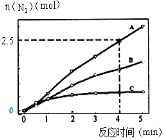
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=______________。
②下列说法不正确的是__________。
A.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如右。溶液中OH−向电极___________移动(填a或b),负极的电极反应式为________________。

-
对已达到平衡的反应4NH3(g)+6NO(g)⇌5N2(g)+ 6H2O( g) ,减小压强,产生的影响是 ( )
A.正反应速率增大,逆反应速率减小
B.正反应速率减小,逆反应速率增大
C.正、逆反应速率都减小
D.正、逆反应速率都增大
-
已知:反应I: 4NH3(g)+6NO(g) 5N2(g)+6H2O(l)△H1
5N2(g)+6H2O(l)△H1
反应II:2NO(g)+O2(g)  2NO2(g) △H2(且|△H1|=2|△H2|)
2NO2(g) △H2(且|△H1|=2|△H2|)
反应III:4NH3(g)+6NO2(g)  5N2(g)+3O2(g)+6H2O(l)△H3
5N2(g)+3O2(g)+6H2O(l)△H3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表:
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 |
| 398 | K1′ | K2′ |
(1)△H3 = (用△H1、△H2 的代数式表示);推测反应III是 反应(填“吸热”或“放热”)
(2)相同条件下,反应I:4NH3(g)+6NO(g) 5N2(g)+6H2O(l)在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。
5N2(g)+6H2O(l)在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①计算0~4分钟在A催化剂作用下,反应速率V(NO)= 。
②下列说法不正确的是 。
A.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)一定条件下,反应II达到平衡时体系中n(NO) ∶n(O2)∶n(NO2)=2∶1∶2。
①保持恒温恒容,再充入NO2气体, NO2体积分数__________(填“变大”、“变小”或“不变”)
②关于平衡体系反应II:2NO(g)+O2(g)  2NO2(g);△H2说法正确的是__________。
2NO2(g);△H2说法正确的是__________。
A、该反应焓变为负值
B、升高温度,逆反应速率增大,正反应速率减小,反应逆向移动
C、不论增大压强还是减小压强,正方向速率改变的程度更大
D、平衡正向移动,NO的转化率一定增大
E、平衡体系中加入NO2,平衡逆向移动,△H2减小
F、混合气体颜色加深说明平衡向右移动,颜色变浅则向左移动
-
对已达到平衡的反应4NH3(g)+6NO(g)⇌5N2(g)+6H2O( g) 减小压强,产生的影响是
A.正、逆反应速率都减小,平衡向正反应方向移动
B.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
D.正、逆反应速率都增大,平衡不发生移动
-
氮的重要化合物如氨(NH3)、 氮氧化物(NxOy)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用。
(1)NH3催化氣化可制备硝酸。
①NH3氧化时发生如下反应:
4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g) △H1=-907.28kJ·mol-1
4NO(g)+ 6H2O(g) △H1=-907.28kJ·mol-1
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H2=-1269.02kJ·mol-1
2N2(g)+6H2O(g) △H2=-1269.02kJ·mol-1
则4NH3(g)+ 6NO(g) 5N2(g)+6H2O(g) △H3_____。
5N2(g)+6H2O(g) △H3_____。
②NO被O2氧化为NO2。其他条件不变时,NO的转化率[a(NO)]与温度、压强的关系如下图所示。则p1____p2 (填“><“或“=”);

③在500℃温度时,2L密闭容器中充入2molNO和1molO2,达平衡时压强为p2MPa。则500℃时该反
应的平衡常数Kp=______,(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
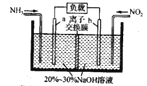
(2)利用反应NO2+NH3→N2+H2O (未配平)消除NO2的简易装置如下图所示。电极b的电极反应式为_____,消耗标准状况下4.48LNH3时,被消除的NO2的物质的量为______mol。
(3) 在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F 等的无水熔融物生产NF3,
其电解原理如图所示。
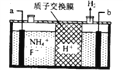
①a 电极为电解池的______(填“阴”或“阳”) 极,写出该电极的电极反应式:_________;电解过程中
还会生成少量氧化性极强的气体单质,该气体的分子式是_________。
②已知同温时NH3·H2O的电离常数小于氢氟酸的电离常数,则0.1mo/LNH4F 溶液中所有离子浓度由大到小的顺序为_______________。
-
用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①
②
③
下列说法不正确的是 ( )
A.等物质的量的CH4参加反应,反应①②转移的电子数相同
B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l);⊿H=-618KJ/mol
C.0.2 mol CH4还原NO2至N2,且生成H2O(g)放出的热量为173.4kJ
D.若用4.48 L(标准状况)CH4还原NO2至N2,整个过程中转移电子1.60mol
-
目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+4NO2 (g)=4NO(g)+CO2 (g)+2H2 O(g) ΔH=-574 kJ·mol-1
②CH4 (g)+4NO(g)=2N2 (g)+CO2 (g)+2H2 O(g) ΔH=-1160 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)  N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
| 浓度/mol·L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
①不能作为判断反应达到化学平衡状态的依据是_____ __
A.容器内CO2的浓度保持不变
B.v正(N2)=2 v正(NO)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
②在该温度下时.该反应的平衡常数为 (保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是___ __。
(3)合成塔失去活性的铬锌触媒可用于制备锌锰电池。在碱性条件下,该电池的总反应为:Zn(s)+2MnO2 (s)+H2O(l)= Zn(OH)2 (s)+Mn2O3(s),该电池正极的电极反应式是 。PbO2 可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生反应的电极反应式为 ,阴极上观察到的现象是 ;若电解液中不加入Cu(NO3)2这样做的主要缺点是 。
-
消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
③H2O(g)=H2O(l)ΔH=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式__________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
| 浓度/mol·L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
①不能作为判断反应达到化学平衡状态的依据是___ ____
A.容器内CO2的浓度保持不变 B.v正(N2)=2 v正(NO) C.容器内压强保持不变
D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为 (保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是____ _ _ ___。
(3) 甲烷燃料电池可以提升能量利用率,下图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
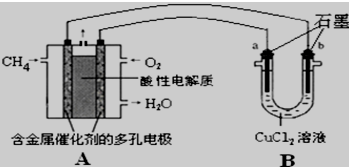
请回答:
①甲烷燃料电池的负极反应式是
②当A中消耗0.15mol氧气时,B中 (用a或b 表示)极增重 g.
-
为消除NO对环境的污染,可利用NH3在一定条件下与NO反应生成无污染的气体。
已知:①N2 (g)+O2 (g) 2NO(g) △H=+180.50 kJ·mol-1
2NO(g) △H=+180.50 kJ·mol-1
②4NH3 (g)+5O2 (g) 4NO(g) +6H2O(g) △H=-905.48 kJ·mol-1
4NO(g) +6H2O(g) △H=-905.48 kJ·mol-1
则反应4NH3 (g)+6NO(g) 5N2 (g)+6H2O(g)的△H是( )
5N2 (g)+6H2O(g)的△H是( )
A.+2.98 kJ·mol-1 B.-2.98 kJ·mol-1
C.+1807.98 kJ·mol-1 D.-1807.98 kJ·mol-1
5N2(g)+6H2O(l) ΔH1
2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
5N2(g)+3O2(g)+6H2O(l) ΔH3








