-
已知:反应I: 4NH3(g)+6NO(g) 5N2(g)+6H2O(l)△H1
5N2(g)+6H2O(l)△H1
反应II:2NO(g)+O2(g)  2NO2(g) △H2(且|△H1|=2|△H2|)
2NO2(g) △H2(且|△H1|=2|△H2|)
反应III:4NH3(g)+6NO2(g)  5N2(g)+3O2(g)+6H2O(l)△H3
5N2(g)+3O2(g)+6H2O(l)△H3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表:
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 |
| 398 | K1′ | K2′ |
(1)△H3 = (用△H1、△H2 的代数式表示);推测反应III是 反应(填“吸热”或“放热”)
(2)相同条件下,反应I:4NH3(g)+6NO(g) 5N2(g)+6H2O(l)在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。
5N2(g)+6H2O(l)在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①计算0~4分钟在A催化剂作用下,反应速率V(NO)= 。
②下列说法不正确的是 。
A.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)一定条件下,反应II达到平衡时体系中n(NO) ∶n(O2)∶n(NO2)=2∶1∶2。
①保持恒温恒容,再充入NO2气体, NO2体积分数__________(填“变大”、“变小”或“不变”)
②关于平衡体系反应II:2NO(g)+O2(g)  2NO2(g);△H2说法正确的是__________。
2NO2(g);△H2说法正确的是__________。
A、该反应焓变为负值
B、升高温度,逆反应速率增大,正反应速率减小,反应逆向移动
C、不论增大压强还是减小压强,正方向速率改变的程度更大
D、平衡正向移动,NO的转化率一定增大
E、平衡体系中加入NO2,平衡逆向移动,△H2减小
F、混合气体颜色加深说明平衡向右移动,颜色变浅则向左移动
-
用NH3催化还原NxOy可以消除氮氧化物的污染。
已知:反应I: 4NH3(g)+6NO(g)  5N2(g)+6H2O(l) ΔH1
5N2(g)+6H2O(l) ΔH1
反应II: 2NO(g)+O2(g)  2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
反应III:4NH3(g)+6NO2(g)  5N2(g)+3O2(g)+6H2O(l) ΔH3
5N2(g)+3O2(g)+6H2O(l) ΔH3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 |
| 398 | K1′ | K2′ |
(1)ΔH3=____________(用ΔH1、ΔH2的代数式表示);推测反应III是________反应(填“吸热”或“放热”)。
(2)相同条件下,反应I在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①计算0~4分钟在A催化剂作用下,反应速率v(NO)=______________。
②下列说法不正确的是_______。
A.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如右。溶液中OH−向电极____移动(填a或b),负极的电极反应式为________________。

-
用NH3催化还原NxOy可以消除氮氧化物的污染。
已知:反应I:4NH3(g)+6NO(g) 5N2(g)+6H2O(l) ΔH1
5N2(g)+6H2O(l) ΔH1
反应II:2NO(g)+O2(g) 2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
反应III:4NH3(g)+6NO2(g) 5N2(g)+3O2(g)+6H2O(l) ΔH3
5N2(g)+3O2(g)+6H2O(l) ΔH3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 |
| 398 | K1′ | K2′ |
(1)ΔH3=_________(用ΔH1、ΔH2的代数式表示);推测反应III是________反应(填“吸热”或“放热”)。
(2)相同条件下,反应I在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。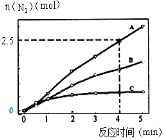
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=______________。
②下列说法不正确的是__________。
A.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如右。溶液中OH−向电极___________移动(填a或b),负极的电极反应式为________________。

-
对已达到平衡的反应4NH3(g)+6NO(g)⇌5N2(g)+ 6H2O( g) ,减小压强,产生的影响是 ( )
A.正反应速率增大,逆反应速率减小
B.正反应速率减小,逆反应速率增大
C.正、逆反应速率都减小
D.正、逆反应速率都增大
-
对已达到平衡的反应4NH3(g)+6NO(g)⇌5N2(g)+6H2O( g) 减小压强,产生的影响是
A.正、逆反应速率都减小,平衡向正反应方向移动
B.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
D.正、逆反应速率都增大,平衡不发生移动
-
(2012•惠州模拟)已知:4NH3(g) + 5O2(g) ═ 4NO(g) + 6H2O(g) , △H=﹣1025kJ/mol,该反应是一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是( )

-
已知4NH3 +5 O2 =4NO + 6H2O ,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)、表正确的关系是
A.4/5v(NH3) = v(O2)
B.5/6v(O2) = v(H2O)
C.2/3v(NH3) = v(H2O)
D.4/5 v(O2) = v(NO)
-
已知:4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g) ΔH=-1025 kJ/mol,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
4NO(g) + 6H2O(g) ΔH=-1025 kJ/mol,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
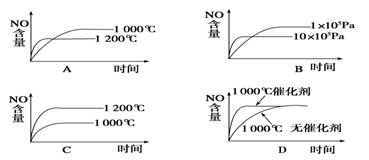
-
已知:4NH3(g) + 5O2(g) =4NO(g) + 6H2O(g),△H= —1025kJ/mol,该反应是一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是
A.
B.
C.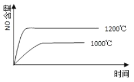
D.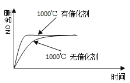
-
已知:4NH3(g) + 5O2(g) =4NO(g) + 6H2O(g),△H= —1025kJ/mol,该反应是一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是
A.
B.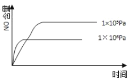
C.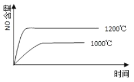
D.
5N2(g)+6H2O(l)△H1
2NO2(g) △H2(且|△H1|=2|△H2|)
5N2(g)+3O2(g)+6H2O(l)△H3
5N2(g)+6H2O(l)在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

2NO2(g);△H2说法正确的是__________。













