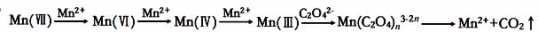-
某小组研究 Na2S 溶液与 KMnO4 溶液反应,探究过程如下。
资料:Ⅰ.MnO4 在强酸性条件下被还原为 Mn2+,在近中性条件下被还原为 MnO2.
Ⅱ.单质硫可溶于硫化钠溶液,溶液呈淡黄色。
(1)根据实验可知,Na2S 具有________性。
(2)甲同学预测实验I中S2-被氧化成 SO32-。
①根据实验现象,乙同学认为甲的预测不合理,理由是_______________。
②乙同学取实验Ⅰ中少量溶液进行实验,检测到有 SO42-,得出 S2-被氧化成 SO42-的结论,丙同学否定该结论,理由是_______________。
③同学们经讨论后,设计了如右下图的实验,证实该条件下 MnO4-的确可以将 S2-氧化成SO42-。
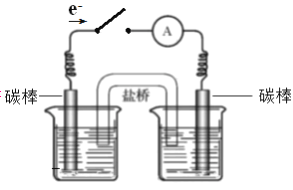
a.左侧烧杯中的溶液是__________。
b.连通后电流计指针偏转,一段时间后,_________(填操作和现象),证明S2-被氧化为SO42-。
(3)实验 I 的现象与资料 i 存在差异,其原因是新生成的产物(Mn2+)与过量的反应物(MnO4-)发生反应,该反应的离子方程式是______________。
(4)实验Ⅱ的现象与资料也不完全相符,丁同学猜想其原因与(3)相似,经验证猜想成立,他的实验方案_______。
(5)反思该实验,反应物相同,而现象不同,体现了物质变化不仅与其自身的性质有关,还与__________因素有关。
-
某小组研究Na2S溶液与KMnO4溶液反应,探究过程如下。

资料:ⅰ.  在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
ⅱ. 单质硫可溶于硫化钠溶液,溶液呈淡黄色。
(1)根据实验可知,Na2S具有________性。
(2)甲同学预测实验I中S2–被氧化成 。
。
①根据实验现象,乙同学认为甲的预测不合理,理由是________。
②乙同学取实验I中少量溶液进行实验,检测到有 ,得出S2–被氧化成
,得出S2–被氧化成 的结论,丙同学否定了该结论,理由是________。
的结论,丙同学否定了该结论,理由是________。
③同学们经讨论后,设计了如下实验,证实该条件下 的确可以将S2–氧化成
的确可以将S2–氧化成 。
。

a.右侧烧杯中的溶液是________。
b.连通后电流计指针偏转,一段时间后,________(填操作和现象)。
(3)实验I的现象与资料i存在差异,其原因是新生成的产物(Mn2+)与过量的反应物( )发生反应,该反应的离子方程式是________。
)发生反应,该反应的离子方程式是________。
(4)实验II的现象与资料也不完全相符,丁同学猜想其原因与(3)相似,经验证猜想成立,他的实验方案是______。
(5)反思该实验,反应物相同,而现象不同,体现了物质变化不仅与其自身的性质有关,还与________因素有关。
-
某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液的用量均为2mL.
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 催化剂的用量/g | KMnO4酸性溶液的浓度/mol•L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响;
(Ⅱ)实验①和______探究温度对该反应速率的影响;
(Ⅲ)实验①和______探究催化剂对该反应速率的影响;) |
| ② | ______ | ______ | ______ |
| ③ | ______ | ______ | ______ |
| ④ | ______ | ______ | ______ |
(2)某同学对实验①和②分别进行三次实验,测得以下实验数据(从混合振荡均匀开始计时):
KMnO4酸性溶液
的浓度/mol•L-1 | 溶液褪色所需时间 t/min |
| 第1次 | 第2次 | 第3次 |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
计算用0.001mol•L-1 KMnO4酸性溶液进行实验时KMnO4的平均反应速率______(忽略混合前后溶液的体积变化,写出计算过程).
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?______.若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案:______.
-
某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液的用量均为2mL.
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 催化剂的用量/g | KMnO4酸性溶液的浓度/mol•L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响;
(Ⅱ)实验①和______探究温度对该反应速率的影响;
(Ⅲ)实验①和______探究催化剂对该反应速率的影响;) |
| ② | ______ | ______ | ______ |
| ③ | ______ | ______ | ______ |
| ④ | ______ | ______ | ______ |
(2)某同学对实验①和②分别进行三次实验,测得以下实验数据(从混合振荡均匀开始计时):
KMnO4酸性溶液
的浓度/mol•L-1 | 溶液褪色所需时间 t/min |
| 第1次 | 第2次 | 第3次 |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
计算用0.001mol•L-1 KMnO4酸性溶液进行实验时KMnO4的平均反应速率______(忽略混合前后溶液的体积变化,写出计算过程).
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?______.若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案:______.
-
草酸 溶液与酸性
溶液与酸性 溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
(查阅资料) 溶液氧化
溶液氧化 的反应历程为:
的反应历程为:

(提出假设)假设1:该反应为放热
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是______。
(设计、完成实验)
 称取______g草酸晶体
称取______g草酸晶体 ,配置500mL
,配置500mL
 溶液。
溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和______。
②下列操作会使所配溶液浓度偏低的是______ 填下列选项的字母序号
填下列选项的字母序号 。
。
A 称取草酸晶体时,将草酸晶体放在托盘天平右盘
B 定容时俯视刻度线
C 将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D 摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
 完成探究,记录数据
完成探究,记录数据
| 实验 编号 | 烧杯中所加试剂及用量 | 控制条件 | 溶液褪 色时间 
|
| 
 溶液 溶液
| 等浓度  溶液 溶液
| 
| 
稀硫酸 |
| 1 | 30 | 20 | 30 | 20 | | 18 |
| 2 | 30 | 20 | 30 | 20 | 水浴控制温度 | 15 |
| 3 | 30 | 20 | 30 | 20 | 加入少量 固体 固体 | 
|
| 4 | 30 | 20 | x | 20 | 加入5mL  溶液 溶液
| 18 |
则 ______,假设______成立。
______,假设______成立。
 由于
由于 能氧化水中有机物等因素,配置好稳定的
能氧化水中有机物等因素,配置好稳定的 溶液,其浓度需标定.取
溶液,其浓度需标定.取

 溶液于锥形瓶中,加入10mL
溶液于锥形瓶中,加入10mL 稀硫酸,用
稀硫酸,用 中
中 溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗
溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗 溶液
溶液 ,则草酸溶液与酸性
,则草酸溶液与酸性 溶液反应的离子方程式为:______,上述实验中
溶液反应的离子方程式为:______,上述实验中 溶液的物质的量浓度为______。
溶液的物质的量浓度为______。
-
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)

已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g。
实验流程:
①往装置A中加入2.7mL(2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL苯甲酸溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示。
| 第一次 | 第二次 | 第三次 | 第四次 |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
请回答:
(1)装置A的名称 。若不用温度计,本实验控制反应温度的措施为 。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为____ 。
(3)操作②中趁热过滤的目的是 ,操作I的名称 。
(4)步骤③中用到的定量仪器有分析天平, ,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为 。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果将 (填“偏大”、“偏小”或“不变”)。
-
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)

已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g。
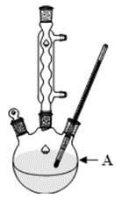
实验流程:
①往装置A中加入2.7mL(2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL,甲醇溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示列举:
| 第一次 | 第二次 | 第三次 | 第四次 |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
请回答:
(1)装置A的名称________________________________________________________________________ 。若不用温度计,本实验控制反应温度的措施为________________________________________________________________________。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为________________________________________________________________________________________________ 。
(3)操作I的名称________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
(4)步骤③中用到的定量仪器有________________________________________________________________________________________________________________________ ,100mL容量瓶,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为 ________________________________________________________________________________________________________________________________________________________________________。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果________________________ ________________________________________(填“偏大”、“偏小”或“不变”)。
-
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)

已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 go。

实验流程:
①往装置A中加入2.7mL (2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL、甲醇溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示列举

请回答:
(1)装置A的名称 。若不用温度计,本实验控制反应温度的措施为 。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为____ 。
(3)操作I的名称 。
(4)步骤③中用到的定量仪器有 ,100mL容量瓶,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为 。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果 (填“偏大”、“偏小”或“不变”)。
-
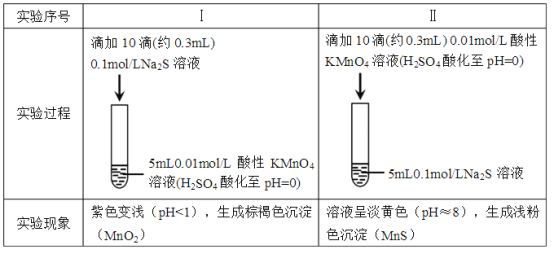
某小组研究Na2S 溶液与KMnO4溶液反应,探究过程如下
| 实验序号 | I | II |
| 实验过程 | 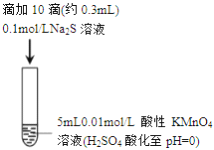
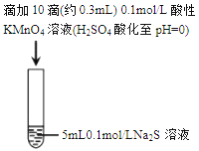
| 
|
| 实验现象 | 紫色变浅(pH 1),生成棕褐色沉淀(MnO2) 1),生成棕褐色沉淀(MnO2) | 溶液呈淡黄色(pH 8),生成浅粉色沉淀(MnS) 8),生成浅粉色沉淀(MnS) |
资料: i.MnO4-在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2
ii.单质硫可溶于硫化钠溶液,溶液呈淡黄色。
下列说法正确的是
A. 根据实验可知,Na2S被还原
B. 取实验I中少量溶液进行实验,检测到有SO42-,得出S2-被氧化成SO42-
C. 实验I中反应离子方程式: 2MnO4-+3Mn2++2H2O=5MnO2↓+4H+
D. 实验II 中反应结束后溶液呈淡黄色,有MnO2生成
-
草酸(H2C2O4)溶液与酸性KMnO4溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为:
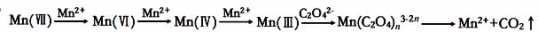
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是 。
【设计、完成实验】
(1)称取 g草酸晶体(H2C2O4·2H2O),配置500mL 0.10mol/L H2C2O4溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和 。
②下列操作会使所配溶液浓度偏低的是 (填下列选项的字母序号)。
A.称取草酸晶体时,将草酸晶体放在托盘天平右盘
B.定容时俯视刻度线
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
(2)完成探究,记录数据
| 实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s) |
| 0.10mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50mol/L 稀硫酸 |
| 1 | 30 | 20 | 30 | 20 | | 18 |
| 2 | 30 | 20 | 30 | 20 | 水浴控制温度65℃ | 15 |
| 3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
| 4 | 30 | 20 | x | 20 | 加入5mL 0.10mol/L K2SO4溶液 | 18 |
| | | | | | |
则x = ,假设2成立。
(3)由于KMnO4能氧化水中有机物等因素,为配制好稳定的KMnO4溶液,其浓度需标定。取10.00 mL 0.10mol/L H2C2O4溶液于锥形瓶中,加入10mL 0.50mol/L稀硫酸,用(2)中KMnO4溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液40.00 mL,则草酸溶液与酸性KMnO4溶液反应的离子方程式为 。上述实验中KMnO4溶液的物质的量浓度为 。

在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
。
,得出S2–被氧化成
的结论,丙同学否定了该结论,理由是________。
的确可以将S2–氧化成
。

)发生反应,该反应的离子方程式是________。