-
肼(N2H4)是一种高能燃料,在生产和研究中用途广泛。化学小组同学在实验室中用过量NH3和NaC1O溶液反应制取N2H4(液)并探究其性质。回答下列问题:
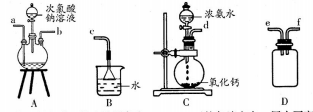
(1)肼的制备
①用上图装置制取肼,其连接顺序为________(按气流方向,用小写字母表示)。
②装置A中发生反应的化学方程式为_________________,装置D的作用是_______________。
(2)探究:N2H4和AgNO3溶液的反应将制得的肼分离提纯后,进行如下实验:
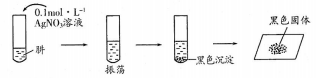
证明黑色沉淀已洗涤干净的操作是__________________________________。
【查阅资料】N2H4水溶液的碱性弱于氨水;N2H4有强还原性。AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水。
【提出假设】
假设1:黑色固体可能是Ag;
假设2:黑色固体可能是_____________;
假设3:黑色固体可能是Ag和Ag2O。
【实验验证】该同学基于上述假设,设计如下方案,进行实验,请完成下表中的空白部分。
| 实验编号 | 操作 | 现象 | 实验结论 |
| 1 | 取少量黑色固体于试管,__________ | 黑色固体不溶解 | 假设1成立 |
| 2 | 操作同实验1 | 黑色固体完全溶解 | 假设2成立 |
| 3 | ①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热②取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ①________________ ②________________ | 假设3成立 |
根据实验现象,假设1成立,则N2H4与AgNO3溶液反应的离子方程式为____________。
-
肼( N2H4)是一种高能燃料,在工业生产中用途广泛。
(1)0.5mol肼中含有__________ mol极性共价键。
(2) 肼的性质与氨气相似,易溶于水,有如下反应过程:
N2H4+H2O N2H4·H2O
N2H4·H2O N2H5++OH-
N2H5++OH-
①常温下,某浓度N2H5C1溶液的pH为5,则该溶液中由水电离产生的c(H+)为______mol/L。
②常温下,0.2mol/L N3H4溶液0.1mol/L HCL溶液等体积混合,混合溶液的pH>7,
则溶液中v(N2H5+)________v(N2H4·H2O)(填“>”、“<”或“=”)。
(3)工业上可用肼(N2H4)与新制Cu(OH)2反应制备纳米级Cu2O,同时放出N2,该反应的化学方程式为______________________________________。
(4)发射火箭时,肼为燃料,双氧水为氧化剂,两者反应成氮气与水蒸气。已知1.6g液态肼在上述反应中放出64.22kJ的热量,写出该反应的热化学方程式___________________。
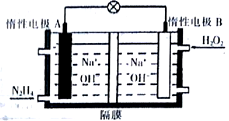
(5)肼-双氧水燃料电池由于其较高的能量密度而广受关注,其工作原理如图所示。则电池正极反应式为_______________,电池工作过程中,A极区溶液的pH____________(填“增大”“减小”或“不变”)
-
肼(N2H4,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
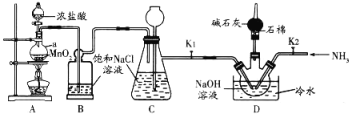
已知:Cl2(g)+2NaOH(aq)=NaC1O(aq)+NaC1(aq)+H2O(g) △H<0。当温度超过40℃时,Cl2与NaOH溶液反应生成NaClO3。回答下列问题:
(1)仪器a的名称是________________,装置B的作用是____________________________。
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是________________。
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭K1。此时装置C的作用是________________________________。
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开K2,通入NH3,使其与NaC1O溶液反应制取肼。理论上通入三颈烧瓶的Cl2和NH3的最佳物质的量之比为______________。
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性____________(说明操作、现象和结论)。
①淀粉-KI溶液 ②稀硫酸(酚酞) ③NaHCO3 ④AgC1
-
氮化铝(AIN)是一种新型无机材料,广泛应用于集成电路生产领域。某化学研究小组利用氮气、氧化铝和活性炭制取氮化铝,设计下图实验装置。
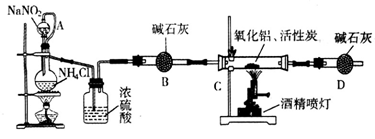
试回答:
(1)实验中用饱和NaNO2与 NH4C溶液制取氮气的化学方程式为________。
(2)装置中分液漏斗与蒸馏烧瓶之间的导管A的作用是________(填写序号)。
a.防止NaNO2 饱和溶液蒸发 b.保证实验装置不漏气 c.使NaNO2 饱和溶液容易滴下
(3)按图连接好实验装置,检查装置气密性的方法是________。
(4)化学研究小组的装置存在严重问题,请说明改进的办法________。
(5)反应结束后,某同学用下图装置进行实验来测定氮化铝样品的质量分数(实验中导管体积忽略不计)。已知:氮化铝和NaOH溶液反应生成Na[Al(OH)4]和氨气
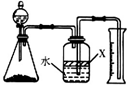 。
。
①广口瓶中的试剂X最好选用________(填写序号)。
a.汽油 b.酒精 c.植物油 d.CCl4
②广口瓶中的液体没有装满(上方留有空间),则实验测得NH3的体积将________(填“偏大”、“偏小”、“不变”)。
③若实验中称取氮化铝样品的质量为10.0g,测得氨气的体积为3.36L(标准状况),则样品中AlN的质量分数为________。
-
氮化铝(AIN)是一种新型无机材料,广泛应用于集成电路生产领域。某化学研究小组利用氮气、氧化铝和活性炭制取氮化铝,设计下图实验装置。
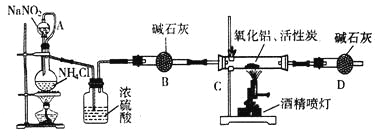
试回答:
(1)实验中用饱和NaNO2与 NH4Cl溶液制取氮气的化学方程式为_____________。
(2)装置中分液漏斗与蒸馏烧瓶之间的导管A的作用是__________(填写序号)。
a.防止NaNO2饱和溶液蒸发 b.保证实验装置不漏气 c.使NaNO2饱和溶液容易滴下
(3)按图连接好实验装置,检查装置气密性的方法是__________________________。
(4)化学研究小组的装置存在严重问题,请说明改进的办法_____________________。
(5)反应结束后,某同学用下图装置进行实验来测定氮化铝样品的质量分数(实验中导管体积忽略不计)。已知:氮化铝和NaOH溶液反应生成Na[Al(OH)4]和氨气
 。
。
①广口瓶中的试剂X最好选用_______(填写序号)。
a.汽油 b.酒精 c.植物油 d.CCl4
②广口瓶中的液体没有装满(上方留有空间),则实验测得NH3的体积将____(填“偏大”、“偏小”、“不变”)。
③若实验中称取氮化铝样品的质量为10.0g,测得氨气的体积为3.36L(标准状况),则样品中AlN的质量分数为___________。
-
氮及其化合物在生产、生活中有极其重要的作用。
(1)我国长征系列运载火箭用肼(N2H4)作燃料。N2H4与NH3有相似的化学性质。
①写出肼与盐酸反应的离子方程式:____________。
②在火箭推进器中装有液态肼和双氧水,当它们混合时迅速反应生成氮气和水蒸气,写出反应的化学方程式:_ 。
③火箭发射时以肼为燃料,也可以用一氧化氮作氧化剂,反应过程中若转移2 mol电子, 则消耗燃料肼的质量为_ 。
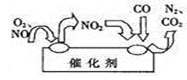
(2)汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,为了 减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。写出写出净化过程中总反应的化学方程式:_ 。
-
氮及其化合物在生产、生活中有极其重要的作用。
(1)我国长征系列运载火箭用肼(N2H4)作燃料。N2H4与NH3有相似的化学性质。
①写出肼与盐酸反应的离子方程式:_______________。
②在火箭推进剂中装有液态肼和双氧水,当它们混合时迅速反应生成氮气和水蒸气,写出反应的化学方程式:______________。
③火箭发射时以肼为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为__________。
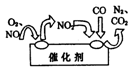
(2)汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。写出净化过程中总反应的化学方程式:_______________。
-
氨的化合物在生产、生活中广泛存在。
(1)我国长征系列运载火箭用肼(N2H4)作燃料。N2H4与NH3有相似的化学性质。
①写出肼与盐酸反应的离子方程式:_______________________________。
②在火箭推进器中装有液态肼和双氧水,当它们混合时迅速反应生成氮气和水蒸气,写出反应的化学方程式:_____________________________________。
③火箭发射时以肼为燃料,也可以用一氧化氮作氧化剂,反应过程中若转移2mol电子则消耗燃料肼的质量为______________。
(2)汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。

写出净化过程中总反应的化学方程式____________________。
-
肼是一种强还原剂,用NaClO与NH3反应可用于生产肼(N2H4),其反应的化学方程式为:NaClO+2NH3= N2H4+NaCl+H2O。
⑴生产1000 g质量分数为25.6%的肼溶液最少需要___________L(标准状况)NH3。
⑵工业次氯酸钠溶液中含有氯酸钠会影响所得肼的产品质量。测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原(ClO3-在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点(Cr2O72-被还原为Cr3+),消耗该溶液20.00 mL。
①用H2O2与次氯酸钠反应的离子方程式为___________。
②实验中加热煮沸的目的是___________。
③计算样品中NaClO3的含量(以g·L-1表示),写出计算过程。___________
-
肼是一种强还原剂,用NaClO与NH3反应可用于生产肼(N2H4),其反应的化学方程式为:NaClO+2NH3= N2H4+NaCl+H2O。
⑴生产1000 g质量分数为25.6%的肼溶液最少需要___________L(标准状况)NH3。
⑵工业次氯酸钠溶液中含有氯酸钠会影响所得肼的产品质量。测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原(ClO3-在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点(Cr2O72-被还原为Cr3+),消耗该溶液20.00 mL。
①用H2O2与次氯酸钠反应的离子方程式为___________。
②实验中加热煮沸的目的是___________。
③计算样品中NaClO3的含量(以g·L-1表示),写出计算过程。___________





 。
。
 。
。

