-
肼( N2H4)是一种高能燃料,在工业生产中用途广泛。
(1)0.5mol肼中含有__________ mol极性共价键。
(2) 肼的性质与氨气相似,易溶于水,有如下反应过程:
N2H4+H2O N2H4·H2O
N2H4·H2O N2H5++OH-
N2H5++OH-
①常温下,某浓度N2H5C1溶液的pH为5,则该溶液中由水电离产生的c(H+)为______mol/L。
②常温下,0.2mol/L N3H4溶液0.1mol/L HCL溶液等体积混合,混合溶液的pH>7,
则溶液中v(N2H5+)________v(N2H4·H2O)(填“>”、“<”或“=”)。
(3)工业上可用肼(N2H4)与新制Cu(OH)2反应制备纳米级Cu2O,同时放出N2,该反应的化学方程式为______________________________________。
(4)发射火箭时,肼为燃料,双氧水为氧化剂,两者反应成氮气与水蒸气。已知1.6g液态肼在上述反应中放出64.22kJ的热量,写出该反应的热化学方程式___________________。
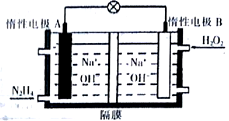
(5)肼-双氧水燃料电池由于其较高的能量密度而广受关注,其工作原理如图所示。则电池正极反应式为_______________,电池工作过程中,A极区溶液的pH____________(填“增大”“减小”或“不变”)
-
肼(N2H4)是一种高能燃料,在生产和研究中用途广泛。化学小组同学在实验室中用过量NH3和NaC1O溶液反应制取N2H4(液)并探究其性质。回答下列问题:
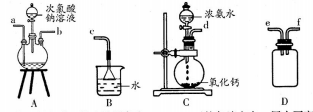
(1)肼的制备
①用上图装置制取肼,其连接顺序为________(按气流方向,用小写字母表示)。
②装置A中发生反应的化学方程式为_________________,装置D的作用是_______________。
(2)探究:N2H4和AgNO3溶液的反应将制得的肼分离提纯后,进行如下实验:
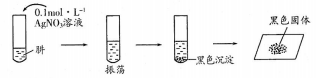
证明黑色沉淀已洗涤干净的操作是__________________________________。
【查阅资料】N2H4水溶液的碱性弱于氨水;N2H4有强还原性。AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水。
【提出假设】
假设1:黑色固体可能是Ag;
假设2:黑色固体可能是_____________;
假设3:黑色固体可能是Ag和Ag2O。
【实验验证】该同学基于上述假设,设计如下方案,进行实验,请完成下表中的空白部分。
| 实验编号 | 操作 | 现象 | 实验结论 |
| 1 | 取少量黑色固体于试管,__________ | 黑色固体不溶解 | 假设1成立 |
| 2 | 操作同实验1 | 黑色固体完全溶解 | 假设2成立 |
| 3 | ①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热②取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ①________________ ②________________ | 假设3成立 |
根据实验现象,假设1成立,则N2H4与AgNO3溶液反应的离子方程式为____________。
-
乌洛托品在工业生产中有广泛用途,其结构式如图所示。下列说法正确的是
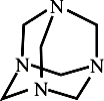
A.化学式为C6H12N4,属于饱和烃
B.不能发生加成反应,一氯取代产物有3种
C.分子中既含极性共价键又含非极性共价键
D.可由甲醛(HCHO)与氨气按物质的量之比3∶2完全反应制得
-
硼烷是一种潜在的高能燃料,工业制取可用反应: ,下列有关说法正确的是
,下列有关说法正确的是
A.该反应中氢气做还原剂,铝做氧化剂
B.在空气中 比
比  更稳定
更稳定
C. 中存在极性键、非极性键、离子键
中存在极性键、非极性键、离子键
D.每生成1mol  要消耗
要消耗
-
(17分)氮及其化合物在工业生产和科技等领域有广泛应用。
(1)肼(N2H4)常用于火箭或原电池的燃料。已知:(i)N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol
(ii)N2H4(g)+ O2(g) N2(g)+2H2O(g) ΔH=-534kJ/mol
N2(g)+2H2O(g) ΔH=-534kJ/mol
(iii)H2O(g)= H2O(1) ΔH=-44kJ/mol
①反应2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l) ΔH =_______kJ·mol-1
②一定温度下,将N2H4与NO2以体积比1:1置于10 L密闭容器中发生反应2N2H4(g)+ 2NO2(g) 3N2(g)+4H2O(1),下列不能说明反应达到平衡状态的是_______。(填序号)
3N2(g)+4H2O(1),下列不能说明反应达到平衡状态的是_______。(填序号)
a.混合气体密度保持不变 b.混合气体颜色保持不变
c.N2H4与NO2体积比保持不变 d.体系压强保持不变
③在10 L的密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:

前2min内NO2的平均反应速率为___________。平衡时NO2的转化率________;该温度下反应的平衡常数K=_________。
反应在第6min时改变了条件,改变的条件可能是__________。(填序号)
a.使用催化剂 b.升高温度 c.减小压强 d.增加NO2的量
(2)HNO3和As2S3能发生反应:As2S3+10HNO3==2H3AsO4+3S+10NO2↑+2H2O,反应中被氧化的元素为_________。
若该反应中转移电子的物质的量为5 mol时,产物中的S经过转化全部生成浓H2SO4,然后与足量的铜在加热条件下反应消耗铜的量_________。(填序号)
a.小于0.75 mol b.等于0.75mol c.大于0.75mol d.无法确定
-
肼(N2H4)又称联氨,广泛用于火箭推进剂、化工原料及燃料电池等方面。请回答下列问题:
(1)肼是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键能如下:
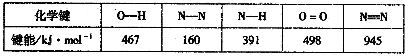
①N2H4中氮元素的化合价为__________。
②气态N2H4在氧气中燃烧的热化学方程式为__________。
(2)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液,该反应的离子方程式为__________。
(3)肼燃料电池原理如图所示,左边电极上发生反应的电极反应式为__________.
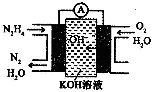
(4)盐酸肼(N2H6Cl2)是一种化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4 Cl类似,但分步水解。
①写出盐酸肼第一步水解的离子方程式__________。
②盐酸肼水溶液中离子浓度的关系为__________ (填序号)。
A.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
B.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
C.c(N2H62+)+ c([N2H5·H2O+]) +c(H+)= c(Cl-)+c(OH-)
(5〕常温下,将0.2 mol/L盐酸与0.2 mol/L肼的溶液等体积混合(忽略混合后溶液体积变化〕。若测定混合液的pH=6,混合液中水电离出的H+与0.1mol/L盐酸中水电离出的H+浓度之比为__________。
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1 mol NaHSO4熔融或溶于水时电离出的离子总数均为3NA
B. 17 g H2O2含有0.5NA个非极性共价键
C. 在1L0.5mol/LH2SO4溶液中,含有的氧原子数为2NA
D. 标准状况下,22.4 L Cl2溶于水转移的电子数为NA
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1 mol NaHSO4熔融或溶于水时电离出的离子总数均为3NA
B. 17 g H2O2含有0.5NA个非极性共价键
C. 在1L0.5mol/LH2SO4溶液中,含有的氧原子数为2NA
D. 标准状况下,22.4 L Cl2溶于水转移的电子数为NA
-
设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 1mol NaHSO4熔融或溶于水时电离出的离子总数均为3NA
B. 17g H2O2含有0.5NA个非极性共价键
C. 1L 0.1mol/L 稀硝酸与足量金属铝反应,生成NO2的分子个数为0.5NA
D. 标准状况下,22.4L Cl2溶于水转移的电子数为NA
-
Ⅰ、火箭升空需要高能的燃料,通常用肼(N2H4)作为燃料,N2O4做氧化剂。
(1)已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g) N2O4(g) △H=-52.7kJ·mol-1
N2O4(g) △H=-52.7kJ·mol-1
试写出气态肼在四氧化二氮气体中燃烧生成氮气和气态水的热化学方程式:______________________。
(2)工业上可用次氯酸钠与过量的氨反应制备肼,该反应的氧化剂和还原剂的物质的量之比为__________________。
(3)工业上常用氨水调节溶液pH除去金属离子,常温下Cr(OH)3的溶度积Ksp=10-32,要使Cr3+浓度降至10-5mol/L,溶液pH应调至____________________
II、在130℃和180℃时,分别将0.50molCH4和a mol NO2充入1L的密闭容器中发生反应:CH4(g)+2NO2(g)  N2(g)+CO2(g)+2H2O(g) △H<0,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) △H<0,测得有关数据如下表:
| 实验编号 | 温度 | | 0min | 10min | 20min | 40min | 50min |
| 1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | | 0.15 |
(4)180℃时达到平衡状态时,CH4的平衡转化率为___________________。
(5)己知130℃时该反应的化学平衡常数为6.4,试计算a=__________。
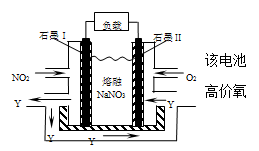
(6)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图。在使用过程中石墨I电极上生成氧化物Y (Y为氮元素最高价化化物),该电极反应为_________________。
N2H4·H2O
N2H5++OH-







