-
某学生在0.1mol/LNaHCO3溶液中滴加酚酞溶液1滴,整个溶液几乎没有什么变化,但溶液加热后,显明显淡红色,加热较长时间后冷却,红色不褪去。
该学生为了了解该过程的原因,进行了下列探究过程:
【实验探究】
实验1: 加热0.1mol/LNaHCO3溶液,测得溶液pH变化如下表
温度(℃)
10
20
30
50
70
80
100
pH
8.3
8.4
8.5
8.9
9.4
9.6
10.1
实验2:10℃时,在烧杯中加入0.1mol/LNaHCO3溶液200mL,测得该溶液pH=8.3,加热到100℃,测得pH=10.2,恢复到10℃,pH=9.8。
实验3:加热0.1mol/LNaHCO3溶液,将产生的气体通入澄清石灰水,溶液变浑浊。
实验4:
①配制0.1mol/LNaHCO3溶液和0.1mol/LNa2CO3溶液各200mL,10℃时,分别测得NaHCO3溶液pH=8.3,Na2CO3溶液pH=11.5。
②加热蒸发0.1mol/L NaHCO3溶液200mL,至溶液体积100mL,停止加热,加水至200mL,冷却至原温度,测得溶液pH=9.8。
③将0.1mol/L NaHCO3溶液200mL敞口放置三天,再加水至200mL,测得溶液pH=10.1。
请根据上述实验回答下列问题:
(1)用离子方程式表示0.1mol/LNaHCO3溶液中存在的平衡(除水电离平衡外)___________
________________、_______________________________。这两个平衡以_______________
为主,理由是_______________________________.
(1)实验3得到的结论是__________________________________________________。
(1)结合实验2、3分析,加热0.1mol/LNaHCO3溶液,pH增大的原因可能是_____________
__________、______________________、________________________________。
(1)实验4①得到的结论是_______________________________________________。
(1)实验4②“加水至200mL”的目的是____________________________________________。
实验4③可以得到的结论是_______________________________________。
(1)要确定NaHCO3溶液加热后pH增大的主要原因还需要解决的问题是________________。
高三化学实验题极难题查看答案及解析
-
某学生做麦芽糖的还原性实验,取2mL 0.5mol•L-1的CuSO4溶液和2mL 0.5mol•L-1的NaOH溶液,将它们混合后,滴入2.0mL的10%麦芽糖溶液,加热煮沸,结果没有看到红色沉淀生成,这是因为( )
A.麦芽糖溶液太浓
B.加热时间不够
C.CuSO4溶液不够量
D.NaOH溶液不够量高三化学选择题中等难度题查看答案及解析
-
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 NaHCO3溶液中:NH
、H+、NO
、SO
B.使酚酞变红色的溶液中:Mg2+、Fe2+、NO
、Cl-
C.0.1 mol·L-1 FeCl3溶液中:K+、Na+、Br-、SCN-
D.c(H+)=1×10-4 mol·L-1的溶液中:K+、Cu2+、Cl-、SO
高三化学单选题简单题查看答案及解析
-
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 NaHCO3溶液中:NH
、H+、NO
、SO
B.使酚酞变红色的溶液中:Mg2+、Fe2+、NO
、Cl-
C.0.1 mol·L-1 FeCl3溶液中:K+、Na+、Br-、SCN-
D.c(H+)=1×10-4 mol·L-1的溶液中:K+、Cu2+、Cl-、SO
高三化学单选题简单题查看答案及解析
-
下列有关电解质溶液的说法正确的是( )
A.常温下,0.1mol/LNa2S溶液中存在:c(OH﹣)=c(H+)+c(HS﹣)+c(H2S)
B.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:C(Na+)>c(CO32﹣)>c(HCO3﹣ )>c(OH﹣)>c(H+)
C.pH相同的①CH3 COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
D.向0.1mol•L﹣1的氨水中加入少量硫酸铵固体,则溶液中
增大
高三化学选择题困难题查看答案及解析
-
常温下,下列说法正确的是
A.0.1mol/LNaHCO3溶液中:c(H+)+2c(H2CO3)=c(CO32-)+c(OH-)
B.0.1mol/LHCN和0.1mol/L NaCN的等体积混合溶液中:c(HCN)>c(Na+)>c(CN-)>c(H+)>c(OH-)
C.0.1mol/LNa2C2O4溶液滴加HCl溶液至c(H2C2O4)=c(HC2O4-):3c(H2C2O4)>c(OH-)+c(Cl-)
D.0.1mol/LNH4HSO4溶液滴加NaOH溶液至pH=7:c(Na+)=c(NH4+)+2c(NH3·H2O)>c(SO42-)
高三化学单选题困难题查看答案及解析
-
室温下,下列溶液中粒子浓度大小关系正确的是
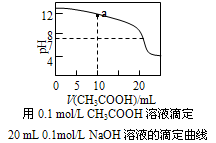
A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
B.pH相同的①CH3COONa②NaHCO3③NaAlO2三份溶液中的c(Na+):②>③>①
C.0.1mol•L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
D.上图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
高三化学选择题极难题查看答案及解析
-
室温下,下列溶液中粒子浓度大小关系正确的是
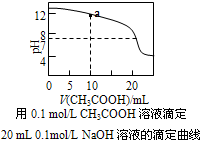
A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
B.pH相同的①CH3COONa②NaHCO3③NaAlO2三份溶液中的c(Na+):②>③>①
C.0.1mol•L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
D.上图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
高三化学选择题极难题查看答案及解析
-
下列溶液中粒子的物质的量浓度关系正确的是
A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
B.20ml0.1mol/LCH3COONa溶液与10ml0.1mol/LHCl溶液混合后呈酸性,所得溶液中:
c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:
c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
c(OH-)>c(H+)+c(CH3COOH)
高三化学选择题中等难度题查看答案及解析
-
下列溶液中粒子的物质的量浓度关系正确的是
A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
B.20mL0.1mol/LCH3COONa溶液与10mL0.1mol/LHCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:
c(Cl-)+c(H+)>c(NH4+)+c(OH-)
D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
c(OH-)>c(H+)+c(CH3COOH)
高三化学选择题困难题查看答案及解析