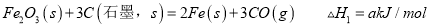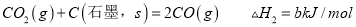-
(14分)研究CO2的利用对促进低碳社会的构建具有重要的意义。
⑴ 在一定体积的密闭容器中,进行化学反应: CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:

①该反应正向反应是________反应。(填“放热”或“吸热”)
②能判断该反应达到化学平衡状态的依据是________。
A.容器压强不变 B.混合气体中c(CO2)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
③当其他条件不变时,若缩小容器的体积,该反应平衡________移动。(选填“正向”、“逆向”或“不”)
⑵工业上合成甲醇可在密闭容器中采用如下反应进行:
CO2(g) +3H2(g)  CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1
CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1
①该反应的平衡常数表达式K=________。
②某实验将1molCO2和3molH2充入一定体积的密闭容器中,在两种不同条件下发生反应(只有一种条件不同)。测得CH3OH的物质的量随时间变化如图所示:

曲线I、Ⅱ对应的平衡常数大小关系为KⅠ________KⅡ(选填“>”、“=”或“<”)。
③一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
经测定甲容器经过5min达到平衡,平衡时CO2的转化率为50%,甲容器中该反应在5min内的平均速率υ(H2)=________mol·L-1·min-1。
要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为________。
-
综合利用CO2、CO对构建低碳社会有重要意义。
(1)利用H2 和CO在一定条件下发生如下反应:CO(g) +2H2(g) CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
①10min后达到平衡时CO的浓度为 ;
②10min内用H2表示的平均反应速率为 ;
③若要加快CH3OH的生成速率,可采取的措施有 (填一种合理的措施)
(2)利用H2 和CO2在一定条件下可以合成乙烯:6H2+2CO2 CH2=CH2+4H2O
CH2=CH2+4H2O
①已知:4.4gCO2与H2完全转化为CH2=CH2和水(气态)共放出6.39kJ的热量,写出该反应的热化学方程式 。
②不同温度对CO2的转化率及催化剂的催化效率的影响如图甲所示。
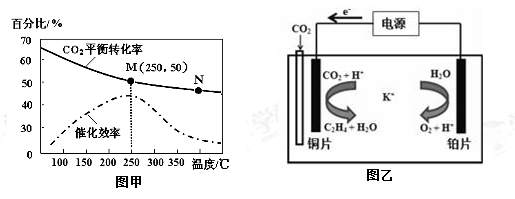
下列有关说法不正确的是 (填序号)。
a.不同条件下反应,N点的速率最大
b.温度在约250℃时,催化剂的催化效率最高
c.相同条件下,乙烯的产量M点比N高
③若在密闭容器中充入体积比为 3∶1的 H2和CO2,则图甲中M点时,产物CH2=CH2的体积分数为 。(保留两位有效数字)
(3)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图乙所示。在阴极上产生乙烯的电极反应方程式为 。
-
综合利用CO2、CO对构建低碳社会有重要意义。
(1)利用H2 和CO在一定条件下发生如下反应:CO(g)+2H2(g) CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
①10min后达到平衡时CO的浓度为 ;
②10min内用H2表示的平均反应速率为 ;
③若要加快CH3OH的生成速率,可采取的措施有 (填一种合理的措施)
(2)利用H2 和CO2在一定条件下可以合成乙烯:6H2+2CO2 CH2=CH2+4H2O
CH2=CH2+4H2O
①已知:4.4gCO2与H2完全转化为CH2=CH2和水(气态)共放出6.39kJ的热量,
写出该反应的热化学方程式 。
②不同温度对CO2的转化率及催化剂的催化效率的影响如图甲所示。
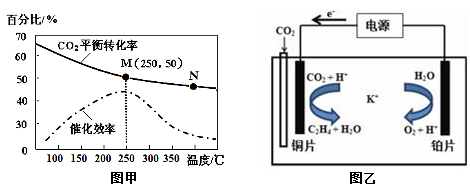
下列有关说法不正确的是 (填序号)。
A.不同条件下反应,N点的速率最大
B.温度在约250℃时,催化剂的催化效率最高
C.相同条件下,乙烯的产量M点比N高
③若在密闭容器中充入体积比为 3∶1的 H2和CO2,则图甲中M点时,产物CH2=CH2的体积分数为 。(保留两位有效数字)
(3)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图乙所示。在阴极上产生乙烯的电极反应方程式为 。
-
CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)金刚石和石墨燃烧反应中的能量变化如图a所示。

在通常状况下,金刚石和石墨中, (填“金刚石”或“石墨”)更稳定,石墨的燃烧热△H= kJ·mol-1。
(2)采用电化学法可将甲烷转化为二氧化碳,试写出以氢氧化钾水溶液作电解质时,该电池正极反应方程式 。
(3)CO2为原料还可合成多种物质。工业上常以CO2(g)与H2(g)为原料合成乙醇。①2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(l) 该反应物的总能量大于生成物的总能量,则该反应的△H= (填“>0”、“<0”、“=0”或“不能确定”)
CH3CH2OH(g)+3H2O(l) 该反应物的总能量大于生成物的总能量,则该反应的△H= (填“>0”、“<0”、“=0”或“不能确定”)
②下图是一种以烟道气为原料合成乙醇的工作原理示意图。
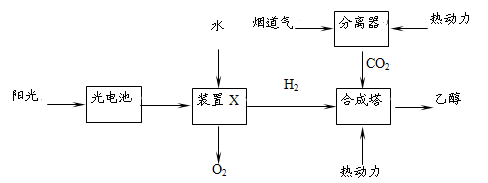
对上述流程的分析,下列说法正确的是 。
A.该流程至少包含4种形式的能量转化
B.流程设计体现了绿色化学思想
C.合成塔中生成乙醇的反应是化合反应
③图b所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。该电池负极的电极反应为 。
-
(13分)研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)已知石墨的标准燃烧热为y kJ·mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量,则石墨与氧气反应生成CO的热化学方程式为________________。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H
①该反应的平衡常数表达式为K=______________________。
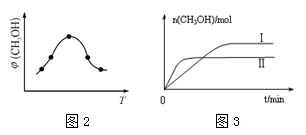
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的ΔH_______________(填“>” “<”或“=”)0。
③在两种不同温度下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ____________KⅡ(填“>” “<”或“=”)。
④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物 投入量 | 1molCO2 3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) (a、b、c均不等于0) |
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为________________。
-
研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)写出镁在CO2中燃烧的化学方程式为_________ _ ____。
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是__________。
②由MgO可制成“镁-次氯酸盐”燃料电池,其装置示意图如图1,该电池反应的离子方程式为 ____________________。
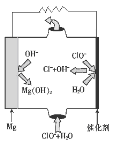
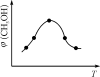
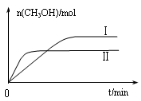
图1 图2 图3
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K=______________。
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的ΔH_______(填“>” “<”或“=”)0。
③在两种不同温度下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ________KⅡ(填“>” “<”或“=”)。
④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物 投入量 | 1molCO2 3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) (a、b、c均不等于0) |
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为____________。
-
CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)金刚石和石墨燃烧反应中的能量变化如图a所示。在通常状况下,金刚石和石墨中,__________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为__________。
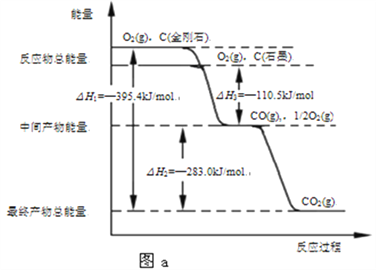
(2)采用电化学法可将二氧化碳转化为甲烷,试写出以氢氧化钾水溶液作电解质时,该转化的电极反应方程式__________________________________________。
(3)CO2为原料还可合成多种物质。工业上常以CO2(g)与H2(g)为原料合成乙醇。
①已知:H2O(l)=H2O(g) △H=+44kJ·mol-1
CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2kJ·mol-1
CO2(g)+H2(g) △H=-41.2kJ·mol-1
2CO(g)+4H2 (g)  CH3CH2OH(g)+H2O(g) △H= -256.1kJ·mol-1
CH3CH2OH(g)+H2O(g) △H= -256.1kJ·mol-1
则:2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(l) △H=___________________。
CH3CH2OH(g)+3H2O(l) △H=___________________。
②下图是一种以烟道气为原料合成乙醇的工作原理示意图。对上述流程的分析,下列说法正确的是_________。
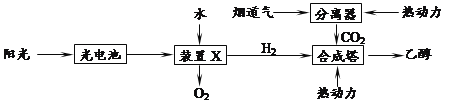
A.该流程至少包含4种形式的能量转化
B.装置X中阴极反应为:2H2O-4e-=4H++O2↑
C.合成塔中生成乙醇的反应是化合反应
D.流程设计体现了绿色化学思想
(4)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图b为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
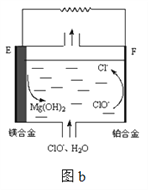
① E为该燃料电池的___________极(填“正”或“负”)。F电极上的电极反应式为___________。
② 镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因__________________________。
-
研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
①已知: 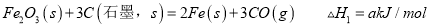
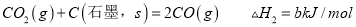
则CO还原Fe2O3(s)的热化学方程式为________________________________。
(2)常温下,用氨水吸收CO2可得到NH4HCO3溶液。已知常温下:NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11。在NH4HCO3溶液中,c(NH4+)______c(HCO3-)(填“>”“<”或“=”),计算反应NH4+ + HCO3- + H2O ⇌ NH3·H2O + H2CO3的平衡常数K=______________,物料守恒表达式为__________________________。
(3)以CO2为原料还可以合成多种物质。
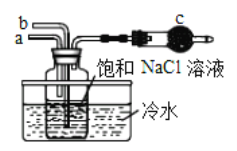
①如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。操作中先在_______处向饱和NaCl溶液中通入_________气体(填NH3或CO2),然后再在通入另一种气体。请写出反应的化学方程式_______________________。
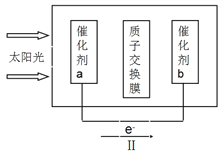
②人工光合作用能够借助太阳能用CO2和水制备化学原料,如图是通过人工光合作用制备HCOOH的原理示意图,请写出催化剂b处的电极反应式:____________________。
-
利用化学反应原理研究化学反应有重要意义。
(1)CO2的减排和综合利用是解决温室及能源问题的有效途径。一定温度下,在体积为1L的密闭容器中,充入1 molCO2和3molH2,此时压强为p0kpa,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
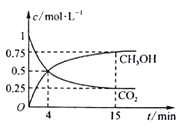
①0~4min,H2的平均反应速率v(H2)=__mol·L−1·min−1。
②下列能说明该反应已达到平衡状态的是___。
A.v正(CH3OH)=3v逆(H2)
B.CO2、H2、CH3OH和H2O浓度之比为1∶3∶1∶1
C.恒温恒容下,气体的密度不再变化
D.恒温恒压下,气体的体积不再变化
③测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L,则此时v(正)___v(逆)(填“>”“<”或“=”)。
④可逆反应的平衡常数可用平衡分压代替平衡浓度计算,已知:分压=总压×物质的量分数,则该温度下Kp=___kPa-2(用含有p0的式子表示,保留1位小数)。
(2)工业中,CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图所示。

图为温度对CO2平衡转化率及甲醇和CO产率的影响
①由图可知温度升高时CO的产率上升,其主要原因可能是___。
②由图可知获取CH3OH最适宜的温度是___。下列措施有利于提高CO2转化为CH3OH的平衡转化率的有___(填字母)。
A.使用对反应A选择性更高的催化剂
B.压缩体积
C.增大CO2和H2的初始投料比
(3)合成氨是人类科学技术上的一项重大突破,反应原理为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1。在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得合成氨反应达到平衡时的有关数据如下。
2NH3(g) ΔH=-92.4kJ·mol-1。在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得合成氨反应达到平衡时的有关数据如下。
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
则a+b___92.4(填“>”、“=”或“<”,下同),c3___2c1,2p2___p3,α1+α3___1。
-
研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
①已知:Fe2O3(s) + 3C(石墨) = 2Fe(s) + 3CO(g) △H 1 = +489.0 kJ·mol-1
C(石墨) +CO2(g) = 2CO(g) △H 2 = +173.0 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
②某含C、H、O三种元素的有机物A,经测定碳的质量分数为52.16%,氢的质量分数13.14%,它可以作燃料电池(以KOH溶液为电解液)的原料,写出该电池的负极反应式 。
(2)某实验将CO2和H2充入一定体积的密闭容器中,发生反应:
CO2(g) +3H2(g)  CH3OH(g) +H2O(g) △H =-49.0 kJ·mol-1
CH3OH(g) +H2O(g) △H =-49.0 kJ·mol-1
回答问题:
①该反应的平衡常数表达式为 。
②把0.5mol的CO2和1.5mol的H2充入2L的密闭容器中,半分钟后测得c(H2)=0.15mol/L,用CH3OH表示该反应的速率:v(CH3OH)=
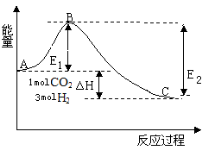
③如图,在反应体系中加入催化剂,反应速率增大,E2的变化是 (填“增大”, “减小”或“不变”)
CO(g)+H2O(g)
CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1