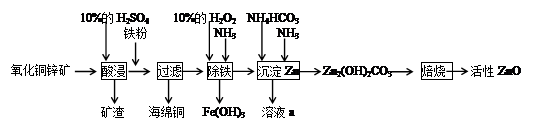-
利用铜—氯热化学循环可制取氢气,主要流程如下:
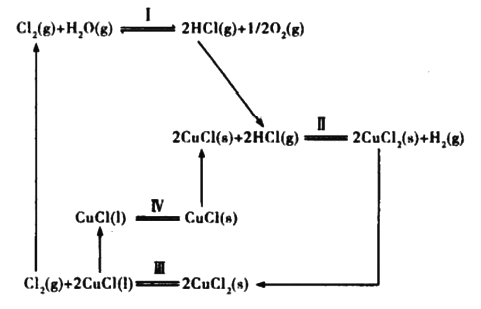
回答下列问题:
(1)图中属于氧化还原反应的是__________(填序号)。
(2)已知25℃时,Ksp(CuOH)=2.0×10-15,Ksp(CuC1)=1.0×10-6,则反应CuC1(s)+H2O(1) CuOH(s)+Cl-(aq)+H+(aq)的平衡常数K=___________(填数值)。
CuOH(s)+Cl-(aq)+H+(aq)的平衡常数K=___________(填数值)。
(3)已知:
Cl2(g)+H2O(g)==2HCl(g)+1/2O2(g) △H1
2CuCl(s)+2HCl(g)==2CuCl2(s)+H2(g) △H2
Cl2(g)+2CuCl(l)==2CuCl2(s) △H3
CuC1(l)==CuC1(s) △H4
则反应H2O(g)==H2(g)+1/2O2(g) △H=_______(用△H1、△H2、△H3、△H4表示)。
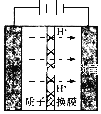
(4)反应Ⅱ若在水溶液中进行可用惰性电极电解实现,其装置如下图所示。阳极的电极反应式为____________________;电解过程中阳极周围溶液的pH__________(填“升高”或“降低”)。
(5)反应I是可逆反应,工业上也常用该反应生成的HC1制取氯气,反应为4HCl(g)+O2(g) 2Cl2(g)+2H2O(g),在不同起始投料比m下,HC1平衡转化率随温度的变化关系如下图所示:
2Cl2(g)+2H2O(g),在不同起始投料比m下,HC1平衡转化率随温度的变化关系如下图所示:
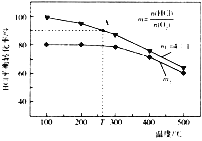
①该反应的正反应为___________热反应(填“放”或“吸”)。
②图中m2________m1(填“>”或“<”)。
③p kPa下,A点对应温度下反应的平衡常数Kp=________kPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,列出计算式即可)。
-
一种热化学循环流程如图所示。下列叙述正确的是

A. 图中循环利用的物质只有3种
B. 设计该热化学循环流程的目的是制备硫酸
C. 反应Ⅱ中氧化产物与还原产物的物质的量之比为1:2
D. 若在恒容密闭容器中进行反应Ⅲ,当气体密度不变时,则说明反应已达到化学平衡
-
某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO实验流程如下:
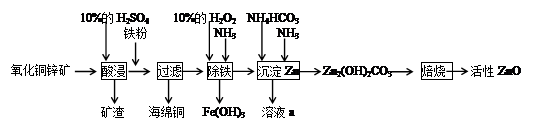
请回答下列问题:
(1)加入铁粉后发生反应的离子方程式为__________。
(2)甲、乙两同学选用下列仪器,采用不同的方法来制取氨气。
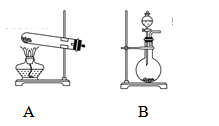
①甲同学使用的药品是熟石灰与氯化铵,则应选用装置______(填写装置代号),生成氨气的化学方程式为____________;
②乙同学选用了装置B,则使用的两种药品的名称为_______________。
(3)H2O2的作用是_____________。
(4)除铁过程中得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂(K2FeO4),该反应中氧化剂与还原剂的物质的量之比为____________。
(5)乙知溶液a中含有CO32-、SO42-两种酸根阴离子,若只允许取用一次样品,检验这种离子存在的实验操作过程为___________________。
-
某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO实验流程如下:
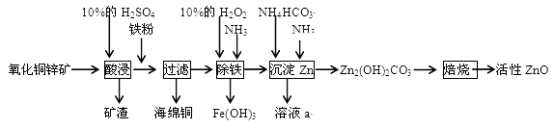
请回答下列问题:
(1)加入铁粉后发生反应的离子方程式为_________。
(2)甲、乙两同学选用下列仪器,采用不同的方法来制取氨气。
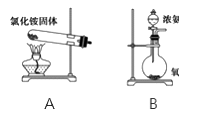
①甲同学使用的药品是熟石灰与氯化铵,則应选用装置_________(填写装置代号),生成氨气的化学程式为_________。
②乙同学选用了装置B,则使用的两种药品的名称为_________。
(3)H2O2的作用是_________。
(4)除铁过程中得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到—种高效的多功能水处理剂(K2FeO4),该反应中氧化剂与还原剂的物质的量之比为_________。
(5)已知溶液a中含有CO32-、SO42-两种酸根阴离子,若只允许取用一次样品,检验这种离子存在的实验操作过程为_________。
-
合成氨及其相关工业中,部分物质间的转化关系如下:
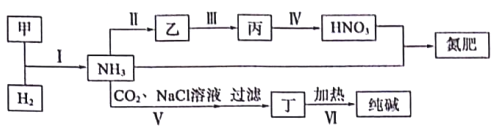
下列说法正确的是
A. 反应I、Ⅱ、Ⅲ、V均属于氧化还原反应
B. 甲、乙、丙和丁四种物质中都含有氮元素
C. 反应Ⅳ和Ⅵ中的部分产物可在上述流程中循环利用
D. 反应V是先向饱和氯化钠溶液中通CO2至饱和再通NH3
-
工业上可以利用废气中的CO2为原料制取甲醇。请回答下列问题:
(1) 已知常温常压下,下列两个可逆反应的能量变化如下图所示:
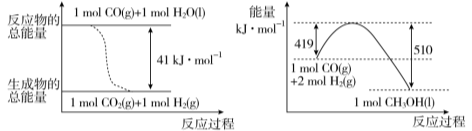
请写出左图反应的平衡常数表达式K= 。
请写出由二氧化碳和氢气制备甲醇的热化学方程式 。
(2) 如果只改变一个条件使上述反应方程式的平衡常数K值变大,则该反应________(选填编号)。
A.一定向正反应方向移动 B.在平衡移动时,正反应速率先增大后减小
C.一定向逆反应方向移动 D.在平衡移动时,逆反应速率先减小后增大
(3) 在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有关说法正确的是________(填字母)。
A.H2的浓度减小 B.正反应速率加快,逆反应速率也加快
C.甲醇的物质的量增加 D.重新平衡时,n(H2)/n(CH3OH)增大
(4) 保持温度和体积不变,通入1molCO2和3molH2 ,下列能说明该反应已达平衡状态的是________(填字母)。
,下列能说明该反应已达平衡状态的是________(填字母)。
A.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
B.容器内压强保持不变
C.H2的消耗速率与CO2的消耗速率之比为3∶1
D.容器内气体的平均相对分子质量保持不变
(5) 若反应容器的容积为2.0 L,反应时间4.0 min,容器 内气体的密度减少了2.0 g·L-1。在这段时间内CO2的平均反应速率为_______________
内气体的密度减少了2.0 g·L-1。在这段时间内CO2的平均反应速率为_______________
(6) 有人设计甲醇-空气燃料电池电源, 用石墨作电极电解200 mL含有下列离子的溶液:
用石墨作电极电解200 mL含有下列离子的溶液:
| 离子 | Cu2+ | H+ | Cl- | SO |
| c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,标况下当两极收集到相同体积的气体时,阳极上收集到氧气的质量为____________(忽略溶液体积的变化及电极产物可能存在的溶解现象)。也有人用此电源利用电解法制备Na2FeO4,阳极材料为铁,其电解质溶液用NaOH溶液,阳极反应式为 。
-
美国通用原子能公司(GA)提出的碘硫热化学循环是由反应Ⅰ、Ⅱ、Ⅲ三步反应组成的(如下图所示),下列有关说法正确的是( )
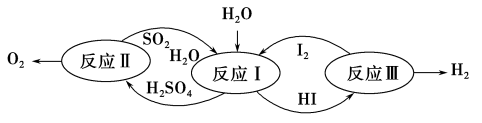
A.设计该循环是为了制取能源气体O2
B.图中反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
C.图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行
D.整个循环过程中产生1 mol O2的同时产生44.8 L H2
-
软锰矿主要成分为MnO2,还含有CaCO3、Fe2O3、Al2O3等杂质。工业上利用软锰矿制取碳酸锰(MnCO3)流程如下:
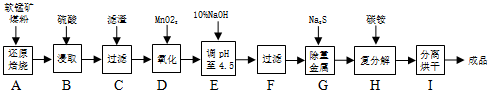
其中,还原焙烧主反应为:2MnO2+C=2MnO+CO2↑。根据要求回答问题:
(1)步骤D中Fe2+被氧化,该反应的离子方程式为 。
(2)步骤H的离子方程式为 。
(3)加入Na2S可以除去Pb2+、Al3+等离子。已知Ksp(PbS)=1×10-28 Ksp(MnS)= 1×10-9.6 ,当溶液中c(Pb2+)=1×10-5mol·L-1时,溶液中c(Mn2+)允许的最大值为 。
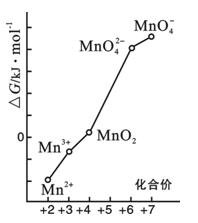
(4)pH=0的溶液中,不同价态锰的微粒的能量(△G)如右图。若某种含锰微粒(如Mn3+)的能量处于相邻价态两种微粒(Mn2+和MnO2)能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒。
①MnO42—能否稳定存在于pH=0的溶液中?答:______________(“能”或“不能”);
②将Mn3+歧化反应设计为原电池,可测定反应平衡常数。电池负极反应为 ,平衡常数表达式为 ;
③实验室可利用以下反应检验Mn2+存在:2Mn2+ + 5S2O82- + 8H2O → 16H+ + 10SO42- + 2MnO4-
确认Mn2+存在的现象是 ;检验时必须控制Mn2+浓度和用量不能过大,否则实验失败。理由是 。
-
工业上可以利用废气中的CO2为原料制取甲醇,其反应方程式为:CO2+3H2 CH3OH+H2O。请回答下列问题:
CH3OH+H2O。请回答下列问题:
(1)已知常温常压下下列反应的能量变化如下图所示:




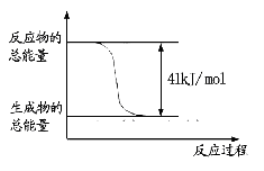

写出由二氧化碳和氢气制备甲醇的热化学方程式__ _。
该反应的△S____0(填“>”或“<”或“=”),在 ______情况下有利于该反应自发进行。
(2)如果上述反应方程式的平衡常数K值变大,则该反应__ (选填编号)。
A.一定向正反应方向移动 B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动 D.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,能说明反应已达到平衡状态的是 __ (选填编号)。
A.3v正(H2)=v逆(CO2) B.C(H2) = C(CO2)
C.容器内气体的密度不变 D.容器内压强不变
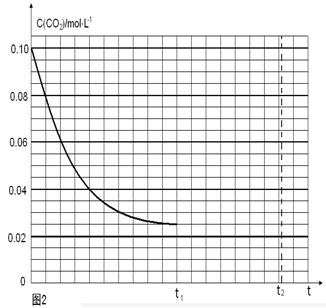
(4)若反应的容器容积为2.0L,反应时间4.0 min,容器内气体的密度增大了2.0g/L,在这段时间内CO2的平均反应速率为 。反应在t1时达到平衡,过程中c(CO2)随时间t变化趋势曲线右图所示。保持其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)。
-
(10分)某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO实验流程如下:
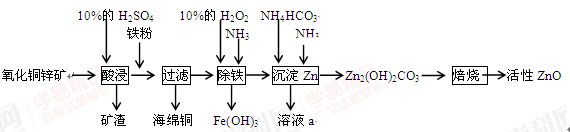
请回答下列问题:
(1)加入铁粉后发生反应的离子方程式为_________________________,_______ _。
(2)甲、乙两同学选用下列仪器,采用不同的方法制取氨气。
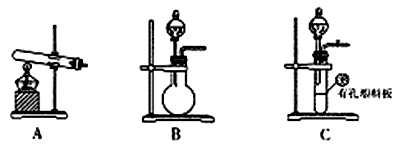
①甲同学使用的药品是熟石灰与氯化铵,则应选用装置_______(填写装置代号),生成氨气的化学方程式为_______________________________________;
②乙同学选用了装置B,则使用的两种药品的名称为______________ _。
(3)H2O2的作用是____________________________________________________。
(4)除铁过程中得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂(K2FeO4),该反应中氧化剂与还原剂的物质的量之比为____________。
(5)已知溶液a中含有CO2- 3、SO2- 4两种酸根阴离子,若只允许取用一次样品,检验这种离子存在的实验操作过程为_____________________________

CuOH(s)+Cl-(aq)+H+(aq)的平衡常数K=___________(填数值)。

2Cl2(g)+2H2O(g),在不同起始投料比m下,HC1平衡转化率随温度的变化关系如下图所示: