有关化学键的键能(指将1mol气态分子拆开形成气态原子时,每个化学键断裂所需的最低能量)数据如表所示:
| 化学键 | C-H | C=C | H-H | C-C |
| 键能/(KJ/mol) | 413.4 | x | 436.0 | 347.7 |
已知CH2=CH2(g)+H2(g)CH3CH3(g) ΔH=-123.5kJ/mol,x的值为
A. 136.8 B. 307.5 C. 615.0 D. 177.3
高二化学单选题中等难度题
有关化学键的键能(指将1mol气态分子拆开形成气态原子时,每个化学键断裂所需的最低能量)数据如表所示:
| 化学键 | C-H | C=C | H-H | C-C |
| 键能/(KJ/mol) | 413.4 | x | 436.0 | 347.7 |
已知CH2=CH2(g)+H2(g)CH3CH3(g) ΔH=-123.5kJ/mol,x的值为
A. 136.8 B. 307.5 C. 615.0 D. 177.3
高二化学单选题中等难度题
有关化学键的键能(指将1mol气态分子拆开形成气态原子时,每个化学键断裂所需的最低能量)数据如表所示:
| 化学键 | C-H | C=C | H-H | C-C |
| 键能/(KJ/mol) | 413.4 | x | 436.0 | 347.7 |
已知CH2=CH2(g)+H2(g)CH3CH3(g) ΔH=-123.5kJ/mol,x的值为
A. 136.8 B. 307.5 C. 615.0 D. 177.3
高二化学单选题中等难度题查看答案及解析
能源短缺是人类社会面临的重大问题,利用化学反应可实现多种形式的能量相互转化。请回答以下问题:
(1)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程。已知反应N2(g)+3H2(g)2NH3(g) △H=-93 kJ·mol-1。试根据表中所列键能数据,计算a 的数值为_______kJ/mol。
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ·mol-1 | 436 | a | 945 |
(2)甲醇是一种可再生能源,具有广泛的开发和应用前景。已知在常压下有如下变化:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =a kJ/mol
② H2O(g)=H2O(l) ΔH =b kJ/mol
写出液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式:________。
(3)可利用甲醇燃烧反应设计一个燃料电池。如下图1,用Pt作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
①写出燃料电池正极的电极反应式________。②若利用该燃料电池提供电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是________极(填”A”或”B”);当铁件的质量增重6.4g时,燃料电池中消耗氧气的标准状况下体积为________L。
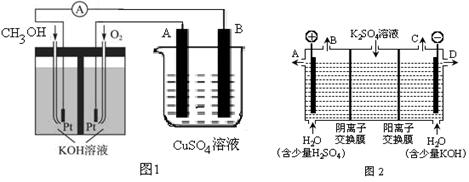
(4)如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图2装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾(电解槽内的阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)。
①该电解槽的阳极反应式为________,单位时间内通过阴离子交换膜的离子数与通过阳离子交换膜的离子数的比值为________。
②从出口D导出的溶液是________(填化学式)。
高二化学填空题极难题查看答案及解析
能源短缺是人类社会面临的重大问题,利用化学反应可实现多种形式的能量相互转化。请回答以下问题:
(1)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程。已知反应N2(g)+3H2(g)2NH3(g) △H=-93 kJ·mol-1。
试根据表中所列键能数据,计算a 的数值为 kJ/mol。
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ·mol-1 | 436 | a | 945 |
(2)甲醇是一种可再生能源,具有广泛的开发和应用前景。已知在常压下有如下变化:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =a kJ/mol
② H2O(g)=H2O(l) ΔH =b kJ/mol
写出液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式: 。
(3)已知:HCN(aq)与NaOH(aq)反应的焓变△H=-12.1kJ·mol-1; HCl(aq)与NaOH(aq)反应的焓变ΔH=-55.6 kJ·mol-1。则HCN在水溶液中电离的焓变ΔH等于 。
(4)已知:H2(g)+1/2O2(g)=H2O(1) △H=-285.83kJ·mol-1
CO(g)+1/2O2(g)=CO2(g) △H=-282.9kJ·mol-1;
若氢气与一氧化碳的混合气体完全燃烧可生成5.4g H2O(l),并放出114.3kJ的热量,则混合气中CO的物质的量为 (计算结果保留以为小数)
高二化学填空题困难题查看答案及解析
化学健的键能指常温常压下,将1mol分子AB拆开为中性气态原子A和B所需要的能量(单位为kJ·mol-1)。根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热△H为( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
A.-485kJ·mol-1 B.+485kJ·mol-1
C.+1940kJ·mol-1 D.-1940kJ·mol-1
高二化学单选题中等难度题查看答案及解析
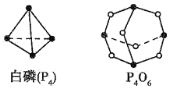
(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____。
(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____。
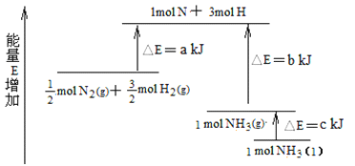
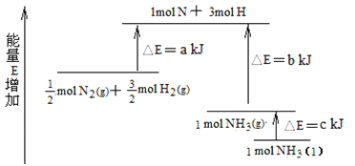
(3)化学反应N2+3H22NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
高二化学填空题中等难度题查看答案及解析
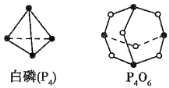
(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____。
(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____。
(3)化学反应N2+3H22NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
高二化学填空题中等难度题查看答案及解析
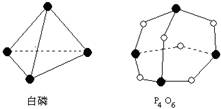
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198 P—O:360 O=O:498则反应P4(白磷)+3O2= P4O6的反应热ΔH为
A.-1638 kJ·mol-1 B.+1638 kJ·mol-1
C.-126 kJ·mol-1 D.+126 kJ·mol-1
高二化学选择题简单题查看答案及解析
(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷(P4)和P4O6的分子结构如图所示,
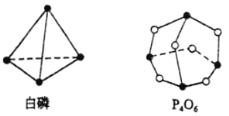
已知:
| 化学键 | P—P | P—O | O=O |
| 键能(kJ·mol1) | 198 | 360 | 498 |
则反应P4(g)+3O2(g)= P4O6(g)的△H=_________。
(2)已知①2C(s)+O2(g)=2CO(g) △H= -221.0 kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H= -483.6 kJ/mol
则制备水煤气的反应C(s)+H2O(g)=CO(g)+ H2(g)的△H=_______。
高二化学计算题中等难度题查看答案及解析
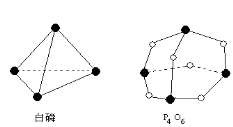
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol1):P—P:198 P—O:360 O=O:498则反应 P4(白磷)+3O2= P4O6的反应热ΔH为
A.-1638 kJ·mol1 B.+1638 kJ·mol1
C.-126 kJ·mol1 D.+126 kJ·mol1
高二化学选择题中等难度题查看答案及解析
化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ·mol-1)P—P:198;P—O:360;O—O:498。则反应P4(白磷)+3O2=P4O6的反应热△H为
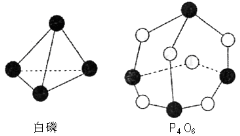
A.-1638kJ/mol B.+1638kJ/mol
C.-126kJ/mol D.+126kJ/mol
高二化学选择题困难题查看答案及解析