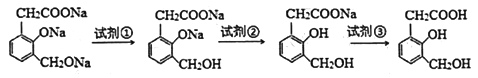-
物质的组成与结构决定了物质的性质与变化,回答下列问题:
(1)量子力学把电子在原子核外的一个空间运动状态称为一个____________,电子除空间运动状态外,还有一种运动状态叫做____________。
(2)硒常用作光敏材料,基态硒原子的价电子排布式为_______________;与硒同周期的p区元素中第一电离能大于硒的元素有_________种。
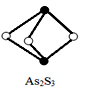
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下图,As原子的杂化方式为___________,雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,写出该反应方程式________________。SnCl4分子的空间构型为_______。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图。
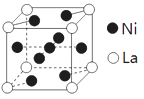
①储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱和面心则形成的储氢化合物的化学式为_________。
②测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为_______。(不必计算出结果,用NA表示阿伏伽德罗常数。)
-
Ⅰ.回答下列问题:
(1)量子力学把电子在原子核外的一个空间运动状态称为一个________,还有一种状态叫做________。
(2)写出 原子的外围电子排布式:______,其在周期表中的位置________,其在周期表中处于______区,与
原子的外围电子排布式:______,其在周期表中的位置________,其在周期表中处于______区,与 同周期的所有副族元素的基态原子中,最外层电子数与
同周期的所有副族元素的基态原子中,最外层电子数与 相同的元素有_________种。
相同的元素有_________种。
(3)下列 原子电子排布图表示的状态中,能量最低和最高的分别为_______、_______(填标号)。
原子电子排布图表示的状态中,能量最低和最高的分别为_______、_______(填标号)。
A 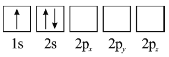 B
B 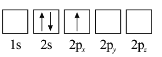
C 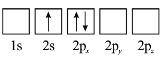 D
D 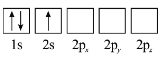
Ⅱ.有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层 能级的电子数等于次外层的电子总数, B元素可分别与A、C、D生成
能级的电子数等于次外层的电子总数, B元素可分别与A、C、D生成 型化合物,并知在
型化合物,并知在 中,
中, 与
与 的质量比为
的质量比为 原子的价电子排布式为
原子的价电子排布式为 。根据以上条件,回答下列问题:
。根据以上条件,回答下列问题:
(1)C的基态原子的电子占据最高能层的符号为_______, 原子的价电子排布图________。
原子的价电子排布图________。
(2)A、B、C三种元素的第一电离能由大到小的顺序______(用元素符号表示)。
(3)元素B和D的电负性由大到小的顺序_________(用元素符号表示)。
(4)写出E的元素符号_________,要证明太阳光中含有E元素,可采用的方法是__________。
-
【化学—选修3:物质结构与性质】
钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:

回答下列问题:
(1)基态钛原子的价电子排布图为 ,其原子核外共有 种运动状态不相同的电子。金属钛晶胞如下图1所示,为 堆积(填堆积方式)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l >> l-b > b-b(l为孤对电子对,b为键合电子对),则关于H2O中的H-O-H键角可得出的结论是________。
| A.180° | B.接近120°,但小于120° |
| C.接近120°,但大于120° | D.接近109°28’,但小于109°28’ |
(3)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃,可知TiCl4为________晶体。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是 。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 。
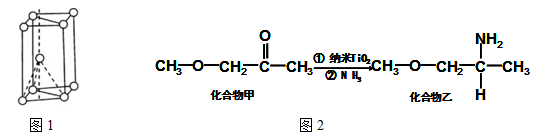
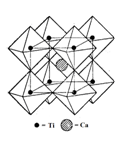
(5)钙钛矿晶体的结构如右图所示。钛离子位于立方晶胞的角顶,被 个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被 个氧离子包围。钙钛矿晶体的化学式为 。若该晶胞的边长为a pm,则钙钛矿晶体的密度为 g.cm-3(只要求列算式,不必计算出数值)。
-
某绿色农药结构简式为,回答下列问题。

(1)N元素的基态原子核外有_____种空间运动状态的电子,该农药组成元素中,第一电离能较大的前三种元素是(按由大到小顺序排列)__________________(用元素符号回答,下同),基态硒原子的价层电子排布式为________________________。
(2)该物质中杂化轨道类型为sp2的原子有__________。
(3)碳、氢、氧元素可形成一系列的化合物,如CH4、C2H6、CH3OH等。与CH4互为等电子体的一种微粒是______。
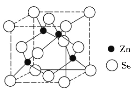
(4)硒化锌的晶胞结构如图所示,则硒的配位数为_______,若晶胞边长为d pm,设阿伏加德罗常数的值为NA,则硒化锌的密度为____________g/cm3。
-
“结构决定性质,性质反映结构”是化学学科重要的学科思想,在有机化学中体现尤为明显。据此回答下列问题:
(1)有机化学中把结构相似、分子组成相差若干个“CH2”原子团的有机化合物互称为同 系物。同系物的化学性质一定_________(填“相同”、“相似”或“不同”),下列有机物中一定属于同系物的是____________(填序号)。
①C3H4和C5H8 ②乙酸和硬脂酸(C17H35COOH)
③ 和
和 ④淀粉和纤维素 ⑤丙烯和聚乙烯
④淀粉和纤维素 ⑤丙烯和聚乙烯
⑥HOOCCH=CHCOOH和HOOCCH=C(CH3)COOH
(2)在有机物中,当同一官能团连接不同基团时,其表现出来的性质也有所不同。如有机物A(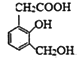 )的分子中有三种烃基(-OH),但由于其直接连接的基团不同而导致活泼性不同。下列转化关系中选用的试剂为①________;②________;③_______。
)的分子中有三种烃基(-OH),但由于其直接连接的基团不同而导致活泼性不同。下列转化关系中选用的试剂为①________;②________;③_______。
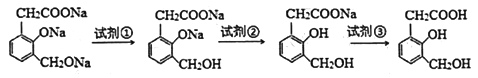
醛和酮的分子中都含有羰基( ),但只有醛能被弱氧化剂氧化,请写出葡萄糖与银氨溶液反应的化学方程式:_____________ 。
),但只有醛能被弱氧化剂氧化,请写出葡萄糖与银氨溶液反应的化学方程式:_____________ 。
(3)某烃A,相对分子质量为140,其中碳的质量分数为0.857。A分子中有两个碳原子 不与氢直接相连。A在一定条件下氧化只生成G,G能使石蕊试液变红。
已知: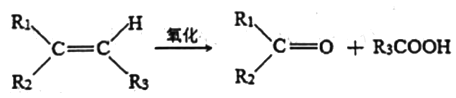
则产物G的结构简式为__________ ,烃A在一定条件下生成高分子化合物的化学方程式为_______________ 。
-
物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_____种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_____。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是_____,1mol(C2H5O)3P=O分子中含有的σ键的数目为_____。
(4)已知固态NH3、H2O、HF的氢键键能和结构如图1:
| 物质 | 氢键X﹣H…Y | 键能kJ.mol﹣1 |
| (HF)n | D﹣H…F | 28.1 |
| 冰 | O﹣H…O | 18.8 |
| (NH3)n | N﹣H…N | 5.4 |

解释H2O、HF、NH3沸点依次降低的原因_____。
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有_____个,与碳原子等距离最近的碳原子有_____个。已知碳化硅晶胞边长为apm,则晶胞图2中1号硅原子和2号碳原子之间的距离为_____pm,碳化硅的密度为_____g/cm3。
-
物质的结构决定物质的性质,请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有________种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的末成对电子数相同,则其基态原子的价层电子排布式为_________________。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是__________________。
1mol(C2H5O)3P=O分子中含有的σ键的数目为_________________。
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:

由此可知NH3、H2O、HF沸点由高到低的顺序为___________________。
(5)碳化硅的结构与金刚石类似,如下图所示,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有______个,与碳原子等距离最近的碳原子有_____个。已知碳化硅晶胞边长为apm,则碳化硅的密度为__________g/cm3(己知C和Si的相对原子质量分别为12和28,阿伏加徳罗常数用NA表示)。

-
物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)氨气极易溶于水的主要原因是_____________________。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的外围电子排布式为________________。
(3)碳化硅的结构与金刚石类似(如图所示),4个硅原子位于体心位置,碳原子位于顶点、面心位置,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个硅原子周围与其距离最近的碳原子有_______个,碳化硅化学式为________。已知碳化硅晶胞边长为acm,阿伏加德罗常数为NA,则碳化硅的密度为_______g·cm3。

(4)(CH3)3N可用于制备医药、农药,则(CH3)3N_______(填“能”或“不能”)溶于水。化合物(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键为_______。
a.离子键 b.配位键 c.氢键 d.非极性共价键
(5)成键原子中的孤电子对对键能有影响,第二周期元素A与氢形成的化合物中A-A键的键能(单位:kJ·mol-1)如下:H3C-CH3 346,H2N-NH2 247,HO-OH 207;
试分析上述化合物中A-A键的键能依次下降的原因__________________________。
-
下列表述不正确的是
A. 福岛核电站泄露的放射性物质131I与127I互为同位素,化学性质几乎相同
B. 电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述
C. 除去SO2中混有的少量HCl,使气体通过盛有饱和NaHSO3溶液的洗气瓶
D. 为了证明氢氧化钠是离子化合物,可在瓷坩埚中将氢氧化钠固体熔化后测其导电性
-
下列表述不正确的是
A.福岛核电站泄露的放射性物质131I与127I互为同位素,化学性质几乎相同
B.电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述
C.除去SO2中混有的少量HCl,使气体通过盛有饱和NaHSO3溶液的洗气瓶
D.为了证明氢氧化钠是离子化合物,可在瓷坩埚中将氢氧化钠固体熔化后测其导电性


 B
B 
 D
D 





 ④淀粉和纤维素 ⑤丙烯和聚乙烯
④淀粉和纤维素 ⑤丙烯和聚乙烯 )的分子中有三种烃基(-OH),但由于其直接连接的基团不同而导致活泼性不同。下列转化关系中选用的试剂为①________;②________;③_______。
)的分子中有三种烃基(-OH),但由于其直接连接的基团不同而导致活泼性不同。下列转化关系中选用的试剂为①________;②________;③_______。