-
探究Na2SO3固体受热时发生分解反应的实验如下.
实验药品:Na2SO3固体、稀盐酸、新制氯水、BaCl2溶液、蒸馏水
查阅资料:Na2SO3固体受热分解可得两种产物
实验步骤:
Ⅰ.取m g Na2SO3固体,隔绝空气加强热,一段时间后,称量冷却后的固体质量仍为m g;
Ⅱ.将Ⅰ中所得固体溶于水配成100mL溶液,测得溶液的pH>7;
Ⅲ.取少量Ⅱ中溶液,加入足量稀盐酸,溶液保持澄清并产生气体,该气体不能使湿润的品红试纸褪色;
Ⅳ.另取少量Ⅱ中溶液,滴入适量新制氯水,产生浅黄色浑浊;
Ⅴ.将Ⅳ中浊液过滤后,向滤液中滴入盐酸酸化的BaCl2溶液,产生大量白色沉淀.
(1)Na2SO3溶液碱性,其原因是______(用离子方程式表示).
(2)能证明Na2SO3完全分解的实验步骤是______(填相应序号).
若仅通过测溶液的pH证明Na2SO3发生了分解,步骤Ⅱ中需补充的实验是______.
(3)步骤Ⅳ中发生反应的离子方程式是______.
(4)根据上述实验,Na2SO3固体发生分解反应的化学方程式是______ 3Na2SO4+Na2S高三化学解答题中等难度题查看答案及解析
-
探究Na2SO3固体受热时发生分解反应的实验如下.
实验药品:Na2SO3固体、稀盐酸、新制氯水、BaCl2溶液、蒸馏水
查阅资料:Na2SO3固体受热分解可得两种产物
实验步骤:
Ⅰ.取m g Na2SO3固体,隔绝空气加强热,一段时间后,称量冷却后的固体质量仍为m g;
Ⅱ.将Ⅰ中所得固体溶于水配成100mL溶液,测得溶液的pH>7;
Ⅲ.取少量Ⅱ中溶液,加入足量稀盐酸,溶液保持澄清并产生气体,该气体不能使湿润的品红试纸褪色;
Ⅳ.另取少量Ⅱ中溶液,滴入适量新制氯水,产生浅黄色浑浊;
Ⅴ.将Ⅳ中浊液过滤后,向滤液中滴入盐酸酸化的BaCl2溶液,产生大量白色沉淀.
(1)Na2SO3溶液碱性,其原因是______(用离子方程式表示).
(2)能证明Na2SO3完全分解的实验步骤是______(填相应序号).
若仅通过测溶液的pH证明Na2SO3发生了分解,步骤Ⅱ中需补充的实验是______.
(3)步骤Ⅳ中发生反应的离子方程式是______.
(4)根据上述实验,Na2SO3固体发生分解反应的化学方程式是______ 3Na2SO4+Na2S高三化学解答题中等难度题查看答案及解析
-
有一Na2SO3固体因部分被氧化而变质。为测定样品纯度,甲、乙两位同学分别设计了如下实验方案:
(甲同学)称取m g样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1 g。
(1)BaCl2溶液必须过量的原因是___________________________________________。在滤液中滴加____________溶液,若没有白色沉淀生成,则证明BaCl2溶液不足,还需继续在滤液中加入BaCl2溶液后进行过滤。洗涤残留固体的方法是__________________________________________________;在洗出液中滴加_______________溶液,可以判断残留固体是否洗涤干净。
(2)判断残留固体质量m1 g能够作为实验测定值代入计算式,推算样品纯度,必须补充的实验操作是_________________________________________________________。
(乙同学)称取m g样品溶于水,配成溶液,用滴定管取V mL于锥形瓶中,用浓度为c mol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO32- + MnO4- SO42- + Mn2+ (未配平)
(3)配制样品溶液时,不一定需要的实验仪器是__________(选填答案编号)。
a.容量瓶 b.玻璃棒 c.滴定管 d.烧杯
(4)滴定终点的判断依据是___________________________________________________。
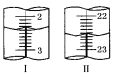
(5)上述滴定中,滴定管在注入酸性高锰酸钾溶液之前,先用蒸馏水洗净,再用__________________________________________。滴定管液面变化如图所示,从图Ⅰ图Ⅱ显示消耗的高锰酸钾溶液体积为__________________。
高三化学实验题困难题查看答案及解析
-
为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是( )

A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
高三化学单选题中等难度题查看答案及解析
-
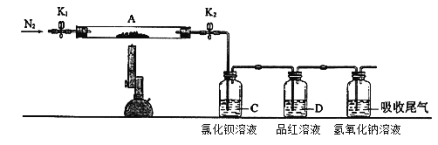
为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是( )
A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
高三化学单选题中等难度题查看答案及解析
-
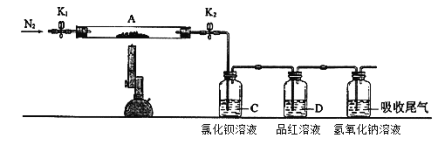
为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是( )
A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
高三化学单选题困难题查看答案及解析
-
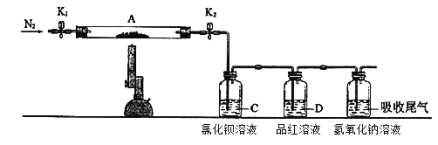
为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是( )
A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
高三化学单选题困难题查看答案及解析
-
为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是( )

A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
高三化学单选题困难题查看答案及解析
-
为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是( )
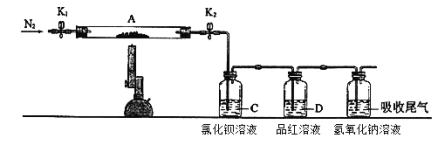
A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
高三化学单选题困难题查看答案及解析
-
为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是
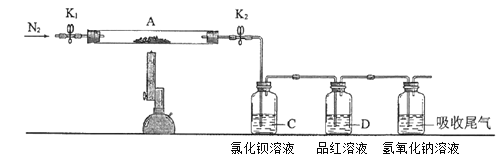
A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
高三化学单选题中等难度题查看答案及解析