-
[化学-物质结构与性质] (13分)
(1)中国古代四大发明之一——黑火药,它的爆炸反应为
 (已配平)
(已配平)
①除S外,上列元素的电负性从大到小依次为________。
②在生成物中,A的晶体类型为________,含极性共价键的分子的中心原子轨道杂化类型为________。
③已知 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为________。
键数目之比为________。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为________, 的未成对电子数是________。
的未成对电子数是________。
(3)在 的水溶液中,一定条件下存在组成为
的水溶液中,一定条件下存在组成为 (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:

交换出来的 经中和滴定,即可求出x和n,确定配离子的组成。¥
经中和滴定,即可求出x和n,确定配离子的组成。¥
将含0.0015 mol  的溶液,与R-H完全交换后,中和生成的
的溶液,与R-H完全交换后,中和生成的 需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,该配离子的化学式为。
需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,该配离子的化学式为。
-
中国古代四大发明之一——黑火药,它在爆炸时发生的化学反应为2KNO3+3C+S=A+N2↑+3CO2↑(已配平)
(1)①除S外,上列元素的电负性从大到小依次为__________。
②在生成物中,A的晶体类型为_______,含极性共价键的分子的中心原子轨道杂化类型为_____。
③已知CN-与N2互为等电子体,推算HCN分子中σ键与π键数目之比为_____。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为______,Q2+的未成对电子数是_______。
(3)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。则晶胞中该原子的配位数为________,该单质晶体中原子的堆积方式为四种基本堆积方式中的________。

-
(1)中国古代四大发明之一--黑火药,它的爆炸反应为2KN03+3C+S
 A+N2↑+3C02↑(已配平)
A+N2↑+3C02↑(已配平)
①除S外,上列元素的电负性从大到小依次为______.
②在生成物中,A的晶体类型为______,含极性共价键的分子的中心原子轨道杂化类型为______.
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为______.
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2.T的基态原子外围电子(价电子)排布为______,Q2+的未成对电子数是______.
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H20)6-n]x++R-H→Rx[CrCln(H2O)6-n]x-+xH-交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成.将含0.0015mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200mol•L-1 NaOH溶液25.00ml,该配离子的化学式为______.
-
(10分) 中国古代四大发明之一——黑火药,它的爆炸反应为:
2KNO3+3C+SA+N2↑+3CO2↑(已配平)
(1)①除S外,上列元素的电负性从大到小依次为______________________。
②在生成物中,A的晶体类型为___,含极性共价键的分子的中心原子轨道杂化类型为____。
③已知CN-与N2为等电子体,推算HCN分子中σ键与π键数目之比为________________。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为______,Q2+的未成对电子数是_______。
(3)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为________ ,该单质晶体中原子的堆积方式为四种基本堆积方式中的________.

(4)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R—H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR—H―→Rx[CrCln(H2O)6-n]x++xH+交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。将含0.0015 mol [CrCln(H2O)6-n]x+的溶液,与R—H完全交换后,中和生成的H+需浓度为0.1200mol·L-1NaOH溶液25.00 mL,可知该配离子的化学式为______,中心离子的配位数为________。
-
(1)中国古代四大发明之一—黑火药,它的爆炸反应为S+2KNO3+3C A+N2↑+K2S(已配平)
①除S外,上列元素的电负性从大到小依次为________(2分)
②在生成物中,A的晶体类型为________,(2分)中心原子轨道的杂化类型是
________(2分)
③已知 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为________(2分)
键数目之比为________(2分)
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2,T基态原子的电子排布式为________(2分),解释Q3+比Q2+稳定的原因是(2分)
(3)将CoCl2溶液中加入氨和氯化铵的混合液,用氧化剂把Co2+氧化成Co3+后加入盐酸可得到[Co(NH3)mCln]+(Co的配位数为6)的配离子,该配合物的化学式为________
(3分)
-
黑火药是我国古代四大发明之一,它的爆炸反应为:2KNO3+3C+S═K2S+N2↑+3CO2↑(已配平)
(1)除S外,上列元素的第一电离能从大到小依次为___________________________;
(2)生成物中,A 的电子式为____________;含极性共价键的分子的中心原子轨道杂化类型_____________;
(3)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
(4)S的基态原子价层电子排布式为___________,S的一种化合物ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0pm,密度为________g·cm3(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为___________pm。

-
黑火药是中国古代四大发明之一,它的爆炸反应为:
2KNO3+3C+S  K2S+N2↑+3a 已配平
K2S+N2↑+3a 已配平
①画出氮原子的结构示意图 ________ 。
②生成物中除氮气与硫化钾外,还有一种物质A生成,则A的化学式为________。
③黑火药中位于元素周期表短周期的元素有________种;其中一种元素的氧化物可用于漂白纸浆、丝、草帽辫等并能用于杀菌、消毒,该元素在周期表中的位置是________,写出该氧化物通入FeCl3溶液反应的离子方程式________。
④下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的是________。
A.同条件同浓度溶液的pH:H2CO3>H2SO4 B.稳定性:H2SO4>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价 D.溶解性:H2S>CH4
⑤已知常温时CuS的Ksp=1.3×10-36,向100 ml 2×10-18 mol/L 的K2S溶液中加入100 ml
2×10-18 mol/L的CuCl2溶液,试通过计算说明有无CuS沉淀生成(写出计算推理过程,忽略溶液混合时的体积变化)。________ 。
-
(物质结构与性质)黑火药是我国古代的四大发明之一。黑火药爆炸时发生的反应为:
2KNO3+S+3C=K2S+N2↑+3CO2↑。回答下列问题:
(1)基态钾原子的核外电子排布式为____________,第一电离能:K____________(填“>”或“<”)Na。
(2)NO3-的空间构型为_____________。
(3)固态硫易溶于CS2,熔点为112℃,沸点为444.8℃。其分子结构为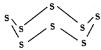 ,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
(4)N2分子中σ键与π键的个数比为___________,,N2的沸点比CO的沸点__________(填“高”或“低”)。
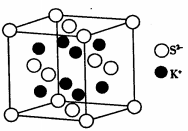
(5)K2S的晶胞结构如图所示。其中K+的配位数为_____________,S2-的配位数为__________;若晶胞中距离最近的两个S2-核间距为acm,则K2S晶体的密度为__________g·cm-3(列出计算式,不必计算出结果)。
-
黑火药是中国古代四大发明之一,它的爆炸反应为:

(1)生成物中除了氮气与二氧化碳外,还有一种物质A生成,则A的电子式为,A属于________晶体。
(2)黑火药中位于元素周期表短周期的元素有种。其中一种元素的单质可用于制药,其氧化物可用于漂白织物和防腐剂,该元素在周期表中的位置是,该元素的原子核外有________种不同运动状态的电子。
(3)黑火药中所含元素的原子半径从大到小的顺序是(用元素符号表示);
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有________。
A.同条件同浓度溶液pH:Na2CO3>Na2SO4 B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价 D.分解温度:CH4>H2S
-
黑火药是中国古代四大发明之一,它的爆炸反应为:
2KNO3+3C+S A+N2↑+3CO2↑(已配平)。
A+N2↑+3CO2↑(已配平)。
(1)生成物中除了氮气与二氧化碳外,还有一种物质A,则A的电子式为 ,A属于________化合物。
(2)黑火药中位于元素周期表短周期的元素有 种。其中一种元素的单质可用于制药,其氧化物可用于漂白织物和作防腐剂,该元素在周期表中的位置是 。
(3)黑火药中所含元素的原子半径从大到小的顺序是 (用元素符号表示);
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有 。
A.同条件同浓度溶液的pH:Na2CO3>Na2SO4
B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
(已配平)
与
结构相似,推算HCN分子中
键与
键数目之比为________。
的未成对电子数是________。
的水溶液中,一定条件下存在组成为
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:

经中和滴定,即可求出x和n,确定配离子的组成。¥
的溶液,与R-H完全交换后,中和生成的
需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,该配离子的化学式为。


 ,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。