-
某小组同学进行如下实验:
①向10mL 1mol/LKBr溶液中通入一定量氯气,溶液变为黄色,将溶液分为两等份;
②往第一分溶液中加入淀粉碘化钾溶液,溶液变为蓝色;
③向第二份溶液中继续通入氯气,溶液由黄色变为橙色。下列分析不正确的是
A. 实验①溶液中发生反应的离子方程式是: Cl2+2Br-=Br2+2Cl-
B. 仅根据实验②能说明氧化性: Br2>I2
C. 向实验③所得溶液中加苯,充分振荡,上层为橙红色
D. 上述实验验证了Cl2、Br2、I2的氧化性相对强弱
高一化学单选题中等难度题查看答案及解析
-
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变为红色(已知:AgBr、AgI分别为浅黄色和黄色不溶于硝酸的沉淀),则下列叙述正确的是( )。
A. 原溶液中的Br-可能未被氧化
B. 反应后的溶液中是否含有Fe2+可以用氯水和KSCN溶液检验
C. 取所得溶液加入CCl4后静置分液,向上层溶液中加入足量AgNO3溶液,能产生黄色沉淀
D. 反应后的溶液中一定不存在Fe2+
高一化学选择题困难题查看答案及解析
-
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变为红色
已知:AgBr、AgI分别为浅黄色和黄色不溶于硝酸的沉淀
,则下列叙述正确的是( )
A.原溶液中的Br-一定被氧化
B.通入氯气之后原溶液中的Fe2+一定被氧化
C.溶液中一定不存在Fe2+
D.若取少量所得溶液,再加入CCl4溶液,静置、分液,向上层溶液中加入足量的AgNO3 溶液,能产生黄色沉淀
高一化学单选题困难题查看答案及解析
-
现有一包铝热剂是铝粉和氧化铁粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(计算浓度时假定溶液体积没有变化):
①向其中一份固体中加入100mL 2.0mol/L的NaOH溶液,加热使其充分反应后过滤,测得滤液的c(OH-)=1mol/L;
②向另一份固体中加入140mL 4.0 mol/L的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)=1mol/L。
(1)写出该铝热反应的化学方程式:_______________________________
写出实验①发生的离子方程式:_________________________________。
(2)这包铝热剂中铝粉的质量为___________________________。
(3)这包铝热剂中氧化铁粉末的质量为__________________________________。
高一化学综合题中等难度题查看答案及解析
-
现有一包铝热剂是铝粉和氧化铁(Fe2O3)粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(假定反应前后溶液的体积不变):
①向其中一份固体中加入100 mL 2.0mol•L-1的NaOH溶液,加热使其充分反应后过滤,测得溶液中的c(OH-)=1mol•L-1
②向另一份固体中加入100 mL 4.0 mol•L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)=0.1mol•L-1则产生的气体的体积(标准状况)为 ( )
A.2.856L B.2.448L C.2.688L D.2.352L
高一化学选择题中等难度题查看答案及解析
-
实验探究Fe3+的氧化性:向FeCl3溶液中通入一定量的SO2气体,溶液由黄色变为浅绿色。
(1)浅绿色溶液中一定存在的离子有H+、Cl-和 。
(2)某同学认为反应后的溶液中可能存在H2SO3,应选择以下试剂 (填写序号)加以检验。
A.稀硫酸 B.NaOH溶液 C.KSCN溶液 D.品红溶液
高一化学填空题中等难度题查看答案及解析
-
某同学为验证同主族元素非金属性的变化规律,设计了如下实验(实验装置如图所示)。
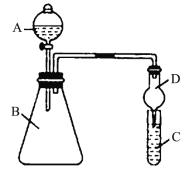
(1)仪器A的名称为___,干燥管D的作用是___。
(2)向Na2S溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为___。
(3)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4固体,C中加淀粉碘化钾混合溶液,观察到___,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用___溶液吸收尾气。
(4)课外活动小组在A中加盐酸、B中加CaCO3固体,C中加Na2SiO3溶液,观察到C中产生白色沉淀(H2SiO3),请你利用原子结构知识解释这一现象:___;有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加盛有___的洗气瓶。
高一化学实验题中等难度题查看答案及解析
-
某同学为验证元素周期表中元素性质的递变规律,利用右图装置可验证同主族非金属性的变化规律。设计了如下系列实验。
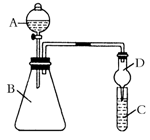
(1)向Na2S溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为____________________________________________。
(2)仪器A的名称为____________________,
(3)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4, (KMnO4 与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到混合溶液 的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用______________ 溶液吸收尾气。
(4)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3,C中加Na2SiO3 溶液观察到C中溶液_____________的现象,即可证明。但有的同学认为盐酸具有挥发性,应用__________溶液除去。
高一化学填空题简单题查看答案及解析
-
某溶液中可能含有Na+、K+、Br-、SO42-、CO32-等离子中的全部或其中的几种,现进行以下的连续操作:a.用洁净铂丝蘸取溶液在无色火焰上灼烧,火焰呈黄色;b.溶液中通入氯气,溶液由无色变为红棕色;c.溶液中加入过量的稀硫酸后,无气体放出;再加Ba(OH)2溶液后,产生白色沉淀。试填写下列空白:
⑴原混合液中一定存在的离子是______________,一定不存在的离子是_____________
⑵上述a—c的操作中,______是错误的,理由是______________________________。
⑶为确定另一种金属离子是否存在,应补充的操作是__________________。
高一化学填空题简单题查看答案及解析
-
下列解释实验事实的离子方程式不正确的是
A.向铜粉中滴加稀HNO3溶液,产生气体:Cu + 2H+ = Cu2+ + H2↑
B.向FeCl2溶液中通入氯气,溶液变为黄色:2Fe2+ + Cl2 = 2Fe3+ + 2Cl-
C.向CuSO4溶液中滴加NaOH溶液,生成沉淀:Cu2+ + 2OH-= Cu(OH)2↓
D.Fe(OH)2由白色变灰绿,最后变为红褐色:4Fe(OH)2 + O2+2H2O = 4 Fe(OH)3
高一化学单选题简单题查看答案及解析