-
(9分)四氧化三铅俗名“铅丹”或“红丹”,由于有氧化性被大量地用于油漆船舶和桥梁钢架防锈,其化学式可写为氧化物2PbO·PbO2或盐Pb2PbO4。欲测定某样品中四氧化三铅含量,进行如下操作:
①称取样品0.1000 g,加还原性酸溶解,得到含Pb2+的溶液。
②在加热条件下用过量K2Cr2O7将Pb2+沉淀为PbCrO4,冷却后过滤洗涤沉淀。
③将PbCrO4沉淀用酸溶液溶解(离子方程式为2PbCrO4+2H+=2Pb2++Cr2O72-+H2O),加入过量KI
溶液,再用Na2S2O3标准溶液滴定到终点(滴定过程中离子方程式为:I2+2S2O32-=2I-+S4O62-)。
(1)已知Pb的原子序数是82,请写出Pb位于周期表的第_____周期______族。
(2)在PbCrO4浊液中加入少量酸,则Ksp(PbCrO4)________(填“增大”、 “减小”、“不变”)
(3)写出步骤③中加入过量KI后溶液中发生反应的离子反应方程式________。
(4)欲求试样中Pb3O4的质量分数,还需要的数据有。
(5)Fe3O4与Pb3O4相似,其氧化物和盐的形式分别是________、________。
高二化学填空题中等难度题查看答案及解析
-
下列有关物质用途的描述不正确的是( )
A.氧化铁可制作防锈油漆
B.碳酸氢钠可制作焙制糕点的发酵粉
C. 氯气不能用来合成药物,因为它有毒
D.NO能促进血管扩张,防止血管栓塞
高二化学选择题简单题查看答案及解析
-
下列有关物质用途的描述不正确的是
A.氧化铁可制作防锈油漆 B.碳酸氢钠可制作烘焙糕点的发酵粉
C.氯气不能用来合成药物,因为它有毒 D.NO能促进血管扩张,防止血管栓塞
高二化学选择题简单题查看答案及解析
-
请阅读下列材料,回答下列小题
将一定比例的三氧化硫和水混合可制得硫酸。硫酸是一种重要的化工原料,用途十分广泛,除用于化学工业外,还非常广泛应用于肥料、非碱性清洁剂、护肤品、油漆添加剂与炸药的制造等方面。
1.关于浓硫酸的说法正确的是
A.易挥发
B.见光分解
C.密度比水的小
D.常温下能使铝片钝化,浓硫酸作氧化剂
2.稀硫酸可以用于实验室制氢气,反应方程式为Zn+H2SO4=ZnSO4+H2↑,该反应的反应类型说法正确的是
A.化合反应 B.复分解反应 C.置换反应 D.分解反应
3.在其他条件不变的情况下,欲提高硫酸与锌反应产生氢气的速率,可以采用的措施有
A.选用颗粒更大的锌粒
B.升高反应温度
C.用98%浓硫酸来代替稀硫酸反应
D.加入硫酸钾溶液
4.下列反应中,生成物总能量高于反应物总能量的是
A.S+O2
SO2
B.CaO+H2O=Ca(OH)2
C.C+CO2
2CO
D.Zn+H2SO4=ZnSO4+H2↑
高二化学选择题组中等难度题查看答案及解析
-
下列有关物质用途的叙述中,错误的是( )
A. 氧化铝可用于制造耐火坩埚 B. 二氧化硫可用来漂白食品
C. 氧化铁可用作红色油漆和涂料 D. 硅酸钠溶液可用作木材防火剂
高二化学单选题简单题查看答案及解析
-
下列关于物质的用途的说法不正确的是
A. 磁性氧化铁可用于制备红色颜料和油漆
B. 氢氧化铝、碳酸氢钠可用于治疗胃酸过多
C. 钢罐可用于储运浓硫酸
D. SO2可用于漂白纸浆
高二化学单选题简单题查看答案及解析
-
下列表述不正确的是( )
A.人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3
B.硅是制造太阳能电池的常用材料
C.四氧化三铁俗称铁红,可用于作油漆、红色涂料
D.分散系中分散质粒子的直径:Fe(OH)3 悬浊液>Fe(OH)3 胶体>FeCl3 溶液
高二化学选择题中等难度题查看答案及解析
-
下列有关物质用途的说法中,正确的是
①Fe2O3常用作红色油漆和涂料 ②碳酸氢钠可用于治疗胃酸过多
③二氧化硅可用于制造光导纤维 ④Cl2可以用来制备漂白粉
A.只有①② B.只有②③ C.只有①②③ D.全部正确
高二化学单选题中等难度题查看答案及解析
-
碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用.
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体.已知室温下,0.1mol燃料完全燃烧释放出的能量为255kJ,请写出该反应的热化学方程式__ ;
(2)298K时,在2L的密闭容器中,发生可逆反应2NO2(g)
N2O4(g)△H=-a kJ•mol-1 (a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题.
① 298k时,该反应的平衡常数为___________;②若反应在398K进行,某时刻测得n(NO2)=0.6mol,n(N2O4)=1.2mol,则此时V(正)_ _V(逆)(填“>”、“<”或“=”).

③在温度为T1、T
2时,平衡体系中NO2的体积分数随压强变化曲线如图3所示。下列说法正确的是___________
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B=C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
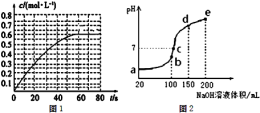
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛.现向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示.试分析图中a、b、c、d、e五个点,①水的电离程度最大的是___________,②其溶液中c(OH-)的数值最接近NH3•H2O的电离常数K数值的是___________。
高二化学填空题困难题查看答案及解析
-
下列有关物质用途的说法中,不正确的是
A.Fe2O3俗称铁红,常用作红色油漆和涂料
B.硅是良好的半导体材料
C.二氧化硅可用于制造光导纤维
D.煤炭是清洁能源,直接燃烧不会造成环境污染
高二化学选择题简单题查看答案及解析