-
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。目前我国已经在技术上取得突破——从硫酸渣中分离出各种成分并加以利用。其流程和相关数据如下:
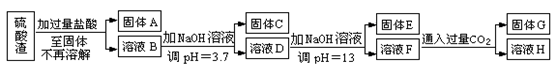
查资料得知:
| 物质名称 | 溶度积(Ksp) | pH值 |
| 开始沉淀 | 完全沉淀 |
| Mg(OH)2 | 5.6×10-12 | 9.3 | 10.8 |
| Fe(OH)3 | 2.8×10-16 | 2.7 | 3.7 |
| Al(OH)3 | 1.3×10-33 | 3.7 | 4.7 |
请回答下列问题:
(1)写出固体A的化学式为________。
(2)若要测定溶液的pH是否达到3.7,下列实验用品中可选用的是________。
A.石蕊试液 B.广泛pH试纸 C.精密pH试纸 D.pH计
(3)完成下列离子反应方程式
①溶液D生成固体E________; ②溶液F生成固体G________。
(4)要将固体C、固体E和固体G都转化为相应的稳定氧化物,需进行的实验操作为________。
(5)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)=________。
-
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3 (约10%)和MgO(约5%)。其同学设计了如下方案,分离样品中各种金属元素。
已知: Fe(OH)3的Ksp=4.0×10-38。请回答下列问题。
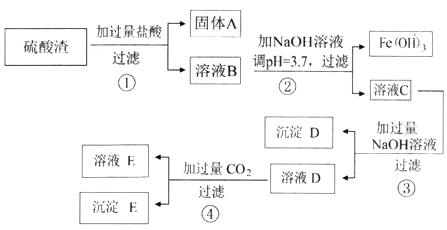
(1) 固体A的一种工业应用________;沉淀D的电子式___________。
(2) 溶液B中所含的金属阳离子有___________。(写离子符号)
(3) 若步骤②中调pH 为3.0,则溶液C中的Fe3+ 是否沉淀完全,通过计算说明______。
(4) 写出步骤④中全部反应的离子方程式_______________。
(5) 为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元索还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①判断到达滴定终点的现象是__________。
②某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL 溶液,移取25.00mL 试样溶液,用0.0050 mol/L KMnO4标准溶液滴定,达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是_________________。
-
(10分)硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%)。某同学设计了如下方案,分离样品中各种金属元素。请回答下列问题。

(1)写出溶液B的溶质是 。
(2)参照以下框图形式进一步完成“溶液C”到“Al2O3”的流程(注明试剂、条件和操作) 。
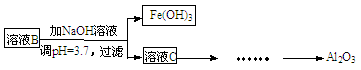
(3)为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。写出反应的离方程式: 。
-
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2:约45%,Fe2O3:约40%,Al2O3:约10%,MgO:约5%.目前我国已经在技术上取得突破--用硫酸渣炼铁.
I.某学生探究性学习小组的同学设计了不同的方案,用化学基本知识进行金属元素的提取实验(已知25℃氢氧化镁Ksp=5.6×10-12;氢氧化铁Ksp=3.5×10-38;一水合氨电离常数K=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol•L-1).
方案一:
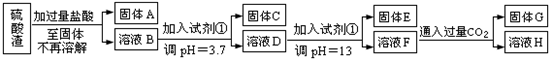
请回答:
(1)写出固体E的化学式:______.
(2)试剂①是______
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(3)若要准确测定溶液的pH是否达到3.7,下列物品中可供使用的是______
A.石蕊试液 B.广泛pH试纸 C.精密pH试纸 D.pH计
(4)溶液H中溶质的化学式:______
(5)要将固体C、固体E和固体G都转化为相应的稳定的氧化物,需进行的实验操作为______.
(6)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)=______.
方案二:
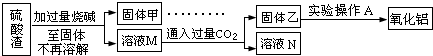
请回答:
(7)此方案的主要问题有:______
(8)写出由溶液M→固体乙这个过程中,最主要化学反应的离子方程式:______
II.为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(1)判断到达滴定终点的现象是______.
(2)某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移取25.00mL,试样溶液,用1.000×10-2mol•L-1KMnO4标准溶液滴定.达到滴定终点时,消耗标准溶液10.00mL,则残留物中铁元素的质量分数是______.
-
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2:约45%,Fe2O3:约40%,Al2O3:约10%,MgO:约5%.目前我国已经在技术上取得突破--用硫酸渣炼铁.Fe3+开始沉淀为氢氧化物的PH=1,沉淀完全时的PH为3.7.
I.某探究性学习小组的同学设计了不同的方案,用化学基本知识进行金属元素的提取实验。
方案一:

请回答:
(1)写出固体E的化学式:______________.试剂①是__________(填选项字母).
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(2)若要准确测定溶液的pH是否达到3.7,下列物品中可供使用的是__________(填选项字母).
A.石蕊试液 B.广泛pH试纸 C.pH计
(3)溶液H中溶质的化学式:______________
(4)要将 固体C、固体E和固体G都转化为相应的稳定的氧化物,需进行的实验操作为________________.
固体C、固体E和固体G都转化为相应的稳定的氧化物,需进行的实验操作为________________.
方案二:

(5) 此方案制得的氧化铝含有的主要杂质是_________________。
此方案制得的氧化铝含有的主要杂质是_________________。
(6)写出由溶液M→固体乙这个过程中,主要化学反应的离子方程式:_______________;_______________。
(7)为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:_______________。
(8)某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移取25.00mL试样溶液,用1.000×10-2mol•L-1KMnO4标准溶液滴定.达到滴定终点时,消耗标准溶液10.00mL,则残留物中铁元素的质量分数是_____________.
-
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2:约45%,Fe2O3:约40%,Al2O3:约10%,MgO:约5%。目前我国已经在技术上取得突破――用硫酸渣炼铁。Fe3+开始沉淀为氢氧化物的pH=1,沉淀完全时的pH为3.7。某学生探究性学习小组的同学设计了不同的方案,用化学基本知识进行金属元素的提取实验。
方案一:
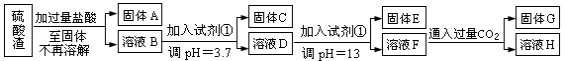
请回答:
(1)写出固体E的化学式:__________________。试剂①是_______
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(2)若要准确测定溶液的pH是否达到3.7,下列物品中可供使用的是_________
A.石蕊试液 B.广泛pH试纸 C.pH计
(3)溶液H中溶质的化学式:__________________
(4)要将固体C、固体E和固体G都转化为相应的稳定的氧化物,需进行的实验操作为 。
方案二:
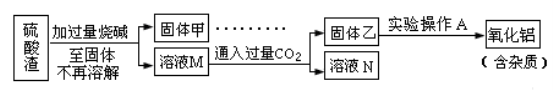
(5)此方案制得的氧化铝含有的主要杂质是:_______________
(6)写出由溶液M固体乙这个过程中,主要化学反应的离子方程式:
_____________________;___________________
-
从古至今,铁及其化合物在人类生产、生活中的作用发生了巨大的变化。
(1)现代工业“接触法制硫酸”用黄铁矿(主要成分为FeS2)为原料。测得硫酸渣的化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
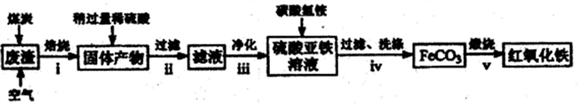
请回答下列问题:
①在步骤i中产生的有毒气体可能有___________________。
②在步骤iii操作中,要除去的离子之一为Al3+,若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上将Al3+沉淀完全,则溶液的pH为_________(注:c(Al3+)≤10-5mol·L-1视为沉淀完全)。
③步骤ⅳ中,洗涤沉淀的操作是___________________。
生成FeCO3的离子方程式是__________________。
(2)氯化铁溶液称为化学试剂中的“多面手”,向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式_____________。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释:______________________。
(3)古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ⅱ的离子方程式是________________________________________。
-
以工业生产硼砂所得废渣硼镁泥为原料制取MgSO4·7H2O的过程如图所示:
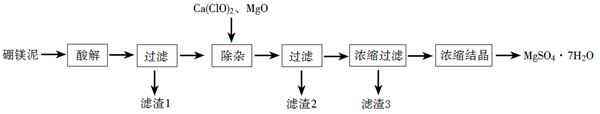
硼镁泥的主要成分如下表:
| MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
| 30%~40% | 20%~25% | 5%~15% | 2%~3% | 1%~2% | 1%~2% |
回答下列问题:
(1)“酸解”时应该加入的酸是_______,“滤渣1”中主要含有_________(写化学式)。
(2)“除杂”时加入次氯酸钙、氧化镁的作用分别是________、_______。
(3)判断“除杂”基本完成的检验方法是____________。
(4)分离滤渣3应趁热过滤的原因是___________。
-
以工业生产硼砂所得废渣硼镁泥为原料制取MgSO4·H2O的过程如图所示:
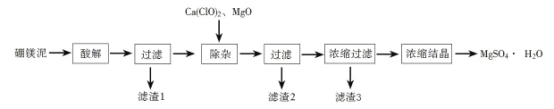
硼镁泥的主要成分如下表:
| MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
| 30%〜40% | 20%~25% | 5%〜15% | 2%~3% | 1%〜2% | 1%〜2% |
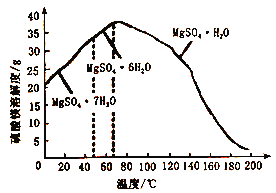
资料:B2O3溶于水形成硼酸,由于硼酸易溶于水,溶解度随温度的升高而升高,而硫酸镁在80℃溶解度最大,所以常规方法很难将二者分离,目前常采用高温结晶法。
回答下列问题:
(1)“滤渣1”中主要含有_________(写化学式)。
(2)“滤渣2”中主要含有_________(写化学式),判断”除杂"基本完成的检验方法正确的是
A.取上层清液,滴加苯酚试液不显紫色
B.取上层淸液,滴加KSCN,不变红
C.取上层清液,滴加K3[Fe(CN)6]不产生蓝色沉淀
(3)氧化镁的作用是______。有同学认为用碳酸镁比用氧化镁要好,原因是________。
(4)分离滤渣3应趁热过滤的原因是___________。分离滤渣3后的母液中含有的溶质是_____和_____,可以采用加压、_____的方法得到一水合硫酸镁。
-
硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质)。用该烧渣制取药用辅料——红氧化铁的工艺流程如下:

(1)在“还原焙烧”中产生的有毒气体可能有。
(2)“酸浸”时间一般不超过20 min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因用离子方程式表示:________。
(3)根据下表数据:
| 氢氧化物 | Al(OH)3 | Mg(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 3.10 | 8.54 | 2.01 | 7.11 |
| 完全沉淀的pH | 4.77 | 11.04 | 3.68 | 9.61 |
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于________,当pH=5时,溶液中c(Al3+)为________mol·L-1(已知常温下Ksp[Al(OH)3]=2.0×10-33)。
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,碳酸氢铵与硫酸亚铁反应的离子方程式为。
若用等物质的量的碳酸铵替代碳酸氢铵,则产品中可能混有的杂质是________。
(5)A的操作是________。
(6)m g烧渣经过上述工艺可得红氧化铁n g。药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含m、n的表达式表示)。

固体C、固体E和固体G都转化为相应的稳定的氧化物,需进行的实验操作为________________.

此方案制得的氧化铝含有的主要杂质是_________________。













