-
氮及其化合物与人类各方面有着密切的联系。目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol
③H2O(g)= H2O(l) △H=-44kJ/mol
写出CH4(g)与NO2(g)反应生成N2(g) 、CO2(g)和H2O ( l ) 的热化学方程式____________________。
(2)用活性炭还原法处理氮氧化物,有关反应为:
某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T0C)条件下反应,反应进行到不同时间测得各物质的浓度如下:
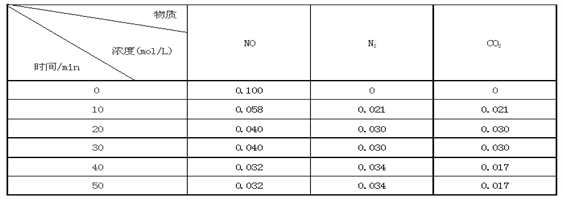
①不能作为判断反应达到化学平衡状态的依据是_______ ;(选填字母代号)
A.容器内CO2的浓度保持不变 B.容器内压强保持不变
C.单位时间内生成NA个N2,同时生成2NA个NO
D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②前20分钟,平均反应速率v(NO)=_________________。
③在T0C时,该反应的平衡常数表达式为_______________________________;
④在30 min,改变某一条件反应重新达到平衡,则改变的条件是______________________________。
(3)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2,其反应为:


如图P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1mol NO(g)和2mol(g)CO,向B容器中充入1.2 mol NO(g)和2.4 mol(g) CO。已知起始时容器A和B的体积均为a L,反应到到平衡时容器B的体积为0.9 a L,容器B中NO的转化率为_____________ ;
(4)亚硝酸(HNO2)是弱酸电离平衡常数 Ka=5.0×10 -4(298K), NH3.H2O的电离平衡常数为
K=2.0×10 -5常温下,用氨水吸收亚硝酸可得到NH4NO2,NH4NO2溶液显_____(填“酸性”“中性”或“碱性”);请计算NH4+ + NO2- + H2O HNO2 + NH3.H2O的平衡常数K =_________。
HNO2 + NH3.H2O的平衡常数K =_________。
-
目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
写出CH4 (g)与NO2 (g)反应生成N2 (g) ,CO2(g)和H2O(l)的热化学方程 式_____________________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)  N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
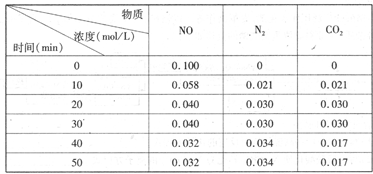
①不能作为判断反应达到化学平衡状态的依据 是_______
A.容器内CO2的浓度保持不变
B.v正(N2)=2 v正(NO)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
②在T。C时.该反应的平衡常数为_______(保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是_______
(3)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2,其反应为:
2CO+2NO  N2+2CO2 ΔH<0 研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反 应速率的影响规律、某同学设计了三组实验,部分实验条件已经填在下表中。
N2+2CO2 ΔH<0 研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反 应速率的影响规律、某同学设计了三组实验,部分实验条件已经填在下表中。

①上表中:a=_______,b=________,e=________
②请在给出的坐标图中,画出上表中实验II和实验III条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明相应的实验编号
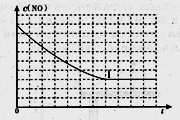
-
目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+4NO2 (g)=4NO(g)+CO2 (g)+2H2 O(g) ΔH=-574 kJ·mol-1
②CH4 (g)+4NO(g)=2N2 (g)+CO2 (g)+2H2 O(g) ΔH=-1160 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式__________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
| 浓度/mol·L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
①不能作为判断反应达到化学平衡状态的依据是_______
A.容器内CO2的浓度保持不变
B.v正(N2)=2 v正(NO)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
②在该温度下时.该反应的平衡常数为 (保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是_____________。
(3)合成塔失去活性的铬锌触媒可用于制备锌锰电池。在碱性条件下,该电池的总反应为: Zn(s) +2MnO2 (s) +H2O(l) = Zn(OH)2 (s) +Mn2O3(s) ,该电池正极的电极反应式是 。PbO2 可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生反应的电极反应式为 ,阴极上观察到的现象是; 若电解液中不加入Cu(NO3)2这样做的主要缺点是 。
-
(14分)目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
写出CH4 (g)与NO2 (g)反应生成N2 (g) ,CO2(g)和H2O(l)的热化学方程 式_____________________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)  N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
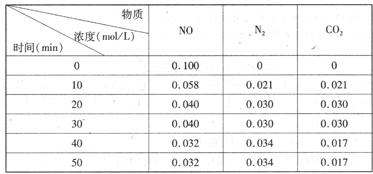
①不能作为判断反应达到化学平衡状态的依据是______________
A.容器内CO2的浓度保持不变
B.v正(N2)=2 v正(NO)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
②在T。C时.该反应的平衡常数为______________(保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是______________
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50ml2mol/L的氯化铜溶液的装置示意图:
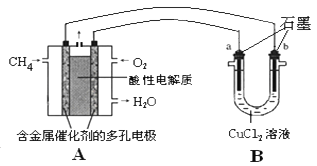
请回答:
①甲烷燃料电池的负极反应式是:__________________________。
②当A中消耗0.05mol氧气时,B中________________极(填“a”或“b”)增重________________g。
-
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少 8%,氮氧化物(NOx)排放量减少 10%。目前,消除大气污染有多种方法。
(1)用 CH4 催化还原氮氧化物可以消除氮氧化物的污染。
已知:①CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g)△H =-574 kJ/mol
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g)△H =-1160 kJ/mol
③H2O(g) = H2O(l) △H =-44.0 kJ/mol
写出 CH4(g)与 NO2(g)反应生成 N2(g)、CO2(g)和 H2O(l)的热化学方程式:__________。
(2)利用 Fe2+、Fe3+的催化作用,常温下可将 SO2 转化为 SO42-,从而实现对 SO2 的治理。已知含 SO2 的废气通入含 Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为 4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O,则另一反应的 离子方程式为__________。
(3)用活性炭还原法处理氮氧化物。有关反应为 C(s) + 2NO(g)  N2(g) + CO2(g)。某研究小组向密闭的真空 容器中(假设容器体积不变,固体试样体积忽略不计)加入 NO 和足量的活性炭,在恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g) + CO2(g)。某研究小组向密闭的真空 容器中(假设容器体积不变,固体试样体积忽略不计)加入 NO 和足量的活性炭,在恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
| 浓度(mol/L) | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
①10~20 min 以υ(N2)表示的反应速率为__________。
②该反应的平衡常数表达式 K=________。根据表中数据,计算 T1 ℃时该反应的平衡常数为__________(保留两位小数)。
③一定温度下,随着 NO 的起始浓度增大,则 NO 的平衡转化率__________ (填“增大”、“不变”或“减小”)。
④下列各项能作为判断该反应达到平衡的是__________ (填序号)。
A.混合气体的密度保持不变
B.υ正(NO) = 2υ逆(CO2)
C.容器内压强保持不变
D.容器内 N2 的体积分数保持不变
-
(15分)随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g) + CO2(g) +2H2O(g) ⊿H= -574 kJ·mol-1
②CH4(g) +4NO(g)=2N2(g) + CO2(g) + 2H2O(g) ⊿H=-1160 kJ·mol-1
③H2O(g)=H2O(l) △H=-44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2 (g)、CO2 (g)和H2O(1)的热化学方程式。
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则另一反应的离子方程式为。
(3)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2(g)+CO2(g)。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g)。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
| 浓度/mol·L-1  时间/min 时间/min
| NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
①10min~20min以v(CO2) 表示的反应速率为 ________。
②根据表中数据,计算T1℃时该反应的平衡常数为________ ________(保留两位小数)。
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率________(填“增大”、“不变”或“减小”) 。
④下列各项能作为判断该反应达到平衡的是________ ________(填序号字母)。
A.容器内压强保持不变 B.2v正(NO)=v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
⑤30min末改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是。请在右图中画出30min至40min 的变化曲线。
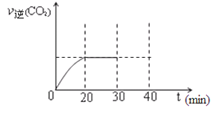
-
随着大气污染的日趋严重,国家拟于“十二”五期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g) =4NO(g) + CO2(g) +2H2O(g) ⊿H= -574 kJ·mol-1
②CH4(g) +4NO(g) =2N2(g) + CO2(g) + 2H2O(g) ⊿H= -1160 kJ·mol-1
③H2O(g) = H2O(l) △H= -44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2 (g)、CO2 (g)和H2O(1)的热化学方程式 。
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为 。
| 浓度/mol·L-1  时间/min 时间/min
| NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
(3)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2 (g)+CO2 (g) 。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2 (g)+CO2 (g) 。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
①10min~20min以v(CO2) 表示的平均反应速率为 。
②根据表中数据,计算T1℃时该反应的平衡常数为 (保留两位小数)。
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率 (填“增大”、“不变”或“减小”) 。
④下列各项能作为判断该反应达到平衡的是________________________________ ________________________ (填序号字母)。
A.容器内压强保持不变
B.2v正(NO) = v逆(N2)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
⑤30min末改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是 。请在图中画出30min至40min 的变化曲线。
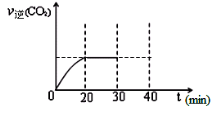
-
(14分)硝酸厂废气、汽车尾气中的氮氧化物可污染大气,现有几种消除氮氧化物的方法如下:
目前,消除氮氧化物污染有多种方法。
(1)方法一:CH4催化还原法。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2
③H2O(g)=H2O(l) ΔH3=-44 kJ·mol-1
现有一混合气体中NO与NO2的体积比为3:1,用22.4L(标准状况下)甲烷气体催化还原该混合气体,恰好完全反应(已知生成物全部为气态),并放出1042.8KJ的热量,则ΔH2为_____________;写出CH4 (g)与NO2 (g)反应生成N2 (g) 、CO2(g)和H2O(l)的热化学方程式_________________________。
(2)方法二:活性炭还原法。
某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T1 ℃)条件下反应,只生成甲和乙,甲和乙均为参与大气循环的气体,且反应进行到不同时间测得各物质的浓度如下:
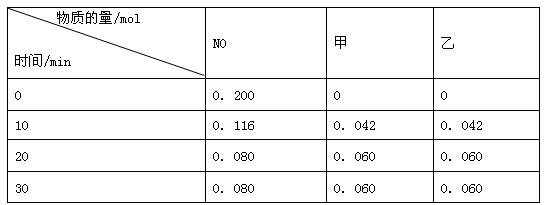
由以上信息可知:
①该原理的化学方程式为____________________________________________________.
②该温度下的平衡常数K=_____________________________。(保留小数点后两位有效数字)
③若20min后升高温度至T2℃,达到平衡后,若容器中NO、甲、乙的浓度之比为1:1:1,则该反应的ΔH_____0 。(填">"、"<"、"=")
(3)方法三:NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。
反应原理为:2NH3(g)+NO(g)+NO2(g)  2N2(g)+3H2O(g) 每生成1molN2转移的电子数为_____________________________________________________________。
2N2(g)+3H2O(g) 每生成1molN2转移的电子数为_____________________________________________________________。
(4)方法四:ClO2氧化氮氧化物。其转化流程如下:
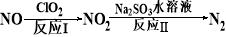
已知反应Ⅰ的化学方程式为2NO+ ClO2 + H2O = NO2 + HNO3 + HCl,则反应Ⅱ的化学方程式是 。
-
(14分)硝酸厂废气、汽车尾气中的氮氧化物可污染大气,现有几种消除氮氧化物的方法如下:
目前,消除氮氧化物污染有多种方法。
(1)方法一:CH4催化还原法。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2
③H2O(g)=H2O(l) ΔH3=-44 kJ·mol-1
现有一混合气体中NO与NO2的体积比为3:1,用22.4L(标准状况下)甲烷气体催化还原该混合气体,恰好完全反应(已知生成物全部为气态),并放出1013.5KJ的热量,则ΔH2为______;写出CH4 (g)与NO2 (g)反应生成N2 (g) 、CO2(g)和H2O(l)的热化学方程式_______________________。
(2)方法二:活性炭还原法。
某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T1 ℃)条件下反应,只生成甲和乙,甲和乙均为参与大气循环的气体,且反应进行到不同时间测得各物质的浓度如下:
|  物质的量/mol 物质的量/mol
时间/min | NO | 甲 | 乙 |
| 0 | 0.200 | 0 | 0 |
| 10 | 0.116 | 0.042 | 0.042 |
| 20 | 0.080 | 0.060 | 0.060 |
| 30 | 0.080 | 0.060 | 0.060 |
由以上信息可知:
①该原理的化学方程式为____________________________________________________.
②该温度下的平衡常数K=_____________________________。(保留小数点后两位有效数字)
③若20min后升高温度至T2℃,达到平衡后,若容器中NO、甲、乙的浓度之比为1:1:1,
则该反应的ΔH_______ 0 。(填">"、"<"、"=")
(3)方法三:NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。
反应原理为:2NH3(g)+NO(g)+NO2(g)  2N2(g)+3H2O(g) 每生成1molN2转移的电子数为_____________________________________________________________。
2N2(g)+3H2O(g) 每生成1molN2转移的电子数为_____________________________________________________________。
(4)方法四:ClO2氧化氮氧化物。其转化流程如下:
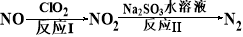
已知反应Ⅰ的化学方程式为2NO+ ClO2 + H2O = NO2 + HNO3 + HCl,则反应Ⅱ的化学方程式是 。
-
碳、氮及其化合物在工农业生产生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) = 2 N2(g)+CO2(g) + 2H2O(g) ΔH2
若2 mol CH4 还原NO2 至N2,整个过程中放出的热量为1734 kJ,则ΔH2= ;
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应如下: Fe2O3(s) + 3CH4(g)  2Fe(s) + 3CO(g) +6H2(g) ΔH>0
2Fe(s) + 3CO(g) +6H2(g) ΔH>0
① 若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g。则该段时间内CO的平均反应速率为 ________________ 。
② 若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是_____(选填序号)
a.CH4的转化率等于CO的产率
b.混合气体的平均相对分子质量不变
c.v(CO)与v(H2)的比值不变
d.固体的总质量不变
③ 该反应达到平衡时某物理量随温度变化如图所示,当温度由T1升高到T2时,平衡常数KA ______KB(填“>”、“ <”或“=”)。纵坐标可以表示的物理量有哪些 。
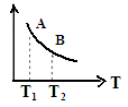
a.H2的逆反应速率
b.CH4的的体积分数
c.混合气体的平均相对分子质量
(3)若往20mL 0.0lmol·L-l的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是________
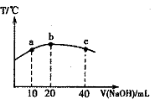
①该烧碱溶液的浓度为0.02mol·L-1
②该烧碱溶液的浓度为0.01mol·L-1
③ HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH )> c(H+)
)> c(H+)

HNO2 + NH3.H2O的平衡常数K =_________。