-
CO(NH2)2(尿素)在制备氢气,碳酸二甲酯及烟气脱硫、脱硝等方面有着广泛的应用。回答下列问题:
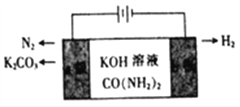
(1)电解尿素的碱性溶液制备氢气的装置如右图所示,a极是________;通电时,阴极周围溶液的pH________(填“增大”或“减小”);阳极的电极反应式为________。
(2)尿素合成碳酸二甲酯的相关反应及平衡常数的对数值与温度的关系如下:
(Ⅰ)2CH3OH(l)+CO(NH2)2(1) CH3OCOOCH3(l)+2NH3(g)△H1
CH3OCOOCH3(l)+2NH3(g)△H1
(Ⅱ)CH3OH(l)+CO(NH2)2(l) CH3OCONH2(l)+NH3(g) △H2
CH3OCONH2(l)+NH3(g) △H2
(Ⅲ)CH3OCONH2(l)+CH3OH(l) CH3OCOOCH3(l)+NH3(g) △H3
CH3OCOOCH3(l)+NH3(g) △H3
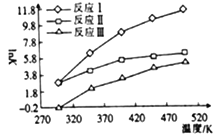
①△H1=_______(用△H2和△H3表示);平衡常数的对数lnK(Ⅰ)=________[用lnK(Ⅱ)和lnK(Ⅲ)表示]。
②对于反应(Ⅱ),升高温度,化学平衡向________(“正”或“逆”)反应方向移动。
③为提高CH3OCOOCH3的产率,可采取的措施有________________________________(列举2点)。
(3)尿素中添加NaClO2 所得混合溶液可用于烟气脱硫、脱硝。用含NO和SO2的混合烟气进行实验。混合液中NaClO2的质量分数与NO和SO2的脱除率关系如图所示。

①含SO2的烟气(含O2)通过尿素溶液得到的盐为_________;NO2与尿素溶液反应。生成N2和另外两种氧化物,写出该反应的化学方程式:_______________________________。
②若用纯尿素溶液,则NO的脱除率仅约为15%,说明NaClO2的作用是_____________。
③SO2的脱除率总是比NO的大,其原因是____________________________(列举2点)。
-
铝电池性能优越,在工业上有广泛的应用。如图为用Al-Ag2O2电池电解尿素[CO(NH2)2]碱性溶液制氢气(隔膜II仅阻止气体通过,a、b均为惰性电极)的装置。下列说法不正确的是( )

A.电池工作时,电解质溶液中Na+移向Ag电极
B.Al电极的电极反应为Al-3e-+3OH-=Al(OH)3
C.a电极上的电极反应为CO(NH2)2+8OH--6e-=CO32- +N2↑+6H2O
D.电池工作时,若有1molAg2O2在电极放电,理论上可以获得氢气44.8L(标准状况)
-
铝电池性能优越,在工业上有广泛的应用。如图为用Al-Ag2O2电池电解尿素[CO(NH2)2]碱性溶液制氢气(隔膜II仅阻止气体通过,a、b均为惰性电极)的装置。下列说法不正确的是( )
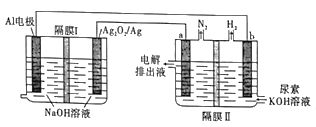
A.电池工作时,电解质溶液中Na+移向Ag电极
B.Al电极的电极反应为Al-3e-+3OH-=Al(OH)3
C.a电极上的电极反应为CO(NH2)2+8OH--6e-=CO32- +N2↑+6H2O
D.电池工作时,若有1molAg2O2在电极放电,理论上可以获得氢气44.8L(标准状况)
-
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
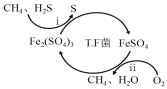
(1)过程i的离子反应方程式为_______________________。
(2)已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
| pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
| Fe2+的氧化速/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
在转化脱硫中,请在上表中选择最佳pH范围是_______<pH<_______,这样选择的原因是:____。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
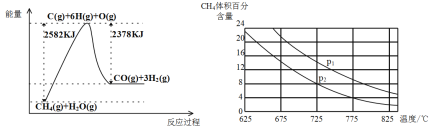
(3)①该过程的热化学方程式是___________。
②比较压强P1和p2的大小关系:P1________P2(选填“>”“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1mol CH4和1mol的水蒸气充分反应达平衡后,测得起始时混合气的密度是平衡时混合气密度的1.4倍,若此时容器的体积为2L,则该反应的平衡常数为______________(结果保留2位有效数字)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程如示意图
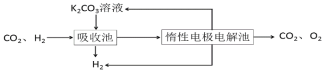
(4)①吸收池中发生反应的离子方程式是______________。
②结合电极反应式,简述K2CO3溶液的再生原理:_____。
-
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
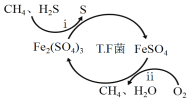
(1)过程i的离子反应方程式为_________________________________________。
(2)已知:
①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
| pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
| Fe2+的氧化速率/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
在转化脱硫中,请在上表中选择最佳pH范围是_______<pH<_______,这样选择的原因是:_______________________________________________。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
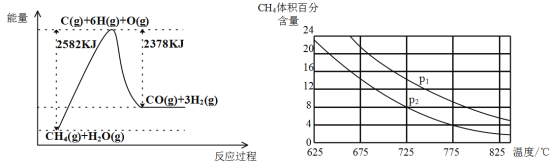
(3)①该过程的热化学方程式是__________________________________________。
②比较压强P1和p2的大小关系:P1 _________ P2(选填“>”“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1molCH4和1mol的水蒸气充分反应达平衡后,测得起始时混合气的密度是平衡时混合气密度的1.4倍,若此时容器的体积为2L,则该反应的平衡常数为______________(结果保留2位有效数字)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程如示意图
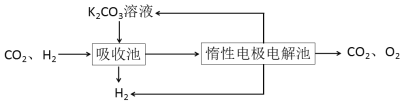
(4)吸收池中发生反应的离子方程式是____________________________________。
-
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。

(1)过程i的离子反应方程式为_________________________________________。
(2)已知:
①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
| pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
| Fe2+的氧化速率/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
在转化脱硫中,请在上表中选择最佳pH范围是_______<pH<_______,这样选择的原因是:_______________________________________________。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
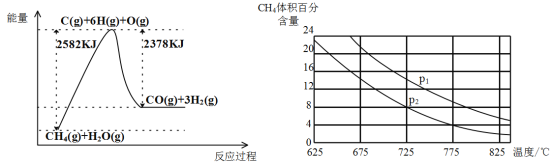
(3)①该过程的热化学方程式是__________________________________________。
②比较压强P1和p2的大小关系:P1 _________ P2(选填“>”“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1molCH4和1mol的水蒸气充分反应达平衡后,测得起始时混合气的密度是平衡时混合气密度的1.4倍,若此时容器的体积为2L,则该反应的平衡常数为______________(结果保留2位有效数字)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程如示意图
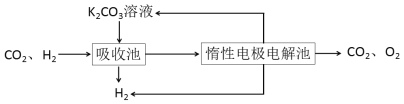
(4)吸收池中发生反应的离子方程式是____________________________________。
-
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如图。
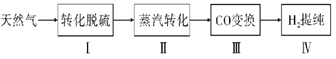
请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T·F菌作用下,酸性环境中脱硫过程示意图如下。
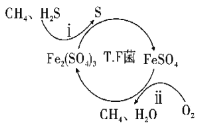
(1)过程i的离子反应方程式为__。
(2)已知:
①Fe3+在pH=1.9时开始沉淀pH=3.2时沉淀完全。
②30℃时,在T·F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
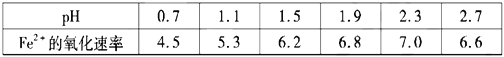
下列说法正确的是___
A.在转化脱硫中,最佳的pH范围是1.5<pH<1.9
B.在转化脱硫中需要不断补充Fe2(SO4)3
C.在转化脱硫中是O2间接地把H2S氧化为S
D.在转化脱硫中CH4作为还原剂被氧化
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。

(3)①该过程的热化学方程式是__。
②比较压强p1和p2的大小关系:p1__p2(选填“<”、“>”或“=”)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.提纯:将CO2和H2分离得到H2的过程示意图如图。
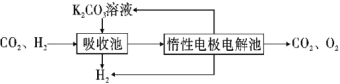
(4)吸收池中发生反应的离子方程式是__。
-
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。
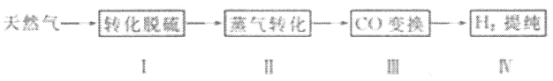
请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如图所示。

(1)过程i中H2S发生了___(填“氧化”或“还原”)反应。
(2)过程ii的离子方程式是___。
(3)已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
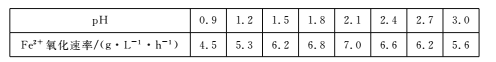
| pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
| Fe2+氧化速率/(g·L-1·h-1) | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
请结合以上信息,判断工业脱硫应选择的最佳pH范围,并说明原因:___。
II.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。
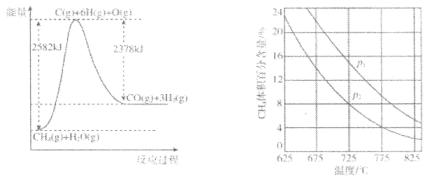
(4)①该过程的热化学方程式是___。
②比较压强p1和p2的大小关系:p1___p2(选填“>”“<”或“=”)。
III.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
IV.H2提纯:将CO2和H2分离得到H2的过程示意图如图。
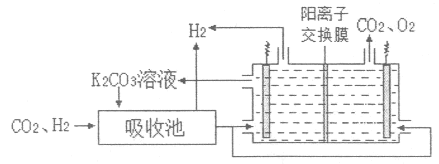
(5)①吸收池中发生反应的离子方程式是___。
②结合电极反应式,简述K2CO3溶液的再生原理:___。
-
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。
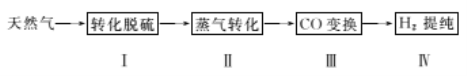
请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
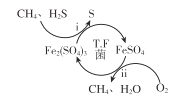
(1)过程i中H2S发生了 ___(选填“氧化”或“还原”)反应。
(2)过程ⅱ的离子方程式是____。
(3)已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeS04溶液中Fe2+的氧化速率如下表。
请结合以上信息,判断工业脱硫应选择的最佳pH范围,并说明原因:____。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
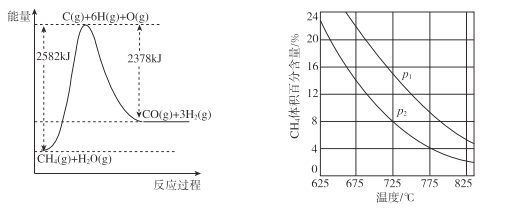
(4)①该过程的热化学方程式是____。
②比较压强P1和p2的大小关系:p1 __ p2(选填“>”“<”或“=”)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程示意图如下。

(5)①吸收池中发生反应的离子方程式是 ___。
②结合电极反应式,简述K2CO3溶液的再生原理:____。
-
已知H2O2是一种弱酸,在强碱溶液中主要以HO2-形式存在。现以Al—H2O2燃料电池电解尿素[CO(NH2)2]的碱性溶液制备氢气 (电解池中隔膜仅阻止气体通过,c、d均为惰性电极)。下列说法正确的是
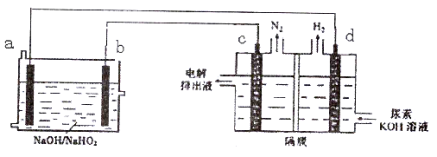
A.燃料电池的总反应为:2Al+3HO2- = 2AlO2- + 2H2O
B.电解时,Al消耗2.7g,则产生氮气的体积为1.12L
C.电极b是负极,且反应后该电极区pH增大
D.电解过程中,电子的流向由a→d,c→b。

CH3OCOOCH3(l)+2NH3(g)△H1
CH3OCONH2(l)+NH3(g) △H2
CH3OCOOCH3(l)+NH3(g) △H3






























