-
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:

回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g)2SO3(g),该反应的平衡常数表达式为K=________;过量的SO2与NaOH溶液反应的化学方程式为
_____________________________________________________________。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是________、________。
(3)通氯气氧化时,发生的主要反应的离子方程式为____________;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为________(写化学式)。
-
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:

回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g) 2SO3(g) ,该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为
2SO3(g) ,该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为
(2)酸溶及后续过程中均需保持盐酸过量,其目的是 、 。
(3)通氯气氧化后时,发生的主要反应的离子方程式为 ;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为 (写化学式)。
-
(12分)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:

回答下列问题:
(1)硫铁矿高温焙烧的化学方程式为________; 少量的SO2与NaOH溶液反应的离子方程式为________。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率和________ ,
题问所涉及反应的离子方程式为________。
(3)通氯气氧化时,发生的主要反应的离子方程式为________ ;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为________________________(写化学式)。
-
某化学兴趣小组以菱铁矿(主要成分为FeCO3,含有SiO2、Al2O3等少量杂质)为原料制备氯化铁晶体(FeCl3·6H2O)的实验过程如下:
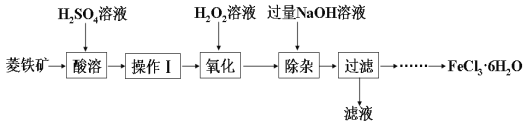
(1)酸溶及后续过程中均需保持酸过量,其目的除了提高铁元素的浸出率之外,还有___________。
(2)操作Ⅰ名称是___________。
(3)滴加H2O2溶液氧化时,发生主要反应的离子方程式为___________。
(4)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3−=Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4−= Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是___________。 (仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(5)加入过量NaOH溶液的目的是___________。
(6)请补充完整由过滤后得到的固体制备FeCl3·6H2O的实验方案:向过滤后所得固体,用水洗涤固体2-3次,低温干燥,得到FeCl3·6H2O。___________
-
以硫铁矿(主要成分为 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下所示:
)的工艺流程如下所示:
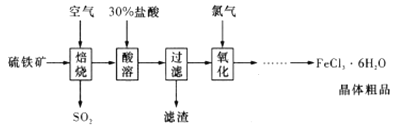
下列说法不正确的是
A. “酸溶”过程中使用的酸也可以是硝酸
B. 为防止污染,“焙烧”过程中产生的 应回收利用
应回收利用
C. 通入氯气的目的是氧化
D. 用 制取无水
制取无水 时,需要在氯化氢气流中加热
时,需要在氯化氢气流中加热
-
以镍黄铁矿为原料制备 的工艺流程如下:
的工艺流程如下:
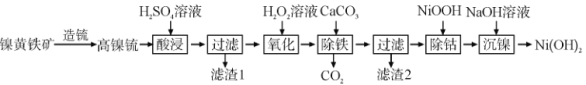
已知:①高镍锍的主要成分为 、
、 、
、 、
、 的低价硫化物及合金;
的低价硫化物及合金;
②氧化性: ;
;
③ ,
, ,
, 。
。
回答下列问题:
(1)“酸浸”时, 溶液需过量,其目的是________。
溶液需过量,其目的是________。
(2)“氧化”时反应的化学方程式为________,若用 代替
代替 溶液,使
溶液,使 转化为
转化为 ,则需
,则需 至少为________
至少为________ 。
。
(3)“除铁”的原理是________。
(4)“过滤”时滤渣1的主要成分是________。
(5)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是________________。若“沉镍”后的滤液中 ,则滤液的
,则滤液的 ________。
________。
(6)“除钴”时,发生反应的离子方程式为________。
-
四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成为是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:
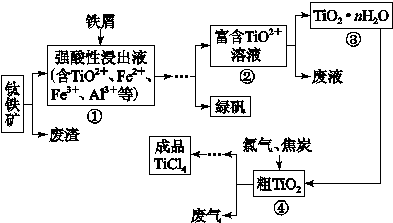
回答下列问题:
往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe=3Fe2+
2TiO2+(无色)+Fe+4H+=2Ti3+(紫色) +Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
加入铁屑的作用是。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在________范围。
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可以制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+ Fe3++3H2O的平衡常数K=________。
Fe3++3H2O的平衡常数K=________。
(4)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式: ________。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是________ (只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4的,可采用________方法。
| TiCl4 | SiCl4 |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
-
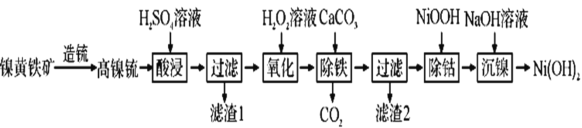
以镍黄铁矿为原料制备 的工艺流程如下:
的工艺流程如下:
已知:①高镍锍的主要成分为 、
、 、
、 、
、 的低价硫化物及合金;
的低价硫化物及合金;
②氧化性: ;
;
③ ,
,  ,
, 。
。
回答下列问题:
(1)“酸浸”时,H2SO4溶液需过量,其目的是________。
(2)“过滤”时滤渣1的主要成分是________。
(3)“氧化”时反应的化学方程式为_________,若用NaClO代替H2O2溶液,使0.2molFe2+转化为Fe3+,则需NaClO至少为___mol。
(4)“除铁”的原理是_________。
(5)“除钴”时,发生反应的离子方程式为____________。
(6)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是_____。若“沉镍”后的滤液中 ,则滤液的pH>____
,则滤液的pH>____
-
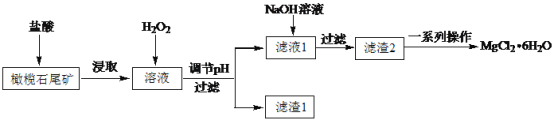
实验室利用橄榄石尾矿(主要成分为MgO及少量FeO、Fe2O3、Al2O3等)制备纯净氯化镁晶体(MgCl2·6H2O),实验流程如下:
已知几种金属阳离子形成氢氧化物沉淀时的pH如下表:
| Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时 | 7.6 | 2.7 | 4.2 | 9.6 |
| 沉淀完全时 | 9.6 | 3.7 | 5.4 | 11.1 |
回答下列问题:
(1)“浸取”步骤中,能加快浸取速率的方法有____(任写一种)。
(2)滤渣1为Fe(OH)3,则调节pH的范围为____。
(3)“一系列操作”主要包括加入足量盐酸,然后经过蒸发浓缩、冷却结晶、过滤、洗涤,即得到氯化镁晶体。加入足量盐酸的作用为①溶解滤渣2,②____。
(4)准确称取2.000 g氯化镁晶体产品于250 mL锥形瓶中,加50 mL蒸馏水使其完全溶解,在不断振荡下,调节pH并加入合适的指示剂,用0.5000 mol/L的EDTA(在方程式中用Y4−表示)标准溶液进行滴定,其反应原理为Mg2++Y4− = MgY2−,滴定达到终点时消耗EDTA标准溶液的体积为19.00 mL。
①计算产品中MgCl2·6H2O的质量分数。____(写出计算过程,结果保留三位有效数字)。
②下列滴定操作会导致测量结果偏高的是____(填字母)。
a.滴定终点时仰视读数
b.锥形瓶洗涤后没有干燥
c.滴定时锥形瓶中有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
-
锶(Sr)为第五周期ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
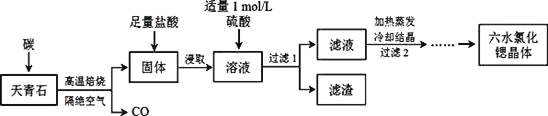
已知:① 经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
② SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③ SrCl2·6H2O的摩尔质量为:267 g/mol。
(1)天青石焙烧前先研磨粉碎,其目的是___________________。
(2)隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:_____________________________________________。
(3)为了得到较纯的六水氯化锶晶体,过滤2后还需进行的两步操作是_______________。
(4)加入硫酸的目的是______________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________mol/L(注:此时滤液中Ba2+浓度为1×10-5mol/L)。
(5)产品纯度检测:称取1.000g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2mol的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应的离子),待Cl―完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______(保留4位有效数字)。









