-
有三份白色固体分别为碳酸钠、碳酸氢钠及二者的混合物。某化学课外活动小组对其进行相关实验和探究。
I.甲组同学采用加热的方法确定其成分。
(1)除托盘天平、药匙、三脚架、泥三角、玻璃棒和干燥器外,完成本实验还需要的实验仪器有_________。
(2)该小组同学准确称取一定量的样品m1g,多次加热、冷却、称量直至恒重,质量为m2g。依据得出结论,请完成下表。
m2与m1的关系
结论
①
样品为Na2CO3
②
样品为NaHCO3
③
样品为Na2CO3和 NaHCO3的混合物
II.乙组同学利用已鉴别出的NaHCO3和Na2CO3,继续进行实验,对于“能否用CaCl2鉴别的NaHCO3和Na2CO3”的问题进行探究。
(3)小组同学先将NaHCO3、Na2CO3、CaCl2固体分别配制成0.5mol/L的溶液。设汁如下实验方案:
表1
实验方案
预测现象
实验1
向2mL Na2CO3溶液中滴加1mL CaCl2溶液
有白色沉淀生成
实验2
向2mL NaHCO3溶液中滴加1mL CaCl2溶液
无白色沉淀生成
若已知:①室温下,0.5mol/L NaHCO3溶液pH=8.5,溶液中c(HCO3-)=0.49 mol/L 。
②室温下, H2CO3的二级电离常数K2=5.6×10-11。
③Ksp(CaCO3)=2.8×10-9。
试估算使0.5mol/L NaHCO3溶液中的CO32-沉淀所需的c(Ca2+)应不低于_____mol/L,并由此得出结论:实验2的预测现象_____(填“正确”或“不正确”)。
⑷实际实验过程发现实验2的现象为白色沉淀并有无色气体生成。此现象对应的离子方程式为_____________。
(5)该小组同学继续设计实验对NaHCO3溶液与CaCl2溶液的反应进行探究,利用气体压力传感器得到的部分实验数据如下:(注:CaCl2溶液浓度相同)
表2 容器内气体浓度达到10000ppm所需时间
C(NaHCO3)/(mol/L)
所需时间/s
v(CaCl2):v(NaHCO3)
1:5
2:5
4:5
1:1
1.0
142
124
114
156
0.5
368
264
244
284
0.25
882
450
354
632
0.1
1126
1316
816
1816
由实验数据可得出的结论是:
①当v(CaCl2):v(NaHCO3)一定时,随着_____,气体逸出速率减小;
②NaHCO3浓度在0.1~1.0mol/L,v(CaCl2)与v(NaHCO3)的比值为____时,气体逸出速率最快,可获得理想的实验观察效果。
高三化学实验题中等难度题查看答案及解析
-
(12分)某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验.
方案Ⅰ.甲组同学用质量法,按如下图所示的实验流程进行实验:

(1)实验时,蒸发结晶操作中,除了酒精灯外,还要用到的仪器是
(2)有同学认为“加入适量盐酸”不好操控,应改为“过量盐酸”,便于操作且不影响测定的准确性,你认为对或错 ,为什么
(3)若实验中测得样品质量为46.4g,固体质量为40.95g,则碳酸钠的质量分数为 .(保留3位有效数字)
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数 (填偏大 偏小 无影响).
方案Ⅱ:乙组同学的主要实验流程图如下:

按如下图所示装置进行实验:

(5)在C中装碱石灰来吸收净化后的气体.D装置的作用是 .
(6)有的同学认为为了减少实验误差,在反应前后都通入N2,反应后通入N2的目的是 .
方案Ⅲ:气体分析法
(7)把一定量样品与足量稀硫酸反应后,用如图装置测量产生CO2气体的体积,B溶液最好采用 (以下选项中选择)使测量误差较小.

A.饱和碳酸钠溶液 B.饱和碳酸氢钠溶液
C.饱和氢氧化钠溶液 D.饱和硫酸铜溶液
高三化学实验题极难题查看答案及解析
-
某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如图所示的实验流程进行实验:
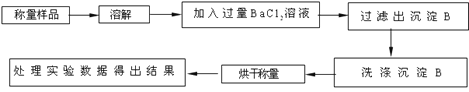
实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为 ______ ;
检验沉淀B已洗净操作是 ______ ;
若实验中测得样品质量为mg,沉淀质量为ng,则碳酸钠的质量分数为 ______ 。
方案Ⅱ.乙组同学的主要实验
如图

按如图所示装置进行实验:
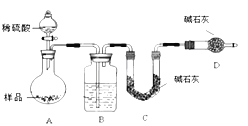
该实验中装置B盛放的物质是 ______ ,分液漏斗中 ______
填“能”或“不能”
用盐酸代替稀硫酸进行实验;
在C中装碱石灰来吸收净化后的气体。
样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差 ______(填“越大”、“越小”或“不变化”);
装置的作用是 ______ 。
有的同学认为为了减少实验误差,在反应前后都要通入
如图
,反应后通入
的目的是 ______ 。
高三化学实验题中等难度题查看答案及解析
-
(15分)某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验.
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:
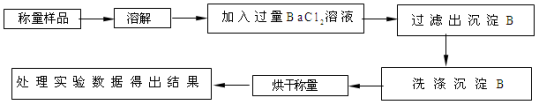
(1)实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为 .
(2)检验沉淀B已洗净操作是 .
(3)在整个实验过程中托盘天平至少使用 次.
(4)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为____________.
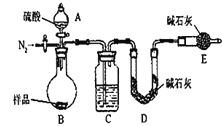
方案Ⅱ.乙组同学的主要实验按如下图所示装置进行实验:

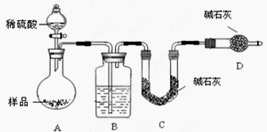
(5)该实验中装置B盛放的物质是__________,分液漏斗中 (填“能”或“不能” )用盐酸代替稀硫酸进行实验.
(6)在C中装碱石灰来吸收净化后的气体.
①样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差____________________(填“越大”、“越小”或“不变化”)
②D装置的作用是_________________.
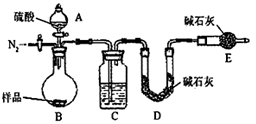
(7)有的同学认为为了减少实验误差,在反应前后都要通入N2(如图),反应后通入N2的目的是_____________________.
高三化学实验题极难题查看答案及解析
-
某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:
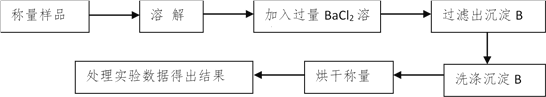
(1)实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为____________。
(2)洗涤沉淀B的操作是__________________________________________________。
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为________。

方案Ⅱ.乙组同学的主要实验流程图如下:
按如下图所示装置进行实验:
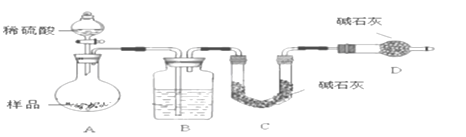
(4)该实验中装置B盛放的物质是_____________________,分液漏斗中___________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(5)在C中装碱石灰来吸收净化后的气体。D装置的作用是_________________。
(6)有的同学认为为了减少实验误差,在反应前后都要通人N2(如下图),
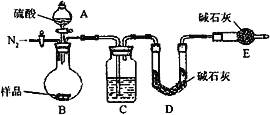
反应后通入N2的目的是_____________________。
高三化学实验题中等难度题查看答案及解析
-
(18分)某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:
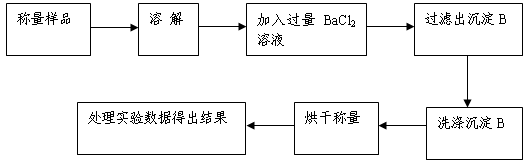
(1)实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为________。
(2)洗涤沉淀B的操作是_______________________________________________
_________________________________________________________________。
(3)在整个实验过程中托盘天平至少使用_____________次。
(4)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为_____________________。
方案Ⅱ.乙组同学的主要实验流程图如下:
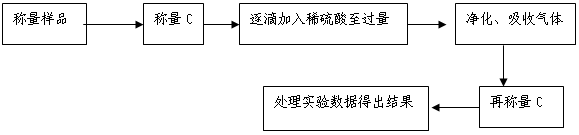
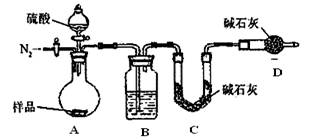
按如下图所示装置进行实验:
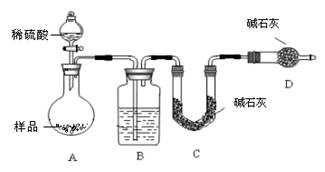
(5)该实验中装置B盛放的物质是_____________________,分液漏斗中________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(6)在C中装碱石灰来吸收净化后的气体。
①样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差____ __。(填“越大”、“越小”或“不变化”)
②D装置的作用是______________ _ _________。
(7)有的同学认为为了减少实验误差,在反应前后都要通人N2(如图),反应后通入N2的目的是________。
高三化学实验题简单题查看答案及解析
-
某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同
学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:[已知Ba(HCO3)2可溶于水]

(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为________。
(2)洗涤沉淀B的操作是。
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为____________。
方案Ⅱ.乙组同学的主要实验流程图如下:

按如下图所示装置进行实验:
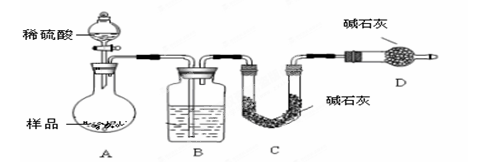
(4)该实验中装置B盛放的物质是_____________________,分液漏斗中________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(5)在C中装碱石灰来吸收净化后的气体。
①样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差
____________________。(填“越大”、“越小”或“不变化”)
②D装置的作用是_________________________。
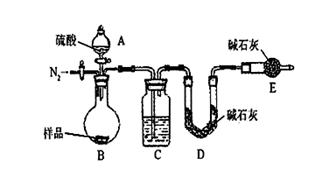
(6)有的同学认为为了减少实验误差,在反应前后都要通入N2(如右图),反应后通入N2的目的是____
__________________________________________________________________________________。
高三化学实验题困难题查看答案及解析
-
(16分)某小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:[已知Ba(HCO3)2可溶于水]
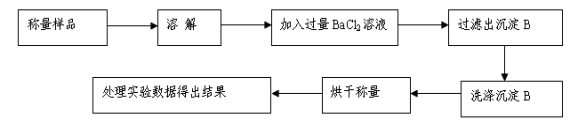
(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为 。
(2)洗涤沉淀B的操作是 。
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为____________。
方案Ⅱ.乙组同学的主要实验流程图如下:

按如下左图所示装置进行实验:
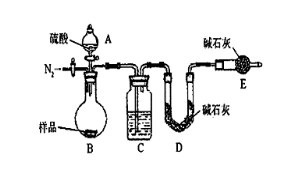
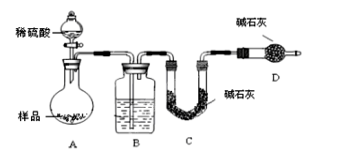
(4)该实验中装置B盛放的物质是_____________________,分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(5)在C中装碱石灰来吸收净化后的气体。
①样品中碳酸钠的质量分数越大,则实验中干燥管C在充分吸收气体前后的质量差____________________。(填“越大”、“越小”或“不变化”)
②D装置的作用是_________________________。
(6)有同学认为为了减少实验误差,在反应前后都要通入N2(如上右图),反应后通入
N2的目的是______________________________。
高三化学实验题困难题查看答案及解析
-
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验.如图I~Ⅳ所示.

(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的是(填装置序号)______;
(2)①图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为______ Na2CO3+H2O+CO2↑;高三化学解答题中等难度题查看答案及解析
-
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如下图所示。

(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号) 。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为________________________________________________________________________;
与实验Ⅲ相比,实验Ⅳ的优点是(填选项序号)________;
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是(填化学式)________。
高三化学实验题简单题查看答案及解析