-
某温度下,将1.1mol I2加入到氢氧化钾溶液中,反应后得到 KI、KIO、KIO3的混合液。经测定IO-与IO3-的物质的量之比是2:3.下列说法错误的是
A. I2在该反应中既作氧化剂又做还原剂
B. I2的还原性大于KI的还原性,小于KIO和KIO3的还原性
C. 该反应中转移电子的物质的量为1.7mol
D. 该反应中,被还原的碘元素与被氧化的碘元素的物质的量之比是17:5
高二化学单选题中等难度题查看答案及解析
-
已知溶液中:氧化性IO3—>I2>SO32-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示,下列说法正确的是( )

A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素
B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
C.c点到d点的反应中共转移0.6mol电子
D.往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:5HSO3-+ 2IO3- =I2+5SO42-+3H++H2O
高二化学选择题简单题查看答案及解析
-
已知:还原性HSO3->I-,氧化性IO3->I2。在含3mol NaHSO3的溶液中逐滴加人KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是

A. 0-a段发生反应:3HSO3-+IO3-=3SO42-+I-+3H+
B. a~b段共消耗NaHSO3的物质的量为1.8mol
C. b~c段反应:氧化产物为I2
D. 当溶液中I-与I2的物质的量之比为5 : 1时,加入的KIO3为1.lmol
高二化学单选题困难题查看答案及解析
-
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法不正确的是
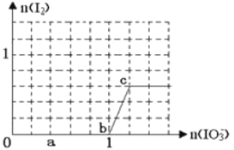
A. 0--b :3HSO3-+ IO3-= 3SO42-+ I-+ 3H+
B. a点时消耗NaHSO3的物质的量为1.2 mol
C. b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2
D. 当溶液中I¯与I2的物质的量之比为5∶2时,加入的KIO3为1.8mol
高二化学单选题困难题查看答案及解析
-
下列表示对应化学反应离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH-
B.FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+
C.用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O
D.过量氯气通入FeI2溶液中:3Cl2+2I- +4Fe2+=I2+4Fe3++4Cl-
高二化学选择题中等难度题查看答案及解析
-
在KIO3、KHSO3的酸性混合溶液中加入少量KI和淀粉,不停地搅拌,有下列反应发生:①IO3-+5I-+6H+===3I2+3H2O;②I2+HSO3-+H2O===2I-+SO42-+3H+。当反应进行到15 min时,溶液颜色迅速变蓝,随之又很快消失,这一反应称为时钟反应,有人用它来解释生物钟现象,下列说法中错误的是
A. 在整个反应过程中,起催化作用的物质是KI
B. 时钟反应的快慢由反应②决定
C. 上述两个反应中,反应速率较快的是②
D. “溶液颜色迅速变蓝,随之又很快消失”这一现象与①②的反应速率有关
高二化学单选题简单题查看答案及解析
-
加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH===5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。下列说法中正确的是( )
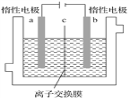
A. 电解过程中OH-从a极区通过离子交换膜c进入b极区
B. 随着电解进行,KOH溶液浓度会逐渐减小
C. a电极反应式:I--6e-+6OH-=== IO3-+3H2O,a极区的KI最终转变为KIO3
D. 当阳极有0.1 mol I-放电时,阴极生成6.72 L H2
高二化学单选题困难题查看答案及解析
-
KIO3是一种重要的无机化合物,可作为食盐中的补碘剂,常见制备方法如下。
(1)氯酸钾氧化法:化学反应方程式为:6I2+11KClO3+3H2O=6KH(IO3)2+5KC1+3C12,每生成3mol KH(IO3)2,反应中转移的电子数为______,向反应后溶液中加______溶液得到KIO3。
(2)一种由含碘废水制取碘酸钾的工艺如图:
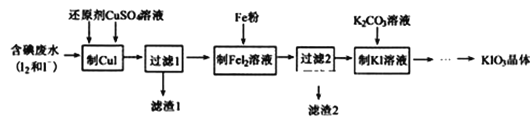
①进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤液中可通过滴加______盐溶液来检验其是否已洗涤干净。
②“制FeI2”时,发生反应的化学方程式为______。
③在KIO3、KHSO3的酸性混合溶液中加入少量KI(催化剂)和淀粉,不停地搅拌,反应机理为:第一步IO3-+5I-+6H+=3I2+3H2O 第二步反应的离子方程式为______。
当反应进行到1.5min时,溶液突然变为蓝色,随之又很快消失,则第______步反应速率快。
④改变反应温度,重复上述实验,得到温度(T)与溶液变蓝所需时间(t)的关系如图所示(超过50℃后溶液不会再变蓝)。根据图象,请你分析温度低于50℃时,溶液变蓝所需时间与反应温度的关系:_________。
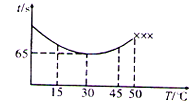
(3)山东省已下调食用盐碘含量标准每千克盐含碘25毫克(波动范围为18~33mg•kg-1)。测定食盐试样中碘元素含量的步骤如下:称取4.000g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00mL 6.000×10-4mol•L-1Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-。计算该食盐试样中碘元素的含量______mg•kg-1。
高二化学综合题中等难度题查看答案及解析
-
(1)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:
2IO3﹣+5SO32﹣+2H+═I2+5SO42﹣+H2O,生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率,某同学设计实验如表所示:
0.01mol•L﹣1
KIO3酸性溶液(含淀粉)的体积/mL
0.01mol•L﹣1
Na2SO3溶液的体积/mL
H2O的体积
/mL
实验
温度
/℃
溶液出现蓝色时所需时间/s
实验1
5
V1
35
25
实验2
5
5
40
25
实验3
5
5
V2
0
该实验的目的是 ,表中V1= mL.
(2)可逆反应C(s)+H2O(g)
H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图.

①图中t2到t3段、t4到t6段时引起平衡移动的条件分别可能是 、 ;
②图中表示平衡混合物中CO的含量最高的一段时间是 .
高二化学填空题极难题查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I 2+6OH-
B.向NH4HCO3溶液中加少量NaOH溶液并加热:NH4++OH-
NH3↑+H2O
C.将少量二氧化硫气体通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+
D.用稀硝酸洗涤试管内壁的银镜:3Ag+4H++NO3-=3Ag++NO↑+2H2O
高二化学选择题简单题查看答案及解析