-
【化学——选修2:化学与技术】(15分)
Ⅰ.合成氨工业的主要反应为:N2(g) + 3H2(g) 2NH3(g) △H<O,下图是合成氨的简要流程示意图:
2NH3(g) △H<O,下图是合成氨的简要流程示意图:
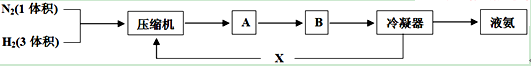
(1)沿X路线进入压缩机的物质是 。
(2)氮、氢混合气体送入合成塔前要通过压缩机压缩的原因是 ;
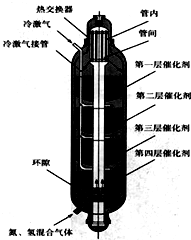
(3)下图为氨合成塔,为什么原料气从塔底流经外筒环隙进入,气体在反应前后都要通过热交换器?
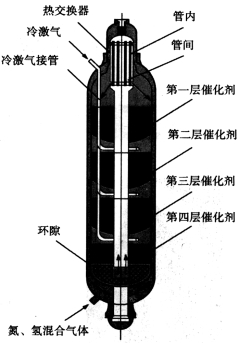
Ⅱ.氨是一种重要的化工原料,能制备氮肥、硝酸和纯碱等。
(1)我国化学家侯德榜改革国外的纯碱生产工艺,采用联合制碱法,生产流程可简要表示如下:
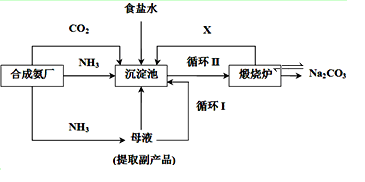
①写出上述流程中X物质的分子式 。
②沉淀池中发生的化学反应方程式是 。
③向母液中通入氨气,加入细小食盐颗粒,冷却析出副产品,通入氨气的作用有 。
a.增大NH4+的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(2)某工厂用氨制硝酸,再进一步制NH4NO3。已知由NH3制HNO3时产率为88%,由NH3被HNO3的吸收率为98%。则该工厂用100吨氨最多能制硝酸铵 吨。
-
[化学——选修化学与技术](15分)
工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g) 2NH3(g),其
2NH3(g),其
部分工业流程如下:
回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g) △H=180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905kJ/mol
2H2(g)+O2(g)=2H2(g) △H=-483.6kJ/mol
则N2(g)+2H2 2NH3(g)的△H=________;
2NH3(g)的△H=________;
(2)如果工业上,在一定温度下,将1.5molN2气体和6molH2气体通入到体积为1升的密闭容器中。当反应达到平衡时,容器内气体的压强为起始时的80%,则其平衡常数为________。改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是________;
①增大压强 ②增大反应物质的浓度
③使用催化剂 ④降低温度
(3)合成氨反应的平衡常数很小,所以在工业采取气体循环的流程。即反应后通过降低混合气体的温度而使氢气分离出来。这种分离物质的方法其原理类似于下列哪种方
法?________(填编号)
①过滤 ②蒸馏 ③渗析 ④萃取
理由是________;
(4)可以用氯气来检验输送氨气的管道是否漏气,如果漏气则会有白烟(成份为氯化铵)生成。该反应的化学方程式为________;
(5)假如该厂生产氨水的物质的量浓度为20mol/L,实验室若需用80mL浓度为5mol/L的氨水时,需取20mol/L的氨水________mL(用100mL的容量瓶)。假如该氨水的pH=a,加入相同体积的盐酸时,溶液呈中性,则此盐酸的pH________14-a(填“大于”“小于”或“等于”)。
-
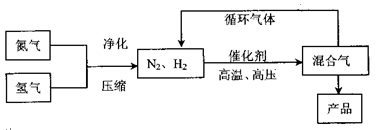
【选修-化学与技术】合成氨工业的主要反应为:N2(g)+3H2(g)⇌2NH3(g)△H<O,下图是合成氨的简要流程示意图:
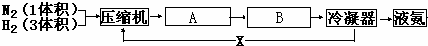 (1)写出设备A、B的名称:A______,B______;沿X路线进入压缩机的物质是______.
(1)写出设备A、B的名称:A______,B______;沿X路线进入压缩机的物质是______.
(2)原料气往往混有CO、NH3等杂质,在进入合成塔之前需净化,净化的原因是______.
(3)氮、氢混合气体送入合成塔前要通过压缩机压缩的原因是______;在合成塔中及时分离出氨气的目的是______.
(4)工业合成氨的反应为:N2(g)+3H2(g)⇌2NH3(g)△H<O,当压强为30MPa,温度为500℃时,在容积为1L的密闭容器中充入1molN2和3molH2,反应达到平衡时NH3的体积分数为20%,求此时的平衡常数______.
(5)合成塔从上到下将催化剂分成四层,在层与层之间冷激气(冷的原料气)和反应气混合,请问这样设计的原因是什么?______.
-
【化学——选修2:化学与技术】(15分)氮的化合物是重要的化工原料,在工农业生产中有很多重要应用。工业上合成氨的流程示意图如下:
回答下列问题:
(1)25℃时合成氨反应热化学方程式为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol。在该温度时,取1 mol N2和3 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4 kJ。其原因是______________。
2NH3(g) ΔH=-92.4 kJ/mol。在该温度时,取1 mol N2和3 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4 kJ。其原因是______________。
(2)原料氢气的来源是水和碳氢化合物,写出工业生产中分别采用煤和天然气为原料制取氢气的化学反应方程式: , 。
(3)设备B的名称是________,其中m和n是两个通水口,入水口是 (填“m”或“n”),不宜从相反方向通水的原因 。
(4)设备C的作用是 。
(5)为了提高其产量,降低能耗,近年有人将电磁场直接加在氮气与氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了较好的产率。从化学反应本质角度分析,电磁场对合成氨反应的作用是 ;与传统的合成氨的方法比较,该方法的优点是 。
-
(8分)【化学-化学与技术】
工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g) 2NH3(g);△H=-92.44 kJ/mol;其部分工艺流程如下:
2NH3(g);△H=-92.44 kJ/mol;其部分工艺流程如下:
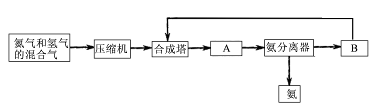
(1)合成氨所需要的原料气中,氮气取自________,氢气来源于________。
(2)对原料气进行净化处理的目的是________。
(3)设备A的名称是________ ,设备B的名称是________ 。
(4)在10~30Mpa时,工业合成氨选择400~500 ℃的温度进行反应,主要原因是________。
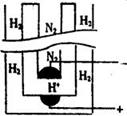
(5)据《科学》杂志报道,希腊化学家在常压下将氢气和用氢气稀释的氮气分另通入一个加热到570 ℃的电解池(如图)中,氢和氮在电极上合成了氨,且转化率达到了78%。
则阳极反应为________,阴极反应为________。
-
选考[化学—选修2:化学与技术](15分)工业合成氨技术是对人类的巨大贡献之一。下面是合成氨的简要流程示意图:
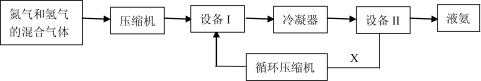
(1)设备I的名称是 ,沿X路线循环的物质是 (填字母)。
A.N2和H2 B.催化剂 C.NH3 D.N2、H2和NH3
(2)合成氨中H2可以由焦炭和水蒸汽反应获得。请写出该反应的化学方程式:_______。
(3)原料气中往往含有H2S、CO、CO2等杂质,必须除去这些杂质的目的是 ,常用K2CO3溶液除去CO2,其反应的离子方程式为 。
(4)近年有人将电磁场直接加在氮气和氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了较高的产率。电磁场对合成氨反应本质的影响是_______,该方法的优点是_________________。
(5)合成氨工业往往含有大量含氨废水,为了防止对环境造成污染,可以利用电解法将NH3·H2O转化为对环境无污染的加以处理。电解时以石墨做电极,以硝酸作为电解质,则理论上处理1mol NH3·H2O,电路中转移电子 mol,阳极的电极反应式为 。
-
(12分)【化学——化学与技术】
合成氨工业对国民经济和社会发展具有重要意义,下图是工业合成氨的简要流程示意图。
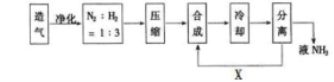
(1)合成氨的原料气往往混有CO2等杂质,在进入合成塔之前需净化,其原因是_______ 。
(2)工业上合成氨选择的适宜条件是:以铁为主的催化剂、_______、________。
(3)沿X路线进入合成塔的物质是_______,这样设计的意义是________。
(4)目前工业制硝酸所采用的主要方法是_______法。
-
合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g) 2NH3(g) ∆H= —92.4kJ•mol‾1 一种工业合成氨的简易流程图如下:
2NH3(g) ∆H= —92.4kJ•mol‾1 一种工业合成氨的简易流程图如下:

(1)天然气中的H2S杂质常用氨水吸收,写出氨水的电离方程式 。吸收产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出吸收液再生反应的化学方程式 。
(2)步骤II中制氢气原理如下:
①CH4(g)+H2O(g)  CO(g)+3H2(g) △H=+206.4 kJ·mol-1
CO(g)+3H2(g) △H=+206.4 kJ·mol-1
②CO(g)+ H2O(g)  CO2(g)+H2(g) △H=-41.2 kJ·mol-1
CO2(g)+H2(g) △H=-41.2 kJ·mol-1
则反应CH4(g)+2H2O(g)  CO2(g)+4H2(g) △H= kJ·mol-1。
CO2(g)+4H2(g) △H= kJ·mol-1。
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是(填编号) 。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
(3)利用反应②,将CO进一步转化,可提高H2产量。若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O蒸气反应,得到1.18mol CO、CO2和H2的混合气体,则CO转化率为 。
(4)下图1表示500℃、60.0MPa条件下,H2和N2为原料气的投料比与平衡时NH3体积分数的关系。根 据图中a点数据计算N2的平衡体积分数为 。
(5)依据温度对合成氨反应的影响,在下图2坐标系中,画出一定条件下的密闭容器内,从通入起始原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。
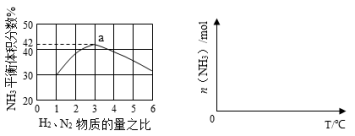
图1 图2
(6)简述本流程中提高合成氨原料总转化率的方法 。
-
(14分)合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g) 2NH3(g) ∆H=—92.4kJ•mol‾1
2NH3(g) ∆H=—92.4kJ•mol‾1
一种工业合成氨的简易流程图如下:

(1)天然气中的H2S杂质常用常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式: 。
(2)步骤II中制氯气原理如下:

对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是 。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18mol CO、CO2和H2的混合气体,则CO转化率为 。
(3)下左图表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数: 。
(4)依据温度对合成氨反应的影响,在下右图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。
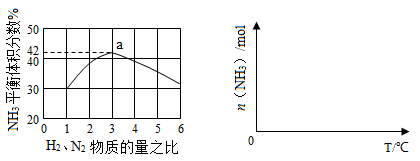
(5)上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是(填序号) ,简述本流程中提高合成氨原料总转化率的方法: 。
-
合成氨是人类科学技术上的一项重大突破,其反应原理为:N2(g)+3H2(g)⇌2NH3(g) △H=-92.4kJ⋅mol-1
一种工业合成氨的简易流程图如图:

(1)天然气中的H2S杂质常用常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:___。
(2)步骤II中制氯气原理如下:
①CH4(g)+H2O(g)=CO2(g)+3H2(g) △H=+206.4kJ⋅mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41.2kJ⋅mol-1
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是___。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若1molCO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO转化率为___。
(3)图2表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:___。
(4)依据温度对合成氨反应的影响,在图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图___。
(5)上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是___(填序号),简述本流程中提高合成氨原料总转化率的方法:___。
 (1)写出设备A、B的名称:A______,B______;沿X路线进入压缩机的物质是______.
(1)写出设备A、B的名称:A______,B______;沿X路线进入压缩机的物质是______.