-
(8分)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
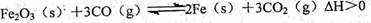
①该反应的平衡常数表达式为:K=________。
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为________。
(2)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。
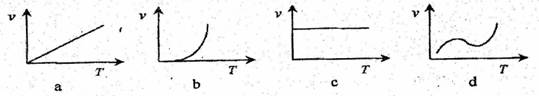
(3)Fe3+盐和Al3+盐在性质上有很多相似的地方,如遇碱都生成难溶的胶状沉淀,可用于净水;也有不同之处,如Fe3+既有氧化性又有还原性,Al3+只有氧化性。但Fe3+只有在碱性介质中才能被氧化为FeO2-4,请完成下列方程式:
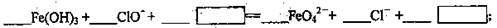
(4)若将ag Fe和Al的混合物溶于2mol/L的足量的硫酸中,将往溶液中加入足量的6mol/L的NaOH溶液,充分反应,过滤.洗涤,干燥灼烧,称量所得固体的质量仍为ag,则原混合物中A1的质量分数为________。
-
(12分)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) △H>0。
2Fe(s)+3CO2(g) △H>0。
①该反应的平衡常数表达式为K=________________;
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为_____________________;
(2)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是__________;
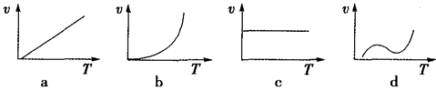
(3)三价铁盐和铝盐在性质上有很多相似的地方,如遇碱都生成难溶的胶状沉淀,可用于净水;也有不同之处,如Fe3+既有氧化性又有还原性,Al3+只有氧化性.但Fe3+只有在碱性介质中才能被氧化为FeO42-,请完成下列化学方程式:
_____Fe(OH)3+___ClO-+____ =____FeO42-+___Cl-+____
=____FeO42-+___Cl-+____ ;
;
(4)若将ag Fe和Al的混合物溶于2mol/L足量的硫酸中,再往溶液中加入足量的6mol/L的NaOH溶液,充分反应,过滤、洗涤、干燥灼烧,称量所得固体的质量仍为ag,则原混合物中Al的质量分数为_____________。
-
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质.
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g)⇌2Fe(s)+3CO2(g)
①该反应的平衡常数表达式为:K=______.
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g.则10min内CO的平均反应速率为______.
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
①______②______.
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应.下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是______.
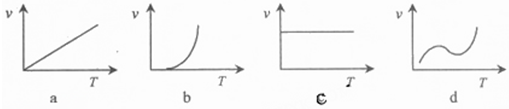
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:______,欲使上述体系中Al3+浓度增加,可加入的物质是______.
-
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质.
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g)⇌2Fe(s)+3CO2(g)
①该反应的平衡常数表达式为:K=______.
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g.则10min内CO的平均反应速率为______.
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
①______②______.
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应.下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是______.
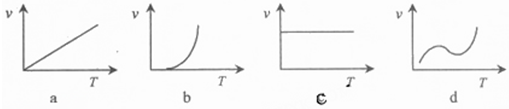
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:______,欲使上述体系中Al3+浓度增加,可加入的物质是______.
-
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
①该反应的平衡常数表达式为:K=________。
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为________。
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
①________②________。
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
和温度(T)的关系示意图中与铝热反应最接近的是________。
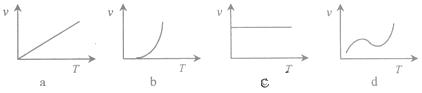
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:________,欲使上述体系中Al3+浓度增加,可加入的物质是________。
-
(10分)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)ΔH>0
2Fe(s)+3CO2(g)ΔH>0
①该反应的平衡常数表达式为:K=________
②该温度下,在2L盛有 粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为________
粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为________
(2)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。
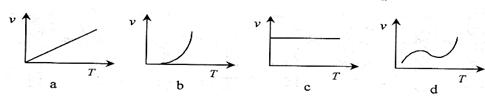
(3)Fe3+盐和Al3+盐在性质上有很多相似的地方,如遇碱都生成难溶的胶状沉淀,可用于净水;也有不同之处,如Fe3+既有氧化性又有还原性,Al3+只有氧化性。但Fe3+只有在碱性介质中才能被氧化为FeO42-,请完成下列方程式:
________Fe(OH)3 +________ClO- + ________ ==________FeO42- + ________Cl- +________ ;
(4)若将ag Fe和Al的混合物溶于2mol/L的足量的硫酸中,再往溶液中加入足量的6mol/L的NaOH溶液,充分反应,过滤,洗涤,干燥灼烧,称量所得固体的质量仍为ag,则原混合物中Al的质量分数为
________
-
铁和铝是两种重要的金属,它们的单质及化合物存在着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(g)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
①该反应的平衡常数表达式为:K=___;
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为___;
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态。
①___;②___。
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是___。
a.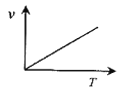 b.
b.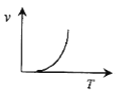
c.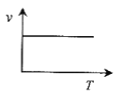 d.
d.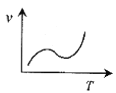
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:___;欲使上述体系中Al3+浓度增加,可加入的物质是___。
-
铁是一种重要的金属,它的单质及化合物有着各自的性质.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)⇌FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图所示:
(1)如果该反应的平衡常数K值变大,该反应______ (选填编号).
a.一定向逆反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向正反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(2)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,(选填编号)______.
a.容器中气体的平均分子量不随时间而变化 b. v(CO)=v(CO2)
c.容器中气体的密度不随时间而变化 d.通入稀有气体能提高反应的速率
(3)请用上述反应中某种气体的有关物理量来说明该反应处于不平衡状态:
①______②______
(4)若反应的容器容积不变且为2.0L,反应时间5.0min,容器内气体的密度减小了0.80g/L,在这段时间内CO2的平均反应速率为______.

-
典型金属元素及化合物的特征性质有着重要的应用,请按要求回答:
(1)Na、Al、Fe、Cu四种元素的单质中:
①Al与NaOH溶液反应的离子方程式是____________,其中作氧化剂的是_______。
②Cu在潮湿的空气中被腐蚀的化学方程式是_______________。
(2)上述四种金属的氧化物中:
①写出能用作供氧剂的一个化学方程式:___________________。
②既能溶于酸溶液又溶于强碱溶液,写出溶于强碱溶液的离子方程式_______________。
③常温下为黑色固体的是_________________。
(3)上述四种金属的氢氧化物中:
①易在空气中被氧化的现象是_______________。
②具有两性的是_________________。
(4)上述四种金属形成的阳离子共__________有种,其中既能表现还原性,又能表现氧化性的是__________;其中氧化性最强的是__________。
-
运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1) 用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的 活性炭和NO,发生 反应C(s)+2NO(g)  N2(g)+CO2(g)△H=QkJ/mol。 在T1℃时,反应进行到不同时间(min) 测得各物质的浓度(mol/L) 如下:
N2(g)+CO2(g)△H=QkJ/mol。 在T1℃时,反应进行到不同时间(min) 测得各物质的浓度(mol/L) 如下:
| 浓度 时间 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①30min 后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________(填字母编号)
a.通入一定量的NO b.加入定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
② 若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3: 1: 1,则Q_____ 0 (填“>”或“<”<)。
(2) 某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,则得NO转化为N2的转化率随温度、CO混存量的变化情况如下图所示,利用以下反应:NO+CO N2+CO2( 有CO) 2NO
N2+CO2( 有CO) 2NO N2+ O2 (无CO)
N2+ O2 (无CO)
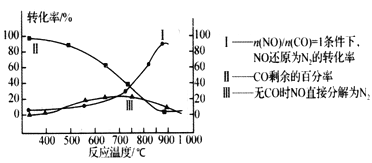
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为: __________;在n(NO)/n(CO)= 1的条件下,应控制最佳温度在_______左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染,写出C2H6与NO2发生反应的化学方程式_________________。
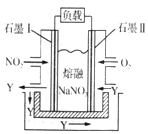
③以NO2、O2 熔融NaNO3组成的燃料电池装置如下图所示,在使用过程中石墨I电极反应生成一种氧化物Y,则该电极反应式为__________________。
(3) 天然气的一个重要用途是制取氢气,其原理如下:
已知:① 2CO(g)+O2(g)=2CO2(g) △H1
②CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) △H2
③2H2(g)+O2(g)=2H2O(l) △H3
1)科学家提出一种利用天然气制备氢气的方法: CH4(g)+ CO2(g)=2CO(g)+2H2(g) △H=_____
2)这种方法的推广与使用,不仅实现资源综合利用,而且还能解决环境问题是_________。

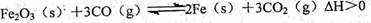

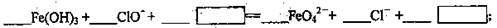
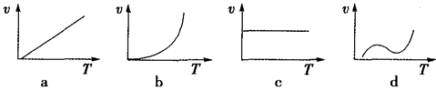



 b.
b.
 d.
d.

