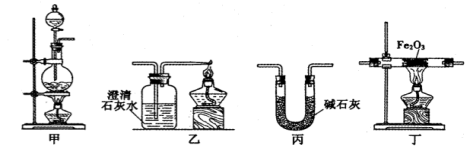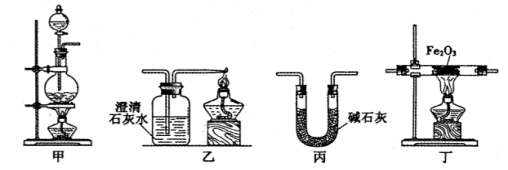-
甲酸(HCOOH)是一种有刺激性气味的无色液体,有很强的腐蚀性。熔点8.4℃,沸点100.7℃,能与水、乙醇互溶,加热至160℃即分解成二氧化碳和氢气。
(1)实验室可用甲酸与浓硫酸共热制备一氧化碳:HCOOH H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃~90℃,再逐滴滴入甲酸。
H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃~90℃,再逐滴滴入甲酸。

①从下图挑选所需的仪器,在虚线框中画出Ⅰ中所缺的气体发生装置(添加必要的塞子、玻璃管、胶皮管,固定装置不用画),并标明容器中的试剂。
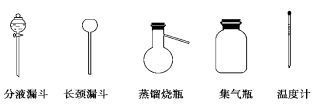
②装置Ⅱ的作用是_____________________________________________。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸制得四水甲酸铜[Cu(HCOO)2·4H2O]晶体。相关的化学方程式是:
2CuSO4+4NaHCO3===Cu(OH)2·CuCO3↓+3CO2↑+2Na2S O4+H2O
O4+H2O
Cu(OH)2·CuCO3+4HCOOH+5H2O===2Cu(HCOO)2·4H2O+CO2↑
实验步骤如下:
I.碱式碳酸铜的制备:

①步骤ⅰ是将一定量CuSO4·5H2O晶体和 NaHCO3固体一起放到研钵中研磨,其目的是___________。
NaHCO3固体一起放到研钵中研磨,其目的是___________。
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃~80℃,如果看到______(填写实验现象),说明温度过高。
II.甲酸铜的制备:
将Cu(OH)2·CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的1/3时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2—3次,晾干,得到产品。
a、“趁热过滤”中,必须“趁热”的原因是 。
b、用乙醇洗涤晶体的目的是 。
-
(13分)甲酸(HCOOH)是一种有刺激臭味的无色液体,有很强的腐蚀性。熔点8.4℃,沸点100.7℃,能与水、乙醇互溶,加热至160℃即分解成二氧化碳和氢气。
(1)实验室可用甲酸与浓硫酸共热制备一氧化碳:HCOOH H2O+CO↑,
H2O+CO↑,
实验的部分装置如下图所示。制备时先加热浓硫酸至80℃—90℃,再逐滴滴入甲酸。
①从下图挑选所需的仪器,画出Ⅰ中所缺的气体发生装置(添加必要的塞子、玻璃管、胶皮管,固定装置不用画),并标明容器中的试剂。





分液漏斗 长颈漏斗 蒸馏烧瓶 集气瓶 温度计
②装置Ⅱ的作用是________。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸斥制得四水甲酸铜[Cu(HCOO)2·4H2O]晶体。相关的化学方程式是:
2CuSO4+4 NaHCO3== Cu(OH)2·CuCO3↓+3CO2↑+2Na2SO4+H2O
Cu(OH)2·CuCO3+4HCOOH+ 5H2O==2 Cu(HCOO)2·4H2O+ CO2↑
实验步骤如下:
Ⅰ、碱式碳酸铜的制备:

③步骤ⅰ是将一定量CuSO4·5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是________。
④步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃—80℃,如果看到________(填写实验现象),说明温度过高。
Ⅱ、甲酸铜的制备:
将Cu(OH)2·CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的1/3时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2—3次,晾干,得到产品。
⑤“趁热过滤”中,必须“趁热”的原因是________。
⑥用乙醇洗涤晶体的目的是________。
-
某化学实验小组欲测定铁的氧化物 样品组成,查阅资料发现:甲酸
样品组成,查阅资料发现:甲酸 是一种有刺激性气味的无色液体,易挥发,有较强的还原性,熔点
是一种有刺激性气味的无色液体,易挥发,有较强的还原性,熔点 ,沸点
,沸点 ,能与水、乙醇互溶,甲酸与浓硫酸共热可制备一氧化碳:HCOOH
,能与水、乙醇互溶,甲酸与浓硫酸共热可制备一氧化碳:HCOOH H2O+CO↑,制备时先加热浓硫酸至
H2O+CO↑,制备时先加热浓硫酸至 ,再逐滴滴入甲酸。根据以上信息设计了实验装置,如图所示:
,再逐滴滴入甲酸。根据以上信息设计了实验装置,如图所示:
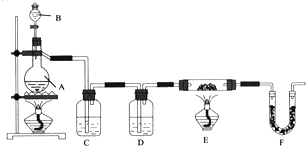
请回答下列问题:
 仪器中装入的试剂:B ______ 、C ______ 、D ______。
仪器中装入的试剂:B ______ 、C ______ 、D ______。
 该实验装置A仪器中须添加一种玻璃仪器,其名称为______;连接好装置后应首先______。
该实验装置A仪器中须添加一种玻璃仪器,其名称为______;连接好装置后应首先______。
 “加热反应管E”和“从B向A逐滴滴加液体”这两步操作应该先进行的是______
“加热反应管E”和“从B向A逐滴滴加液体”这两步操作应该先进行的是______ 在这两步之间还应进行的操作是______。
在这两步之间还应进行的操作是______。
 反应过程中F管
反应过程中F管 内盛碱石灰
内盛碱石灰 逸出的气体是______,其处理方法是______。
逸出的气体是______,其处理方法是______。
 测得下列数据
测得下列数据 空E管的质量为
空E管的质量为 ;
; 管和
管和 样品的总质量为
样品的总质量为 ;
; 反应后冷却至室温称量E管和铁粉的总质量为
反应后冷却至室温称量E管和铁粉的总质量为 经确认样品全部变为铁粉
经确认样品全部变为铁粉 计算可知该铁的氧化物化学式为______。
计算可知该铁的氧化物化学式为______。
 设计实验证明:
设计实验证明:
 甲酸的酸性比碳酸的强______。
甲酸的酸性比碳酸的强______。
 的氧化性比
的氧化性比 的弱______。
的弱______。
-
无色而有刺激性气味的甲酸,是最简单的羧酸液体,熔点8.6℃,沸点100.8℃。化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其反应方程式为:HCOOH CO↑+H2O,制备时先加热浓硫酸至80℃-90℃,控制温度,再逐滴滴入甲酸。
CO↑+H2O,制备时先加热浓硫酸至80℃-90℃,控制温度,再逐滴滴入甲酸。

(1)请从图中选用所需的仪器(仪器可重复使用)组成一套验证甲酸(HCOOH)和浓硫酸加热生成产物的实验装置。现提供以下药品:甲酸、浓硫酸、无水硫酸铜、氧化铜粉末、澄清石灰水。将所用仪器的序号按连接顺序由上至下依次填入下表(可以不填满),并写出该仪器中应加试剂的名称或化学式(划横线部分不需要填写)。___
| 选用的仪器 | 加入的试剂 |
| A | 甲酸、浓硫酸 |
| D | -- |
证明有一氧化碳生成的现象是___。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸制得四水甲酸铜[Cu(HCOO)2⋅4H2O]晶体。查阅资料可知四水甲酸铜晶体为浅蓝色晶体,可溶于水,难溶于醇。
相关的化学方程式是:2CuSO4+4NaHCO3=Cu(OH)2⋅CuCO3↓+3CO2↑+2Na2SO4+H2O;Cu(OH)2⋅CuCO3+4HCOOH+5H2O=2Cu(HCOO)2⋅4H2O+CO2↑
实验步骤如下:
Ⅰ.碱式碳酸铜的制备:
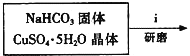
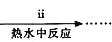

①步骤ⅰ是将一定量CuSO4⋅5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是___。
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃-80℃,如果看到___(填写实验现象),说明温度过高。
Ⅱ.甲酸铜的制备:将Cu(OH)2⋅CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的 时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2-3次,晾干,得到产品。
时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2-3次,晾干,得到产品。
③制取甲酸铜时需要趁热过滤的原因是___。
④用无水乙醇洗涤晶体的目的是___
-
甲酸(化学式HCOOH,分子式CH2O2,相对分子质量46),俗名蚁酸,是最简单的羧酸,无色而有刺激性气味的易挥发液体。熔点为8.6 ℃,沸点100.8℃,25℃电离常数Ka=1.8×10-4。某化学兴趣小组进行以下实验。
Ⅰ.用甲酸和浓硫酸制取一氧化碳
A. 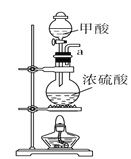 B.
B. 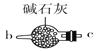 C.
C. 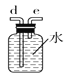 D.
D. 
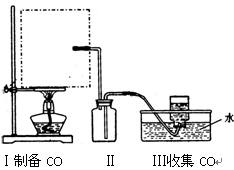
(1)请说出图B中盛装碱石灰的仪器名称__________。用A图所示装置进行实验。利用浓硫酸的脱水性,将甲酸与浓硫酸混合,甲酸发生分解反应生成CO,反应的化学方程式是________;实验时,不需加热也能产生CO,其原因是_______。
(2)如需收集CO气体,连接上图中的装置,其连接顺序为:a→__________(按气流方向,用小写字母表示)。
Ⅱ.对一氧化碳的化学性质进行探究
资料:ⅰ.常温下,CO与PdCl2溶液反应,有金属Pd和CO2生成,可用于检验CO;
ⅱ.一定条件下,CO能与NaOH固体发生反应:CO+NaOH HCOONa
HCOONa
利用下列装置进行实验,验证CO具有上述两个性质。
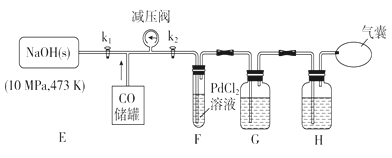
(3)打开k2,F装置中发生反应的化学方程式为_____________;为了使气囊收集到纯净的CO,以便循环使用,G装置中盛放的试剂可能是_________,H装置的作用是____________。
(4)现需验证E装置中CO与NaOH固体发生了反应,某同学设计下列验证方案:取少许固体产物,配置成溶液,在常温下测该溶液的pH,若pH>7,证明CO与NaOH固体发生了反应。该方案是否可行,请简述你的观点和理由:________,_________。
(5)25℃甲酸钠(HCOONa)的水解平衡常数Kh的数量级为____________。若向100ml 0.1mol.L-1的HCOONa溶液中加入100mL0.2mol.L-1的HCl溶液,则混合后溶液中所有离子浓度由大到小排序为_________。
-
苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理及装置示意图(加热、 夹持及辅助仪器省略)和一些相关信息如下:

| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 溶解性 |
| 水 | 乙醇 |
| 甲苯 | 无色液体易燃易挥发 | ﹣95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 112.4(100℃左右升华) | 248 | 1.2659 | 微溶 | 易溶 |
苯甲酸在水中的溶解度如表:
| 温度/℃ | 4 | 18 | 75 |
| 溶解度/g | 0.2 | 0.3 | 2.2 |
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
Ⅰ.在b 中加入 2.7 mL 甲苯、100 mL水和几片碎瓷片,开动电动搅拌器,a中通水。将b 中的液体加热至沸腾,分批加入 8.5 g 高锰酸钾,继续搅拌约5 h,停止加热和搅拌,静置。
Ⅱ.在反应混合物中加入一定量草酸(H2C2O4)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,再用浓盐酸酸化,苯甲酸全部析出后减压过滤,冷水洗涤,干燥,得到粗产品。
Ⅲ.称取m g产品,配成 100 mL乙醇溶液,移取25.00 mL溶液于锥形瓶,滴加2~3滴酚酞,然后用标准浓度KOH溶液滴定。请回答下列问题:
(1)装置a的作用___________
(2)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐和无色气体生成。加入草酸的作用_______,请用离子方程式表示该反应原理_____。
(3)产品减压过滤时用冷水洗涤的原因是_____________
(4)选用下列________(选填字母)操作,可以将粗产品进一步提纯。
A 溶于水后过滤 B 溶于乙醇后蒸馏
C 用甲苯萃取后分液 D 升华
(5)测定纯度步骤中,滴定终点溶液的颜色变化是__。若m=1.200 g,滴定时用去0.1200 mol·L-1 标准KOH溶液20.00 mL,则所得产品中苯甲酸的质量分数为______。
-
(15分)某兴趣小组利用以下实验装置模拟工业炼铁的主要过程:
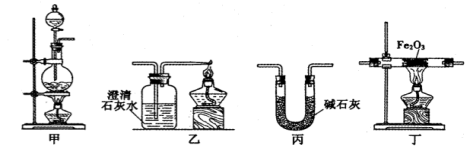
(1)装置甲中发生的反应为:HCOOH(甲酸) CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该 (填字母)。
CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该 (填字母)。
a.将甲酸滴入浓硫酸
b.将浓硫酸滴入甲酸
c.将甲酸与浓硫酸混合后加入
(2)请按合适的顺序连接好以下装置:甲→( )→( )→( )
(3)丙装置中碱石灰的作用是 。
(4)实验将近完成时,熄灭装置甲、乙、丁中酒精灯的先后顺序为 。
(5)为了探究影响反应产物的外界因素,在Fe2O3与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
| 加热方式 | 通CO加热 时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
①甲同学猜想黑色产物中可能含有碳单质。乙同学排除了该可能,他提出的两种理由是 、 。
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假设:
i.全部为铁;
ii. ;
iii. 。
-
(16分)某兴趣小组利用以下实验装置模拟工业炼铁的主要过程:
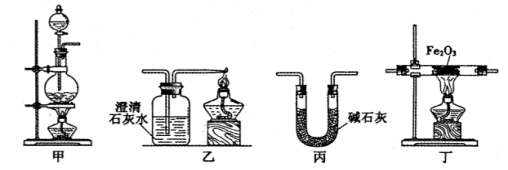
(1)装置甲中发生的反应为:HCOOH(甲酸) CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该 (填字母)。
CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该 (填字母)。
a.将甲酸滴入浓硫酸 b.将浓硫酸滴入甲酸 c.将甲酸与浓硫酸混合后加入
(2)请按合适的顺序连接好以下装置:甲→( )→( )→( )
(3)丙装置中碱石灰的作用是 。
(4)实验将近完成时,熄灭装置甲、乙、丁中酒精灯的先后顺序为 。
(5)为了探究影响反应产物的外界因素,在Fe2O3,与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
| 加热方式 | 通CO加热 时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
①甲同学猜想黑色产物中可能含有碳单质。乙同学排除了该可能,他提出的两种理由是: 、 。
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假设:i.全部为铁;ii. ;iii. 。
③通过进一步定量实验,黑色产物所含元素组成和质量分数如下:
| 样品序号 | 加热方式 | 元素组成和质量分数 |
| 产物样品I | 酒精灯 | w(Fe)=74.4%、w(O)=25.6% |
| 产物样品II | 酒精喷灯 | w(Fe)=100% |
样品I的成分及质量分数为 。
-
某兴趣小组利用以下实验装置模拟工业炼铁的主要过程:

(1)装置甲中发生的反应为:HCOOH(甲酸) CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该______________(填字母)。
CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该______________(填字母)。
a.将甲酸滴入浓硫酸 b.将浓硫酸滴入甲酸 c.将甲酸与浓硫酸混合后加入
(2)请按合适的顺序连接好以下装置:甲→(_____)→(_____)→(_____)
(3)丙装置中碱石灰的作用是__________________________。
(4)实验将近完成时,熄灭装置甲、乙、丁中酒精灯的先后顺序为__________。
(5)为了探究影响反应产物的外界因素,在Fe2O3,与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
| 加热方式 | 通CO加热时间/min | 澄清石灰水变浑浊时间/min | 产物颜色 | 产物能否全部被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
①甲同学猜想黑色产物中可能含有碳单质。乙同学排除了该可能,他提出的两种理由是:____、____。
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假设:i.全部为铁;ii.________;iii.___________。
③通过进一步定量实验,黑色产物所含元素组成和质量分数如下:
| 样品序号 | 加热方式 | 元素组成和质量分数 |
| 产物样品I | 酒精灯 | w(Fe)=74.4%、w(O)=25.6% |
| 产物样品II | 酒精喷灯 | w(Fe)=100% |
样品I的成分及质量分数为______________________。
-
下列有关常见羧酸的说法中正确的是
A.甲酸是一种无色有刺激性气味的气体,易溶于水
B.乙酸的沸点小于丙醇,大于乙醇
C.苯甲酸的酸性比碳酸强,可以和碳酸氢钠反应制取CO2
D.乙二酸具有还原性,可以使酸性KMnO4溶液退色
H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃~90℃,再逐滴滴入甲酸。


O4+H2O

NaHCO3固体一起放到研钵中研磨,其目的是___________。






 B.
B.  C.
C.  D.
D.