-
已知A、B、C、D都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他3种元素既不在同一周期又不在同一主族。B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D原子的L层电子数与最外层电子数之比为4:1,其d轨道中有一对成对电子。请回答:
(1)A与C形成的共价化合物的分子式是 ,中心原子杂化类型是__ ,分子的立体结构是 ,是 分子(填“极性”或“非极性”)
(2)B与C比较,电负性较小的是 (填元素符号);B与C形成的化合物晶体类型是 。
(3)D位于元素周期表中第 族,D2+的结构示意图是 ,它的+3价离子的电子排布式为 。
(4)A与B形成的化合物分子极易溶于水,其原因 是 。
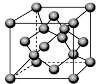
(5)由C原子构成的晶体中微粒间作用力是 ,右图是由C单质构成的晶体的一个晶胞,若设该晶胞的边长为a cm,NA表示阿伏加德罗常数,则该晶体的密度是 g/cm3.(只要求列出算式)。
-
(14分)A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大.B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族.B、C、D的最高价氧化物的水化物均能互相反应生成盐和水.A和E可形成离子化合物,其晶胞结构如下图所示:

(1)A、C、D、E四种元素依次是____ ____ ____ ____ (用元素符号表示)。
(2)上述四种元素ABCD中第一电离能最小的是________电负性最大的是________其原子半径由小到大的顺序为________________(均用元素符号表示)。
(3)A和D的氢化物中,前者沸点较高,原因是________________________________。
(4)A和E的化合物晶体中,每个阳离子的周围与它最近且等距离的阳离子共有个________。
-
(14分)Q、W、X、Y、Z均为元素周期表中前四周期元素,且其原子序数依次增大,Q元素的阳离子核外无电子,W元素原子的最外层电子数是其次外层电子数的2倍,Y是地壳中含量最多的元素,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
⑴W位于元素周期表第 周期第 族。Y的第一电离能 (填“大于”或“小于”)X的第一电离能。
⑵XQ3分子中的化学键类型为 (填“极性”或“非极性”)共价键,空间类型为 。Q—X﹑Q—Y﹑Q—W中键长最短的是 。
⑶Z的基态原子核外电子排布式是 ,Z的单质与X的最高价氧化物对应水化物的稀溶液反应的离子方程式为 。
⑷已知:①WQ4(g) +4XY2(g) ﹦4XY(g)+WY2 (g)+2Q2Y(g) △H﹦-574KJ·mol-1
②WQ4(g) +4XY(g) ﹦2X2 (g) +WY2 (g) +2Q2Y(g) △H﹦-1160KJ·mol-1
则由WQ4还原XY2生成X2的热化学方程式为 。
-
短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14。X是元素周期表中原子半径最小的元素,Z与X原子的最外层电子数相同,Y与W同主族。下列说法正确的是
A.Y与Z只能形成一种化合物
B.原子半径:r(Y)<r(Z)<r(W)
C.W的简单气态氢化物的热稳定性比Y的强
D.Z的最高价氧化物对应的水化物是碱
-
(14分)
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
(1)A基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形。
(2)某同学根据上述信息,所画的B电子排布图如图
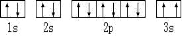
违背了 原理。
(3)F位于 族 区,其基态原子有 种运动状态。
(4)CD3 中心原子的杂化方式为 ,用价层电子对互斥理论推测其分子空间构型为 。
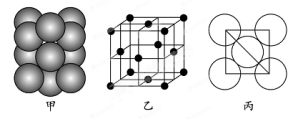
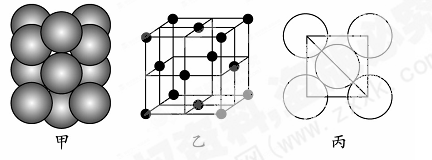
(5)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为 ,该单质晶体中原子的堆积方式为四种基本堆积方式中的 。若已知该金属的原子半径为d cm,NA代表阿伏加德罗常数,金属的相对原子质量为M,则该晶体的密度为______g·cm-3(用字母表示)。
-
(14分)现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
(1)A基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形。
(2)某同学根据上述信息,所画的B电子排布图如图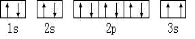 ,违背了 原理。
,违背了 原理。
(3)F位于 族 区,其基态原子有 种运动状态。
(4)CD3 中心原子的杂化方式为 ,用价层电子对互斥理论推测其分子空间构型为 ,检验E元素的方法是 。
(5)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为 ,该单质晶体中原子的堆积方式为四种基本堆积方式中的 。若已知该金属的原子半径为d cm,NA代表阿伏加德罗常数,金属的相对原子质量为M,则该晶体的密度为______g·cm-3(用字母表示)。
-
短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14。X是元素周期表中原子半径最小的元素,Z与X原子的最外层电子数相同,Y与W同主族。下列说法正确的是
A. X与Y只能形成一种化合物
B. 原子半径:r(Y)<r(W)<r(Z)
C. W的简单气态氢化物的热稳定性比Y的强
D. Z的最高价氧化物对应的水化物是酸
-
(14分) A、B、C、D、E是原子序数依次增大的短周期主族元素,A、D在周期表中的相对位置如下表;A元素最低负化合价的绝对值与其原子最外层电子数相等;C是地壳中含量最多的金属元素。
(1)A与氢元素组成的化合物分子有6个原子,其结构简式为_____________,写出该化合物在常温下使溴水褪色的化学方程式______________________________,该化合物还是一种重要的化工原料,写出其加聚生成高分子的化学方程式:____________________________。
(2)B元素的最高氧化物对应的水化物与它的氢化物反应得到离子化合物,则B元素的单质分子空间构型为___________,写出该单质的一种等电子体:_________________。
(3)C的离子结构示意图为____________,元素E在周期表中的位置是_________________。
-
(14分)
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大。其中A、C原子的L层有2个未成对电子。D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构。F3+离子M层3d轨道电子为半满状态。
请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出A、B、C三种元素电负性由大到小的顺序________。
(2)由A、B、C和氢四种元素组成的某种离子晶体,1mol该晶体含有配位键2mol,该晶体的化学式是________。
(3)F和Mn(锰)两元素的部分电离能数据列于下表:预测a________b(填“大于”、“小于”、“等于”),理由是________
________
| 元素 | Mn | F |
| 电离能 ( ) ) | I1 | 717 | 759 |
| I2 | 1509 | 1561 |
| I3 | a | b |
(4)AC2分子中σ键和π键数目比为________;
(5)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
H2S和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因是:
② 熔点、沸点差异的主要原因________
②在水中的溶解度差异的主要原因________
-
(14分)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子最外层电子排布为3s23p1,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)则W为 ,X为 ,Y为 ,Z为 。(填元素符号)
W的气态氢化物稳定性比H2O(g) (填“强”或“弱”)。
(2)Z原子的基态原子核外电子排布式是 ,Y的电负性比X的________(填“大”或“小”),W的第一电离能比O的 (填“大”或“小”)。
(3)X的最高价氧化物对应水化物与NaOH溶液反应的离子方程式是 。




 ,违背了
,违背了