-
氢气是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为______________;
②该反应的热化学方程式为________________________________;
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)= MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)= Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)= 2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
则ΔH2=____________kJ·mol-1;
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
(3)倒入NaOH溶液的正确操作是_______________(从下列选出)。
A.沿玻璃棒缓慢倒入 B.一次迅速倒入 C.分三次少量倒入
(4)使硫酸与NaOH溶液混合均匀的正确操作是_________(从下列选出)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃棒搅拌棒轻轻地搅动
高二化学填空题中等难度题查看答案及解析
-
氢气是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为______________;
②该反应的热化学方程式为________________________________;
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
则ΔH2=____________kJ·mol-1;
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
(3)倒入NaOH溶液的正确操作是_______________(从下列选出)。
A.沿玻璃棒缓慢倒入 B.一次迅速倒入 C.分三次少量倒入
(4)使硫酸与NaOH溶液混合均匀的正确操作是_________(从下列选出)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃棒搅拌棒轻轻地搅动
(5)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
起始温度t1/℃
终止温度
t2/℃
温度差平均值
(t2-t1)/℃
H2SO4
NaOH
平均值
1
26.2
26.0
26.1
30.1
______
2
27.0
27.4
27.2
33.3
3
25.9
25.9
25.9
29.8
4
26.4
26.2
26.3
30.4
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H=______________(取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是:___________。(任意写出一点)
高二化学填空题中等难度题查看答案及解析
-
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量______________生成物总能量(填“大于”,“小于”或“等于”)
②氢气的燃烧热为_________。 ③该反应的热化学方程式为___________________。
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为_____________kJ·mol-1
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=____________kJ·mol-1
高二化学填空题中等难度题查看答案及解析
-
氢气是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为________________
②该反应的热化学方程式为_____________________
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:Mg(s)+H2(g)=MgH2(s)ΔH1=-74.5kJ·mol-1,Mg2Ni(s)+2H2(g)=Mg2NiH4(s)ΔH2,Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1,则ΔH2=____________kJ·mol-1。
高二化学计算题简单题查看答案及解析
-
氢气是一种理想的绿色能源。
(1)在101kPa下,1 g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为_________________;②写出氢气燃烧热的热化学方程式__________________;
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,己知:
Mg(s)+H2(g)=MgH2(s) △H1=-74.5kJ•mol-1
Mg2Ni (s)+2H2(g)=Mg2NiH4(s) △H2;
Mg2Ni(s)+2MgH2(s)==2Mg(s)+ Mg2NiH4(s) △H3=+84.6 kJ•mol-1。
则△H2=______ kJ•mol-1;
(3)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,下图就是能够实现该转化的装置(其中电解质溶液为KOH溶液),被称为氢氧燃料电池。该电池的正极是____ (填a或b),负极反应式为________。该电池反应后溶液的pH将________(填“增大”“减小”或“不变”)
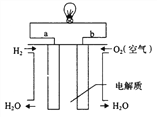
(4)若将上图中的氢氧燃料电池用固体金属氧化物陶瓷作电解质(能够传导O2-),己知正极上发生的电极反应式为:O2+4e-=2O2-则负极上发生的电极反应式为_______;电子从______极(填a或b)流出。该电池工作时,外电路每流过1 mol e-,消耗标况下氧气_____L。
高二化学简答题中等难度题查看答案及解析
-
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g 氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是
A.2H2+O2=2H2O ΔH=-142.9 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1
高二化学单选题中等难度题查看答案及解析
-
氢气是人类最理想的能源。已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是
A.2H2+O2 2H2O;△H =142.9kJ/mol
B.2H2(g)+O2(g) 2H2O(l);△H =-142.9kJ/mol
C.2H2(g)+O2(g) 2H2O(l);△H =-571.6kJ/mol
D.2H2(g)+O2(g) 2H2O(l);△H = +571.6kJ/mol
高二化学选择题简单题查看答案及解析
-
氢气是人类最理想的能源。已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是:
A.2H2 + O2=2H2O △H= –142.9 kJ/mol
B.2H2(g) + O2(g)=2H2O(l) △H= – 142.9 kJ/mol
C.2H2(g) + O2(g)=2H2O(l) △H= – 571.6 kJ/mol
D.2H2(g) + O2(g)=2H2O(l) △H = + 571.6 kJ/mol
高二化学选择题简单题查看答案及解析
-
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g 氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是( )
A.2H2+O2=2H2O ΔH=-142.9 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1
高二化学单选题中等难度题查看答案及解析
-
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是: ( )
A. 2H2(g)+O2(g)===2H2O(l) ΔH =-571.6 kJ/mol
B. 2H2(g)+O2(g)===2H2O(l) ΔH =-142.9 kJ/mol
C. 2H2+O2===2H2O ΔH =-142.9 kJ/mol
D. 2H2(g)+O2(g)===2H2O(l) ΔH =+571.6 kJ/mol
高二化学单选题简单题查看答案及解析