-
(14分)钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1mol·L-1的下列五种钠盐溶液的pH如下表;
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
上述盐溶液中的阴离子,结合H+能力最强的是_______ _,根据表中数据,浓度均为0.01mol·L—1的下列四种酸的溶液分别稀释100倍,pH变化最大的是________(填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100ml 0.1 mol/L NaHCO3 ②100ml 0.1 mol/L Na2CO3两种溶液,溶液中水电离出的H+个数:
① ②(填“>”、“=”或“<”,下同)。溶液中阴离子的物质的量浓度之和:① ②
(3)NaHCO3是一种 (填“强”或“弱”)电解质;写出HCO3―水解的离子方程式: ,常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3―、H2CO3、CO32―、OH― 五种微粒的浓度由大到小的顺序为: 。
(4)实验室中常用NaOH来进行洗气和提纯。
①当150ml 1mol/L的NaOH溶液吸收标准状况下2.24LCO2时,所得溶液中各离子浓度由大到小的顺序为
②几种离子开始沉淀时的PH如下表:
离子
Fe2+
Cu2+
Mg2+
pH
7.6
5.2
10.4
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时, (填离子符号)先沉淀,
Ksp[Fe(OH)2] Ksp[Mg(OH)2] (填“>”、“=”或“<”),要使0.2mol/L硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为 。(KspCu(OH)2=2×10-20mol2·L-2)
高二化学填空题困难题查看答案及解析
-
(10分)钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1mol·L-1的下列五种钠盐溶液的pH如下表;
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
上述盐溶液中的阴离子,结合H+能力最强的是_________,根据表中数据,浓度均为0.01mol·L—1的下列四种酸的溶液分别稀释100倍,pH变化最大的是________(填编号)。
A. HCN B. HClO C. CH3COOH D. H2CO3
(2)实验室中常用NaOH来进行洗气和提纯。
①当300mL 1mol·L-1的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为________________________________。
②几种离子开始沉淀时的pH如下表:
离子
Fe2+
Cu2+
Mg2+
pH
7.6
5.2
10.4
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时,_______(填离子符号)先沉淀,
_________
(填“>”、“=”或“<”)。
高二化学填空题简单题查看答案及解析
-
钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1mol/L的下列五种钠盐溶液的pH如下表;
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
上述盐溶液中的阴离子,结合氢离子能力最强的是 ,根据表中数据,浓度均为0.01mol/L的下列四种酸的溶液分别稀释100倍,pH变化最大的是 (填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100mL0.1mol/L碳酸氢钠 ②100mL0.1mol/L碳酸钠两种溶液,溶液中水电离出的氢离子个数:
① ② (填“>”“=”“<”下同)。溶液中阴离子的物质的量浓度之和:① ②。
(3)碳酸氢钠是一种 (填“强”或“弱”)电解质;写出HCO3-水解的离子方程式: ,常温下,0.1mol/L碳酸氢钠溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH-五种微粒的浓度由大到小的顺序为: 。
(4)实验室中常用氢氧化钠来进行洗气和提纯。
①当150mL1mol/L的氢氧化钠溶液吸收标况下2.24L二氧化碳时,所得溶液中各离子浓度由大到小的顺序为: 。
② 几种离子开始沉淀时的pH如下表:
离子
Fe2+
Cu2+
Mg2+
pH
7.6
5.2
10.4
当向含相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时, (填离子符号)先沉淀,Ksp[Fe(OH)3]
Ksp[Mg(OH)2] (填“>”“=”或“<”),要使0.2mol/L硫酸铜溶液中铜离子沉淀较为完全(使铜离子浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为 。
( Ksp[Cu(OH)2]=2×10-20mol2/L2)
高二化学填空题中等难度题查看答案及解析
-
钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1 mol/L的下列五种钠盐溶液的pH如表所示:
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
上述几种钠盐的阴离子,结合氢离子能力最强的是______(填离子符号),根据表中数据,将浓度均为0.01mol/L的下列四种溶液分别稀释100倍,pH变化最大的是______.(填字母)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)已知几种离子开始沉淀时溶液的pH如下表所示:
离子
Fe2+
Cu2+
Mg2+
pH
7.6
5.2
10.4
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,________(填离子符号)先沉淀;Ksp[Fe(OH)2]______(填“>”“=”或“<”)Ksp[Mg(OH)2];要使0.2 mol/L的硫酸铜溶液中铜离子沉淀较为完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液使溶液pH=_______。{Cu(OH)2的Ksp=2×10-20。}
高二化学综合题中等难度题查看答案及解析
-
常温下,浓度均为0.1mol/L的4种钠盐溶液pH如下:
溶质
Na2CO3
NaHCO3
NaClO
NaHSO3
pH
11.6
9.7
10.3
5.2
下列说法不正确的是
A. 四种溶液中,Na2CO3溶液中水的电离程度最大
B. NaHSO3溶液显酸性的原因是:电离程度大于水解程度
C. 常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3
D. 向氯水中加入少量Na2CO3(s),可以增大氯水中次氯酸的浓度
高二化学单选题中等难度题查看答案及解析
-
已知常温下,浓度均为0.1 mol·L-1的4种钠盐溶液pH如下表:
溶质
Na2CO3
NaHCO3
NaClO
NaHSO3
pH
11.6
9.7
10.3
5.2
下列说法中,正确的是
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HSO3-)>c(SO32-)>c(OH-)
高二化学选择题中等难度题查看答案及解析
-
完成下列各题.
(1)常温下,浓度均为 0.1mol•L﹣1 的下列五种钠盐溶液的 pH 如表;
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
上述盐溶液中的阴离子,结合H+能力最强的是 ,根据表中数据,浓度均为0.01mol•L﹣1 的下列四种酸的溶液分别稀释 100倍,pH变化最大的是 (填编号).
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100ml 0.1mol/L NaHCO3②100ml 0.1mol/L Na2CO3 两种溶液:
溶液中水电离出的OH-个数:① ②(填“>”、“=”或“<”,下同).
溶液中阴离子的物质的量浓度之和:① ②.
(3)NaCN遇水可产生易燃的HCN气体,浓度均为0.1mol/L的NaCN和HCN的混合液中滴加酚酞,溶液变红,则混合液中各离子的浓度大小关系为_______________________。
(4)研究证实,CO2可在酸性水溶液中通过电解生成甲醇(CH3OH),则生成甲醇的反应发生在 (填阴极或阳极),该电极反应式是 。
(5)已知Ksp(CuS)=1.3×10-36,Ksp(NiS)=1.0×10-24;在含Cu2+,Ni2+的溶液中,当Ni2+恰好完全沉淀[此时溶液中c(Ni2+)=1.0×10-5 mol·L-1],溶液中Cu2+的浓度是_____________mol·L-1。
高二化学填空题简单题查看答案及解析
-
完成下列各题.
(1)常温下,浓度均为 0.1mol•L﹣1 的下列五种钠盐溶液的 pH如表;
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
上述盐溶液中的阴离子,结合H+能力最强的是___________,根据表中数据,浓度均为0.01mol•L﹣1 的下列四种酸的溶液分别稀释 100倍,pH变化最大的是___________(填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100ml 0.1mol/L NaHCO3②100ml 0.1mol/L Na2CO3 两种溶液:
溶液中水电离出的OH-个数:①_________②(填“>”、“=”或“<”,下同)。溶液中阴离子的物质的量浓度之和:①__________②。
(3)NaCN遇水可产生易燃的HCN气体,浓度均为0.1mol/L的NaCN和HCN的混合液中滴加酚酞,溶液变红,则混合液中各离子的浓度大小关系为_______________________。
(4)研究证实,CO2可在酸性水溶液中通过电解生成甲醇(CH3OH),则生成甲醇的反应发生在_______ (填阴极或阳极),该电极反应式是_________________。
(5)已知Ksp(CuS)=1.3×10-36,Ksp(NiS)=1.0×10-24;在含Cu2+,Ni2+的溶液中,当Ni2+恰好完全沉淀[此时溶液中c(Ni2+)=1.0×10-5 mol·L-1],溶液中Cu2+的浓度是_____________mol·L-1。
高二化学填空题简单题查看答案及解析
-
碳及其化合物在能源、材料等方面具有广泛的用途。回答下列问题:
(1)碳酸和草酸均为二元弱酸,其电离分为两步进行,已知其电离常数的有关数据如下表:向Na2CO3溶液中滴加草酸溶液,开始时所发生反应的离子方程式为 。
H2CO3
H2C2O4
K1
4.2×10-7
5.4×10-2
K2
5.6×10-11
5.4×10-5
(2)常温时,C和CO的燃烧热△H分别为-394.0 kJ·mol-1、-283.0 kJ·mol-1,该条件下C转化为CO的热化学方程式为 。
(3)氢气和一氧化碳在一定条件下可合成甲醇,反应如下
2H2(g)+CO(g)
CH3OH(g) △H=Q kJ·mol-1。
①该反应在不同温度下的化学平衡常数(K)如下表:
温度(℃)
250
300
350
K(L2·mol-1)
2.041
0.270
0.012
由此可判断Q 0(填“>”、“=”或“<”)
②一定温度下,将6 mol H2和2mol CO充入到体积为2 L的密闭容器中,10 min时反应达到平衡状态,此时测得c(CO)=0.2 mol·L-1,该温度下的平衡常数K= 。0~10 min内,反应速率v(CH3OH)= 。
③在两个密闭容器中分别都充入20 mol H2和10 mol CO,测得一氧化碳的平衡转化率随温度(T)、压强(p)的变化如下图所示:
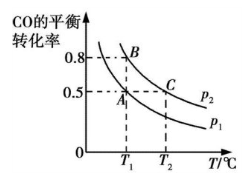
A、B两点压强大小关系:p1 p2(填“>”、“=”或“<”)。若A点对应容器的容积为20 L,则B点对应的容器的容积为 L。
高二化学填空题困难题查看答案及解析
-
25 ℃时,浓度均为0.1mol/L的下列五种钠盐溶液的pH如下表:
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
回答下列问题:
(1)下列反应不能发生的是: ;
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+HClO=CO2↑+H2O+ClO-
d.2ClO-+CO2+H2O=CO32-+2HClO
(2)体积为10 mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如右上图,则HX的电离平衡常数________(填“大于”、“等于”或“小于”)醋酸的平衡常数,写出HX的电离方程式 。
(3)某温度下,纯水中c (H+)=2.0×10-7 mol·L1, 0.9mol·L-1NaOH溶液与0.1mol·L-1HCl溶液等体积混合后(不考虑溶液体积变化),溶液的pH= 。
(4)等浓度等体积的CH3COONa和NaCN混合后,所得混合溶液中各离子浓度的大小关系是: 。
(5)某二元酸H2B在水中的电离方程式为H2B = H+ + HB— ;HB—
H++ B2—,则NaHB溶液显 (填“酸性”、“中性”或“碱性”)。
高二化学填空题困难题查看答案及解析