(7分)(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是________(填符号),画出配合物离子中的配位键________。
(2)根据价层电子对互斥理论,H30+中VSEPR模型名称为________,BCl3分子的立体结构为________。
(3)按要求写出由第二周期元素为中心原子,通过SP3杂化形成中性分子的化学式(各写一种):正四面体分子________,三角锥形分子________,V型分子________。
高二化学填空题简单题
(7分)(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是________(填符号),画出配合物离子中的配位键________。
(2)根据价层电子对互斥理论,H30+中VSEPR模型名称为________,BCl3分子的立体结构为________。
(3)按要求写出由第二周期元素为中心原子,通过SP3杂化形成中性分子的化学式(各写一种):正四面体分子________,三角锥形分子________,V型分子________。
高二化学填空题简单题
(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是____(填符号),配合物离子[Cu(NH3)4]2+为平面正方形结构, 画出其中的配位键_____________。
(2)配合物Co[(N3)(NH3)5]SO4中Co3+的配位数为___,Co3+与NH3之间的作用属于_____(选填“离子键”、“配位键”、“范德华力”、“氢键”)。
(3)Co(Ⅲ)的八面体配合物CoClm·nNH3,若1 mol配合物与AgNO3作用生成1 molAgCl沉淀,则m=__________, n= ___________。(填具体数值)
高二化学综合题困难题查看答案及解析
(7分)(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是________(填符号),画出配合物离子中的配位键________。
(2)根据价层电子对互斥理论,H30+中VSEPR模型名称为________,BCl3分子的立体结构为________。
(3)按要求写出由第二周期元素为中心原子,通过SP3杂化形成中性分子的化学式(各写一种):正四面体分子________,三角锥形分子________,V型分子________。
高二化学填空题简单题查看答案及解析
高二化学填空题中等难度题查看答案及解析
(1)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是__,画出配合物离子[Cu(NH3)4]2+中的配位键__.
(2)根据VSEPR模型,H3O+的分子立体结构为__,BCl3的立体结构为__.
(3)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种)
正四面体分子__,三角锥形分子__,V形分子______。
高二化学填空题中等难度题查看答案及解析
(14分)(1)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是___________________,[Cu(H2O)4]2+名称为________,画出该配离子中的配位键_________________________ 。
(2)根据VSEPR预测HCN的空间结构为形,其中C原子用于形成σ键的是________个________轨道,用于形成π键的是________个________轨道。
(3)根据甲醛的分子结构特点推测俗称光气的二氯甲醛分子(COCl2)结构式为________,中心原子杂化方式为________,空间结构为________形。
(4)按要求写出仅由第三周期非金属元素的原子构成且中心原子通过sp3杂化形成分子的化学式(各写一种):
正四面体分子_____________,三角锥形分子________________,V形分子___ ___________ ___。
高二化学填空题简单题查看答案及解析
(7分)(1)在配合物Ni(CO)4 和 [Cu(NH3)4]2+,[Fe(SCN)]2+配合物离子中,提供空轨道接受孤对电子的原子或离子分别是:________ _______、___________、_____________________ 。
(2)H3O+的空间构型为:___________ ________________,BCl3的空间构型为:___________
(3)按要求写出第二周期非金属元素构成的中性分子的化学式:(只需写一种)
平面三角形分子________________,三角锥形分子_________________________。
高二化学填空题中等难度题查看答案及解析
((9分) (1)在配合物离子(FeSCN)2+中,提供空轨道接受孤对电子的微粒是________。
(2)根据VSEPR模型,H3O+的分子立体结构为________,BCl3的构型为________。
(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有________(填序号)。
A.配位键 B.离子键
C.极性共价键 D.非极性共价键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为________。
(4)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一为绿色。两种晶体的组成皆为TiCl3?6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的2/3。绿色晶体配合物的化学式为________,由Cl所形成的化学键类型是________。
高二化学填空题困难题查看答案及解析
高二化学解答题中等难度题查看答案及解析
碳、氮、氧、氟、硫是中学常见的非金属元素,铁离子可与由它们组成的SCN﹣,CN﹣,F﹣等形成很多的配合物。
(1)基态Fe原子中,电子占据的最高能层符号为____,该能层具有的原子轨道数为_____,电子数为______。
(2)已知(CN)2是直线型分子,并有对称性,则(CN)2中π键和σ键的个数比为______,在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是______。
(3)配合物K4[Fe(CN)6]中不存在的作用力_______(填序号)。
A.共价键 B.离子键 C.非极性键 D.配位键
(4)写出一种与SCN﹣互为等电子体的分子_________(用化学式表示),该分子的空间构型为___________________。
(5)肼(N2H4)可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ·mol-1,若该反应中有4mol N-H键断裂,则形成的π键有________mol。
(6)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。
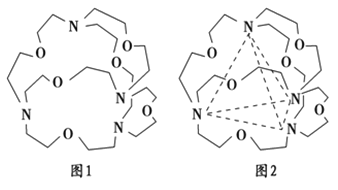
下列分子或离子中,能被该有机化合物识别的是_________(填标号)。
a. CF4 b. CH4 c. NH4+ d. H2O
高二化学解答题中等难度题查看答案及解析
下列说法中一定错误的是( )
A. 过渡金属的原子或离子一般都有接受孤电子对的空轨道,易形成配合物
B. 中心离子采取 sp3 杂化轨道形成的配离子可能呈正四面体结构
C. 当中心离子的配位数为 6 时,配离子常呈八面体结构
D. 含有两种配体且配位数为 4 的配离子一定存在异构体
高二化学单选题简单题查看答案及解析